
科目: 来源:高考三人行 化学 题型:022
已知30℃时几种盐的溶解度(g/100g H2O):

1862年比利时的索利维以CO2、NH3、水为原料制得纯净的Na2CO3,叫索尔维法,其主要操作是:①在氨化饱和NaCl溶液中通入CO2制得小苏打;②再把小苏打焙烧,制得纯碱,CO2循环使用;③在析出小苏打的母液中加入生石灰,NH3循环使用.
1943年我国著名科学家侯德榜先生,冲破了“索尔维法”的技术封锁,并加以改进,用固体NaCl代替生石灰加入母液中,使NH4Cl晶体析出,生产出纯碱和NH4Cl,这便是举世闻名的“侯氏制碱法”.
(1)写出在氨化饱和NaCl溶液中通入CO2的化学方程式:________,该方法能制得小苏打的原因是________.
(2)不能在NaCl溶液中先通入CO2,然后再通入NH3制得NaHCO3的原因是________.
(3)在析出小苏打后的母液中加入生石灰发生反应的化学方程式为________.
(4)“侯氏制碱法”的化学原理中涉及的化学反应类型有________.
(5)“两法”相比,侯氏制碱法的优点是________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
向碳酸钠浓溶液中缓慢滴入稀盐酸,直到不产生气体为止,这一过程中,溶液里原有阴离子数和生成的阴离子数的变化是________;用离子方程式解释为________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
A、B和C都是同一种金属的化合物,它们的焰色反应均呈黄色.根据下表中的实验记录,推断:A________B________C________D________(写化学式)并填写出各相应的化学方程式:

查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
向盛有水的试管里加入Na2O2,再向所得的溶液中滴加2滴酚酞,溶液先呈________色,但很快________,原因是________.该反应的离子方程式为________,电子转移数目为________,氧化剂为________,还原剂为________.
查看答案和解析>>
科目: 来源: 题型:022
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子的电子总数大4,1 mol A的单质跟足量盐酸反应可置换出11.2L(标准状况)氢气,这时A变成与氖原子具有相同电子层结构的离子.试回答:
(1)写出各元素的名称:A_______,B_______,C_______.
(2)分别写出A、B最高价氧化物对应水化物,分别跟C的气态氢化物水溶液反应的离子方程式_______,________.
(3)A离子的氧化性比B离子的氧化性_______(填“强”或“弱”),其原因是________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
碱金属能形成离子型氢化物.如氢化钠的化学式为NaH,其中H-具有较强的还原性.
(1)常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为________.
(2)NaH能与水剧烈反应生成对应的碱和氢气,反应的化学方程式为________,并在化学方程式中标明电子的转移方向和数目.该反应中氧化产物和还原产物的质量比为________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
把少量的金属钠分别放入下列溶液中,说明实验现象,并写出相应反应的离子方程式.
(1)钠放入Ca(HCO3)2溶液中,现象是________,离子方程式为________.
(2)钠放入稀盐酸中,现象是________离子方程式为________.
(3)钠放入CuSO4溶液中,现象是________,离子方程式为________.
查看答案和解析>>
科目: 来源: 题型:022
美国等国家发射的航天器将我国研制的磁谱仪带入太空,其目的是探索反物质.反物质的主要特征是电子带正电荷,质子带负电荷.
(1)以下表示反物质酸碱中和反应的通式是___________;
A.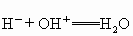
B.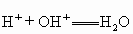
C.
D.
(2)若有α-粒子,它的质量数为_______,电荷数为_______;
(3)一对正负电子相碰发生了湮灭,转化为一对频率相同的光子,已知电子的质量为 ,普朗克常数
,普朗克常数 ,则这两个光子的频率约为______
,则这两个光子的频率约为______ (保留两位有效数字).
(保留两位有效数字).
查看答案和解析>>
科目: 来源: 题型:022
在1911年前后,新西兰出生的物理学家——卢瑟福把一束变速运动的α-粒子(质量数为4的带2个正电荷的质子),射向一片极薄的金箔.他惊奇地发现,过去一直认为原子是“实心球”,而由这种“实心球”紧密排列而成的金箔,竟为大多数α-粒子畅通无阻地通过,就像金箔不在那儿似的,但也有极少数的α-粒子发生偏转,或被笔直地弹回.根据以上实验现象能得出关于金箔中Au原子结构的一些结论,试写出其中的三点:
A_______________________________.
B_______________________________.
C_______________________________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
配平方程式:□FeS2+□O2→□Fe3O4+□SO2,其中还原剂是________,配平了的化学方程式中还原剂失去电子的总数是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com