
科目: 来源:高考三人行 化学 题型:022
已知SO2气体和H2S气体可以发生如下反应:
2H2S+SO2=3S+2H2O(1)常温下,向20L真空容器中通入a mol H2S和b mol SO2(a、b都是正整数,且a≤5,b≤5)反应完全后,容器内气体可能达到的最大密度为________g/L.
(2)在室温条件下,在一体积不变的密闭容器中充入H2S和SO2气体,反应前压强为P,反应结束后压强为![]() ,则反应前H2S和SO2的体积比是________或________.
,则反应前H2S和SO2的体积比是________或________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
在BaBr2溶液中滴入氯气,观察到现象是________,再通入SO2,观察到的现象是________,反应的离子方程式是:①________;②________;③________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
放射性同位素测定也是生物学研究和一种常用手段.科学家曾利用14C对河姆渡遗传稻谷的年代进行测定.稻谷中仅由C、H、O三种元素组成的有机物是脂肪和________,因而可对它们进行14C测定.
放射性同位素在遗传学研究上应用的一个典型事例是________实验,在该实验中,科学家利用了放射性35S和32P,从而得到了________的直接证据.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
A、B、C、D四种元素都是短周期元素.A元素的离子具有黄色的焰色反应.B元素的离子结构和Ne具有相同的电子层排布;5.8g B的氢氧化物恰好能与100mL 2mol/L盐酸完全反应,B原子核中质子数和中子数相等.H2在C单质中燃烧产生苍白色火焰.D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍.根据上述条件,回答:
(1)元素C位于第________周期________族,它的最高价氧化物的化学式为________.
(2)A是________元素,B是________元素,D是________元素.
(3)A与D形成稳定化合物的化学式为________,判断该化合物在空气中是否变质的简单方法是________.
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
科学家发现铂的两种化合物其化学式都为PtCl2(NH2)2,且均为平面正方形结构,但一种为黄绿色,在水中溶解度较大,具有抗癌作用,另一种为淡黄色,在水中溶解度较小,不具有抗癌作用.试回答下列问题:
(1)画出这两种铂的化合物的几何构型图.
黄绿色:________;淡黄色________.
(2)黄绿色固体在水中溶解度大的原因是________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
主族元素A、B、C、D的原子序数都小于18,A、D为同主族元素,B、C在同一周期,A、D原子价电子为1,C原子的最外层电子数比B原子的少2个,且最外层电子数是次外层电子数的2倍.A、B的单质在常温下都是气体,它们在高温下能以体积比2∶1完全反应,生成物在常温下是液体.此液体与D的单质能激烈反应生成A的单质,所得溶液滴入酚酞显红色,同时溶液中含有和氖原子的电子层结构相同的阳离子,回答下列问题:
(1)写出元素符号A________,B________,C________,D________.
(2)写出B与C在高温下完全反应生成物的分子式________,电子式________,结构式________.它是由________性键(填“极性”或“非极性”)结合的________分子,分子的构型为________.
(3)用电子式表示B、D在高温下形成的化合物的结构________,判断其中的化学键类型________.
(4)写出由A、B、C、D四种元素组成的化合物分子式________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
A、B、C、D、E、F、G为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
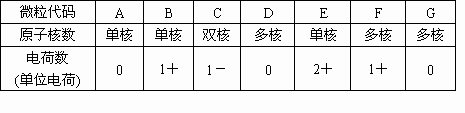
其中:B的离子半径大于E的离子半径;D是由极性键构成的4原子极性分子;C与F可形成D和G分子.
(1)A微粒的结构示意图是________.
(2)比较B与E相应元素的最高价氧化物对应水化物的碱性强弱,为:________>________(用化学式表示).
(3)D和G微粒是否为极性分子?答:________.
(4)C微粒是________,F微粒是________(用电子式表示).
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
氰(CN)2为无色可燃气体、剧毒、有苦杏仁味,和卤素单质的性质相似.
(1)写出氰与苛性钠溶液反应的离子方程式:________.
(2)已知氰分子键之间夹角为![]() 并有对称性,(CN)2的电子式为________,结构式为________,(CN)2分子为________(填“极性”或“非极性”)分子.
并有对称性,(CN)2的电子式为________,结构式为________,(CN)2分子为________(填“极性”或“非极性”)分子.
(3)CN-中电子数为________,CN-的电子式为________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
有4种化合物W(通常状况下是气态)、X(通常状况下是液态)、Y、Z(通常状况下是固态),它们共由5种短周期元素A、B、C、D、E组成.已知:①原子序数A<B<C<D<E,且A与D同族;C与E同族;B与C同周期.②W由A和B组成,且W分子中,A与B的原子个数比为4∶1;X由A和C组成,且X分子中A与C的原子个数比为1∶1;Y由C和D组成,属离子化合物,且测得Y固体中C与D的原子个数比为1∶1.③Z由D和E组成,属离子化合物,且其中阳离子比阴离子少1个电子层,阳离子数与阴离子数之比为2∶1.试推断写出:
(1)W的化学式是________,W属于________型化合物.
(2)X的电子式是________,X属于________型化合物.
(3)1mol Y在干燥的空气中质量会________(填“增大”或“减小”),其变化量(Δm)为________.
(4)用电子式表示化合物Z的形成过程________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
A、B、C三种元素为短周期元素.A元素的阴离子不能被任何氧化剂氧化,则A离子的结构示意图为________,它是________离子.1mol B单质能从盐酸中置换出3g氢气,此时B转变为与Ne原子具有相同电子层结构的离子,则B元素是________;B的最高价氧化物的对应水化物的化学式为________.C元素有3个电子层,且最外电子层比L电子层少2个电子,则C元素是________;C与Na反应后生成物的电子式为________,化合物中的化学键属于________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com