
科目: 来源:高考三人行 化学 题型:022
磷是存在于自然界和生物体内的重要元素,回答下列与磷及其化合物有关的问题.
(1)磷在自然界里主要以________的形式存在于矿石中.磷的单质有多种同素异形体,其中最常见的是有毒的________无毒的________.
(2)磷在不充足的氯气中燃烧的化学方程式为:________.
而在过量的氯气中燃烧的化学方程式则是:________.
(3)磷(相对原子质量为31)在空气中燃烧生成的氧化物通常可用做干燥剂.制备100g这种干燥剂所消耗的空气的体积约为________L(在标准状况下).
(4)有机磷农药“乐果”的结构简式是:
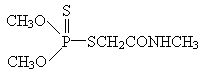 .其中所含的双键有________个.
.其中所含的双键有________个.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
矿泉水一般是由岩石风化后被地下水溶解其中可溶部分生成的.此处所指的风化作用是指矿物与水和CO2同时作用的过程.例如;钾长石(KAlSi3O8)风化生成高岭土[Al2Si2O5(OH)4],此反应的离子方程式为:2KAlSi3O8+2H2CO3+9H2O=2K++![]() +4H4SiO4↓+Al2Si2O5(OH)4↓.这个反应能够发生的原因是________.
+4H4SiO4↓+Al2Si2O5(OH)4↓.这个反应能够发生的原因是________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
某核素R具有微弱放射性,其原子核内中子数比质子数多43个,由它组成的固体单质A,在一定条件下密度为6.88g/cm3,用X射线研究其固体表明,在边长为1.00×10-7cm的立方体中含有20个原子.R在化学反应中常表现为+2价、+4价.在溶液中R2+稳定,而R4+有强氧化性.请回答:
(1)R原子的摩尔质量为________.
(2)R元素处于周期表中第________周期________族.
(3)将SO2通入到黑色的RO2悬浊液中,有白色沉淀生成,推测该反应的化学方程式:________.
(4)R3O4因具有氧化性(其氧化性强于硝酸),被大量用于油漆涂料,涂在钢铁表面,有利于形成耐腐蚀的钝化层.R3O4与足量的稀HNO3反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的方程式为:________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
某型号的水泥主要成分有:Ca2SiOx、Ca3SiOy、Ca3Al2Oz,则x=________,y=________,z=________.
水泥具有水硬性,跟水掺和搅拌后很容易________.
普通水泥以________和________为主要原料,在水泥回转窑中煅烧后,再加入适量的________,它的作用是________.
查看答案和解析>>
科目: 来源: 题型:022
高炉炼铁中发生的基本反应之一:
(正反应吸热),其平衡常数可表示为 ,已知1100℃时,K=0.263.
,已知1100℃时,K=0.263.
(1)温度升高,化学平衡移动后达到新的平衡,高炉内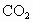 和CO的体积比值________,平衡常数K值________(“增大”“减小”或“不变”).
和CO的体积比值________,平衡常数K值________(“增大”“减小”或“不变”).
(2)1100℃时测得高炉中c(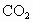 )=0.025
)=0.025 ,c(CO)=0.1
,c(CO)=0.1 ,在这种情况下,该反应是否处于平衡状态________(填“是”或“否”),此时,化学反应速率
,在这种情况下,该反应是否处于平衡状态________(填“是”或“否”),此时,化学反应速率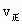 ________
________ (填“大于”“小于”或“等于”),其原因是_______________.
(填“大于”“小于”或“等于”),其原因是_______________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
锗是ⅣA族元素,它的单质晶体是一种良好的半导体材料,被广泛地应用在电子工业上.锗可以从燃烧的烟道灰中提取,其过程可表示如下:

根据以上实验过程,写出各步反应的化学方程式:①________;②________;③________;④________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
阅读下列材料,回答有关的问题.
锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡离子有强还原性,+4价铅元素的化合物有强氧化性.例如Sn2+还原性比Fe2+还原性强,PbO2的氧化性比Cl2氧化性强.
(1)写出下列反应的化学方程式:①氯气跟锡共热:________;②氯气跟铅共热:________;③二氧化铅跟浓盐酸共热:________.
(2)能说明Sn2+还原性比Fe2+还原性强的离子方程式为________.
查看答案和解析>>
科目: 来源: 题型:022
某化学反应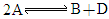 在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(
在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(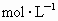 )随反应时间(min)的变化情况见下表.
)随反应时间(min)的变化情况见下表.
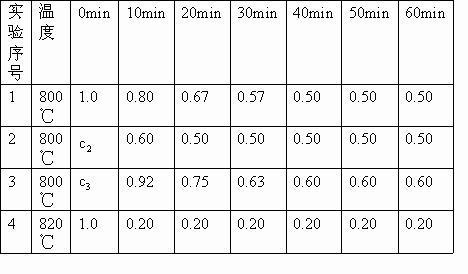
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20min时间内平均速率为_________ .
.
(2)在实验2中,A的初始浓度 =________
=________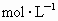 ,反应经20min就达到平衡,可推测实验2中还隐含的条件是________.
,反应经20min就达到平衡,可推测实验2中还隐含的条件是________.
(3)设实验3的反应速率为 ,实验1的反应速率为
,实验1的反应速率为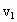 ,则
,则 ________
________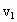 (填“>”=”或“<”),且
(填“>”=”或“<”),且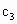 ________1.0
________1.0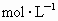 (填“>”“=”或“<”).
(填“>”“=”或“<”).
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”“放热”).理由是_______________________.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
在元素周期表中,位于第三周期第ⅣA族元素A的原子结构示意图是________.元素A的最高价氧化物的化学式是________.元素A的气态氢化物的稳定性比它上一周期同族元素E的气态氢化物________.与A相邻的同一周期的G、J两元素分别是________和________.A、E、G、J四种元素最高价氧化物对应水化物的化学式分别为________、________、________和________.在这四种物质中,________的酸性最弱,________的酸性最强.
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:022
某地有一池塘,生长着丰富的水生植物和多种鱼、虾.后来,由于化工厂将大量污水排入池塘中,使水质恶化,各种水生生物先后死亡.根据题意回答下列问题:
(1)从生态平衡角度看,池塘这种变化说明了________.
(2)造成这种变化的原因是________.
(3)经检测,污水中含有0.012mol/L的游离溴,可用亚硫酸钠除去污水中的溴,请写出其化学方程式:________.
(4)处理5L这种污水,需加入0.05mol/L的亚硫酸钠多少升才能将溴全部除去.
(5)要使池塘恢复本来面目,首先要解决的问题是________,首先要恢复的生物是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com