
科目: 来源: 题型:022
为制备MgNH4PO4,通常是往镁盐溶液中加入Na2HPO4、氨水和NH4Cl三种溶液,发生反应的化学方程式为:MgCl2+Na2HPO4+NH3=2NaCl+MgNH4PO4↓,由此可见,加入铵盐的目的是_______。
查看答案和解析>>
科目: 来源: 题型:022
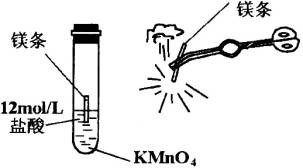
KMnO4可将12mol/L盐酸氧化成氯气。现将0.05gKMnO4固体和两段2cm长的镁条放入22mm×220mm的试管中,加入1.5mL12mol/L盐酸后立即盖上软木塞,并用一燃着的镁条在试管附近进行照射(见下图)。请回答下列问题:
(1)点燃镁条以后试管内最主要的现象是_______________。
(2)写出试管内全部反应的化学方程式_______________。
查看答案和解析>>
科目: 来源: 题型:022
为了将混有Na2SO4和NH4CO3的NaCl提纯,并制得纯净的NaCl溶液,某学生设计了如下实验方案:
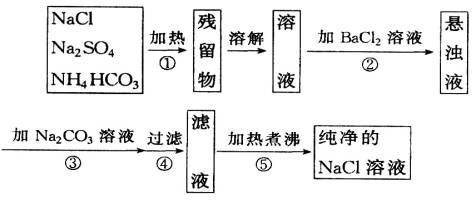
请回答:
(1)操作①加热时盛放药品的仪器应选用________(填仪器名称)。
(2)操作②能否选用其他试剂?简述理由。答:________。
(3)操作③的目的是什么?如何判断已经达到此目的?答:________。
(4)此实验方案设计是否严密?请说明理由。答:________。
查看答案和解析>>
科目: 来源: 题型:022
阅读下列材料,回答有关的问题
锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡离子有强还原性,+4价铅元素的化合物有强氧化性。例如:Sn2+还原性比Fe2+的还原性强。PbO2的氧化性比Cl2氧化性强。
(1)写出下列反应的化学方程式
①氯气跟锡共热:________________;
②氯气跟铅共热:________________;
③二氧化铅跟浓盐酸共热:________________。
(2)能说明Sn2+还原性比Fe2+还原性强的离子方程式是________。
查看答案和解析>>
科目: 来源: 题型:022
若把Fe3O4看作“混合氧化物”时可以写成FeO·Fe2O3,若看作一种盐时又可写出Fe(FeO2)2。根据化合价规则和这种书写方法,Pb3O4可以分别写出________和________。等物质的量的Fe3O4和Pb3O4分别和浓盐酸反应时,所消耗HCl的物质的量相等,不同的是,高价的铅能将盐酸氧化而放出氯气。试写出Fe3O4、Pb3O4分别和浓盐酸反应的化学方程式:________________________。
查看答案和解析>>
科目: 来源: 题型:022
古代的“药金”外观与金相似,常被误认为是金子。它的冶炼方法如下:将碳酸锌、赤铜[Cu2O]和木炭混合加热至800℃,得到金光闪闪的“药金”,则“药金”的主要成分是________,有关化学方程式是________,________,________。
查看答案和解析>>
科目: 来源: 题型:022
在配平KMnO4、H2O2、H2SO4三者反应的化学方程式时,出现多组配平的化学计量数,如:
①2KMnO4+7H2O2+3H2SO4=K2SO4+2MnSO4+10H2O+6O2↑
②2KMnO4+5H2O2+3H2SO4= K2SO4+2MnSO4+8H2O +5O2↑
③2KMnO4+9H2O2+3H2SO4= K2SO4+2MnSO4+12H2O +7O2↑
用H218O2进行示踪实验,证实生成的氧气全部是18O2,仅根据这一实验事实,回答下列问题:
①H2O2仅起还原作用的化学方程式是 。
②研究三个化学方程式中各组化学计量数的变化规律,写出符合该规律的一个新的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:022
在0.1 mol·L-1的酸醋中溶液中存在下列平衡:CH3COOH![]() CH3COO-+H+
CH3COO-+H+
当改变条件时,表中各项内容有何变化?
|
|
c(CH3COO-) |
c(H+) |
平衡移动方向 |
|
加纯CH3COOH |
|
|
|
|
加CH3COONa固体 |
|
|
|
|
加少量NaOH固体 |
|
|
|
|
加水稀释 |
|
|
|
|
加少量Zn粒 |
|
|
|
|
加少量HCL |
|
|
|
|
加热 |
|
|
|
查看答案和解析>>
科目: 来源: 题型:022
将等物质的量A、B、C、D四种物质混合,发生如下反应:aA+bB![]() cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了
cC(s)+dD,当反应进行一定时间后,测得A减少了nmol,B减少了![]() mol,C增加了
mol,C增加了![]() mol,D增加了nmol,此时达到化学平衡。
mol,D增加了nmol,此时达到化学平衡。
(1)该化学方程式中各物质的系数为:
a=___________,b=___________,c=___________, d=___________。?
(2)若只改变压强,反应速率发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A_________,B_________,C_________,D_________。
(3)若只升高温度,反应一段时间后,测得四种物质的量又达到相等,则该反应为_________反应(填“放热”或“吸热”)。
查看答案和解析>>
科目: 来源: 题型:022
在密闭容器中发生下列反应:
I2(g)+H2(g)
![]() 2HI(g)(正反应吸热)
2HI(g)(正反应吸热)
起始时,n(H2)=amol,n(I2)=bmol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变(“增大”“减小”或“不变”)填入相应的表格。
|
编号 |
反应条件 |
反应速率 |
|
(1) |
升高温度 |
|
|
(2) |
加入催化剂 |
|
|
(3) |
再充入a mol H2 |
|
|
(4) |
将容器容积扩大为原来2倍 |
|
|
(5) |
通入b mol N2(g) |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com