
科目: 来源:物理教研室 题型:022
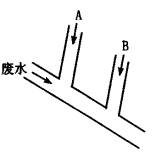
试回答:
(1)A处应注入________溶液,离子方程式为________;B处应注入________溶液,离子方程 式为_________。
(2)A处溶液的流量和B处溶液的流量分别应控制为多少(mL·s-1)?
查看答案和解析>>
科目: 来源:物理教研室 题型:022

现已用平底烧瓶收集得到CO2,在瓶内有一只紧扎在玻璃管末端的气球,如上图所示。打开塞子迅速往瓶里加入下列物质中的________(填序号),立即塞紧塞子,一段时间后,气球就会自动膨胀起来。
A.Na2O
B.Na2O2
C.KO2
D.RbO3
查看答案和解析>>
科目: 来源:物理教研室 题型:022
□FeSO4+□KNO3=□H2SO4→□k2SO4+□Fe2(SO4)3+□NxOy+□H2O
(1)推算出x=________,y=________。
(2)配平上述化学方程式,标出电子转移的方向和数目。
(3)反应中的氧化剂是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)反应前的O2的体积是(标准状况)________。
(2)化合物XY2的相对分子质量是________。
(3)若XY2分子中X、Y两元素的质量比是3:16,则X、Y两元素分别为________和
________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022

试回答:
(1)气体C是________,沉淀D是________。
(2)A中溶质的化学式是________。
(3)A与B混合时,生成不溶物的化学方程式是________。
(4)G中溶质转化为E中的溶质的离子方程式为________。
(5)F溶液中的主要溶质跟B的浓溶液反应的化学方程式为________。
(6)C与X生成D的化学方程式为:________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)某厂废水中含有KCN,其浓度为650 mg·L-1。现用氯氧化法处理,发生如下反应(其中N为-3价):KCN+2KOH+Cl2→KCNO+2KCl+H2O被氧化的元素是________。
(2)投入过量液氯,可将氰酸盐进一步氧化成为氮气。请配平下列化学方程式,并标出电子转移方向和数目:________。KCNO+KOH+Cl2—CO2+N2+KCl+H2O
(3)若处理上述废水20L,使KCN完全氧化转化为无毒物质,至少需液氯________g。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)计算20℃时饱和氯化钠溶液和盐酸溶液的物质的量浓度。
(2)通过计算说明20℃时,当氯气中混有氯化氢气体时,可以用饱和食盐水除去。
查看答案和解析>>
科目: 来源:物理教研室 题型:022

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上发生反应的化学方程式为____________,与电源负极相连的电极附近,溶液Ph________(选填“不变”“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+、SO42-等杂质。精制过程发生反应的离子方程式为________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去________,该钡试剂可以是________。
(选填“a”“b”或“c”,多选扣分)
A. Ba(OH)2 B. Ba(NO3)2 C. BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为____________。
(选填“a”“b”或“c”,多选扣分)
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、_______
除去NaCl。(填写操作名称)
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应,采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________
查看答案和解析>>
科目: 来源:物理教研室 题型:022
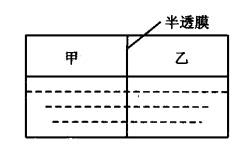
(1)若甲、乙室中装入的液体体积相同,对实验开始时的叙述正确的是( )
A. 水分子从甲室向乙室的扩散速度大于乙室向甲室的扩散速度
B. 水分子从乙室向甲室的扩散速度大于甲室向乙室的扩散速度
C. 两室中水分子的扩散速度相同
D. 两室中水分子的扩散速度将越来越小
(2)对于实验进行足够长时间后的情况预测正确的是( )
A. 最终两室水分子的相互扩散速度可以相等
B. 甲室中淀粉溶液的浓度始终不变
C. 甲室中淀粉溶液的体积将变大,乙室中水的体积将变小
D. 最终扩散将停止
查看答案和解析>>
科目: 来源:物理教研室 题型:022
已知反应A(g)+2B(g)![]() 2C(g),现向容器中加入6.5molA、xmolB、2.0molC。
2C(g),现向容器中加入6.5molA、xmolB、2.0molC。
(1)若x=5.5时,需要降低体系的温度使反应在平衡时达到题设条件,由正反应为 反应(填吸热或放热)。
⑵欲使起始反应维持向逆反应方向进行,则x的取值范围
。
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比通入D和E两种气体(此时容器内气体的总物质的量不要求保持12mol),按下式反应:D(g)+E(g)![]() 2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入mmolD
、nmolF和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为 mol(设A、B、C与D、E、F之间均不反应)。
2F(g),当反应达到平衡时,D在这三种物质中的体积分数为p%。若向容器中投入mmolD
、nmolF和一定量的E,在这三种物质新的平衡体系中,D的体积分数仍为p%。则投入E的物质的量为 mol(设A、B、C与D、E、F之间均不反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com