
科目: 来源:物理教研室 题型:022
甲:①取一定量的HA配制0.1mol×L-1的溶液100mL;
②用实验方法测出该溶液中的c(H+),即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制c(H+)=0.1mol×L-1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的c(H+)________0.1mol×L-1。(填“>”、“<”或“=”)
乙方案中,说明HA是弱电解质的现象是________。
a.装HCl溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两个试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现和不妥之处________、________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
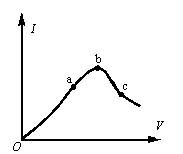
(1)“O”点导电能力为0的理由是:____________。
(2)a,b,c三点处,溶液的c(H+)由小到大的顺序为:____________。
(3)a,b,c三点处,醋酸的电离程度最大的是____________。
(4)若想使c点溶液中c(Ac-)增大,c(H+)减小,可采取的措施是____________。
a.加热 b.加水 c.加NaAc晶体 d.通入HCl气体 e.加入NaOH固体
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)醋酸和小苏打溶液混合:____________。
(2)HCN溶液和NaF溶液混合:____________。
(3)SO2通入CH3COONa溶液中:____________。
(4)H2SO3溶液存在的电离平衡:____________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
加入的物质 电离平衡移动方向 溶液中c(H+)变化
少量固体KOH
固体醋酸钠
同浓度的醋酸
少量盐酸溶液
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)用已准确称量的1.06gNa2CO3固体配制0.100mol•L-1Na2CO3溶液100mL,所需要的仪器为:________。
(2)除去NaNO3固体中混有的少量KNO3,所进行的实验操作依次为________、蒸发、结晶、________。
(3)除去KCl溶液中的SO42-,依次加入的溶液为(填溶质的化学式):________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022

(1)利用图8—9所示仪器可组成实验装置,则仪器的连接顺序为:________接________,________接________,________接________。
(2)写出实验步骤、现象和有关的化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com