
科目: 来源:高中化学必修2第一章《原子结构与元素周期律》单元测试卷 题型:022
麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗中感觉不到疼痛.
(1)一种常用的麻醉剂氯仿(CHCl3),常因保存不善而被氧化,产生剧毒物光气(COCl2).反应方程式为2CHCl3+O2![]() 2HCl+2COCl2.为防止发生事故,使用前可用于检验麻醉剂是否变质的试剂是(填序号)________.
2HCl+2COCl2.为防止发生事故,使用前可用于检验麻醉剂是否变质的试剂是(填序号)________.
A.淀粉碘化钾溶液
B.NaOH溶液
C.酚酞溶液
D.硝酸酸化的硝酸银溶液
(2)作为麻醉剂,疝气在医疗上很受重视,疝气能溶于细胞的油脂里,引起细胞麻醉和膨胀,从而神经末梢作用暂时停止.人们曾试用体积分数为80%疝气和20%的氧气组成的混合气体,作为无副作用的麻醉剂疝在元素周期表中位于________周期,________族,它的原子序数是________.
(3)作为稀有气体,氙的化学性质不活泼,但它可在一定条件下生成化合物.
取1 mol氙气和3.5 mol氟气于一密闭容器内充分反应,后来余下了1.5 mol的氟气同时有白色固体生成,此白色固体的化学式为________.
查看答案和解析>>
科目: 来源:高中化学必修2第一章《原子结构与元素周期律》单元测试卷 题型:022
A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,B、C、D同周期,A、D同主族,E与其它元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应.根据以上信息,回答下列问题:
(1)A和D的氢化物中,稳定性较弱的是________(选填A或D);A和B的离子中,半径较小的是________(填离子符号).
(2)元素C在元素周期表中的位置是________.
(3)E元素的名称是________.
查看答案和解析>>
科目: 来源:高中化学必修2第一章《原子结构与元素周期律》单元测试卷 题型:022
A、B、C、D、E、F、G为由七种短周期元素构成的粒子,它们都有10个电子,其结构特点如下表:

其中,B的离子半径大于E的离子半径;D是由极性键构成的4原子极性分子;C常用作F的检验(加热).请填写下列空白:
(1)A粒子的结构示意图________.
(2)比较BOH和E(OH)2的碱性强弱BC________EC2(填<、>、=).
(3)F与C反应的离子方程式:________
查看答案和解析>>
科目: 来源:高中化学必修2第一章《原子结构与元素周期律》单元测试卷 题型:022
在第三周期中,置换酸中氢的能力最强的元素的元素符号为________,化学性质最稳定的元素符号是________,最高价氧化物的水化物的酸性最强的化合物的化学式是________,碱性最强的化合物的化学式是________,显两性的氢氧化物的化学式是________,该两性氢氧化物与盐酸、氢氧化钠溶液分别反应的离子方程式为________.
________,原子半径最大的金属元素的名称是________,离子半径最小的离子结构示意图是________.
查看答案和解析>>
科目: 来源:高中化学必修2第一章 《物质结构 元素周期律》单元测试题 题型:022
A,B,C,D,E五种元素,它们的原子序数依次增大,A原子最外层有4个电子.B的阴离子与C的阳离子跟氟离子的电子层结构相同.E原子的M层上的电子数比次外层少1个电子.常温、常压下B单质是气体,0.1mol单质B与氢气完全反应时,有2.408×1023个电子发生转移.C的单质在高温下与B的单质充分反应之后,生成淡黄色固体F,F与AB2反应后可生成单质B.D的氢化物化学式是H2D,D的最高氧化物中含有40%的D,而且D原子是由相同数目的质子、中子、电子组成,根据以上的已知条件进行推测:
(1)下列元素的名称:D________,E________.
(2)写出下列的化学方程式:
B+C→F:________;
F与AB2反应:________.
查看答案和解析>>
科目: 来源:高中化学必修2第一章 《物质结构 元素周期律》单元测试题 题型:022
X、Y、Z是三种短周期的主族元素,原子序数:Z>X>Y,其中Y原子的次外层电子数为2,X与Y的族序数之和等于Z的族序数.已知X的氢氧化物A难溶于水,Y的最高价氧化物的对应水化物B是一种强酸.由此推知:X是________,Y是________,Z是________,A和B反应的离子方程式是________.
查看答案和解析>>
科目: 来源:高一化学期末试卷 题型:022
在水溶液中,YO3n-与S2-发生反应的离子方程式为:
YO3n-+3S2-+6H+请回答:
(1)此反应中,氧化剂是________.
(2)YO3n-中n=________.
(3)Y元素原子的最外层有________个电子,在周期表中位于________族.
查看答案和解析>>
科目: 来源:高一化学必修2月考1试题 题型:022
下表是元素周期表的前三周期:
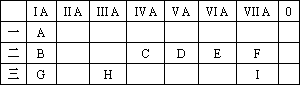
回答下列问题:
(1)G元素与E元素形成的化合物的化学式是________、________,它们都是________(填“共价化合物”或“离子化合物”)
(2)表格中十种元素的最高价氧化物对应的水合物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是________,属于两性氢氧化物的是________
查看答案和解析>>
科目: 来源:高一化学必修2月考1试题 题型:022
已知A、B、C、D、E是短周期中的5种非金属元素,它们的原子序数依次增大.A元素原子形成的阳离子核外电子数为零,C、D在元素周期表中处于左右相邻的位置,B原子的最外层电子数是内层电子数的2倍.E元素与D元素同主族;E的单质为黄色晶体,易溶于CS2.
(1)请写出元素符号:A________;B________;C________;D________;E________.
(2)画出E的阴离子的离子结构示意图________.
(3)C的气态氢化物的水溶液呈________性(填“酸”、“碱”或“中”),写出C的气态氢化物和HCl形成的盐X的电子式________.
查看答案和解析>>
科目: 来源: 题型:022
1869年,门捷列夫提出了“元素的性质随着相对原子质量的递增而呈周期性变化”的元素周期律,对照你的学习,在查阅元素周期表相对原子质量排布情况的基础上,探讨门氏周期律的科学性并与同学们交流你的意见。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com