
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
在烷烃分子中的基团:-CH3、-CH2-、![]() 、
、![]() 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如:

分子中,N1=6,N2=1,N3=2,N4=1.试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)中各原子数的关系.
(1)烷烃分子中氢原子数N0与N1、N2、N3、N4之间的关系是N0=________.
(2)4种碳原子数之间的关系为N1=________.
(3)若分子中N2=N3=N4=1,则该分子的结构简式可能为(任写一种)________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
已知某种气态矿物燃料含有碳和氢两种元素.为了测定这种燃料中碳和氢两种元素的质量,可将气态燃料通入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如下表所列的实验数据(假设产生的气体完全吸收).

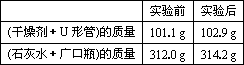
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g.假设广口瓶里生成一种正盐,其质量是________g.
(2)生成的水中氢元素的质量为________g.
(3)生成的CO2中碳元素的质量为________g.
(4)气态矿物燃料中碳元素与氢元素的质量比为________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便出现红棕色锈斑[该锈斑为Fe(OH)3失水的产物],试用有关的电极反应式、离子方程式和化学方程式表示Fe(OH)3的生成.
(1)负极________.
(2)正极________.
(3)离子方程式________.
(4)化学方程式________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
由铜片、锌片和200 mL稀H2SO4组成的原电池中,若锌片只发生原电池反应,当在铜片上放出3.36 L(标准状况)的H2时,H2SO4恰好用完,则产生这些气体消耗的Zn为________g,在导线上有________mol电子通过,原稀H2SO4的物质的量浓度是________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业作出了突出贡献.他利用NaHCO3、NaCl、NH4Cl等物质溶解度的差异,以食盐、氨气为原料先制得NaHCO3,进而生产出纯碱.侯氏制碱法的步骤如下(已知常温下1体积水可溶解700体积NH3).

试完成下列问题:
(1)上述悬浊液是NaHCO3和NH4Cl的混合液,则a和b两步的总反应方程式为:________.
(2)由这一反应可知NaHCO3溶解度比NaCl________.
(3)操作a、b的试剂不能颠倒的原因是________.
(4)操作c称作________,操作d称作________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
实验室利用下列装置和试剂制取少量氯化氢气体.

试剂:①浓硫酸;②浓盐酸;③食盐固体;④硫酸氢钠固体;⑤二氧化锰固体.
请用实验装置编号(A、B……)完成下列问题:
(1)若选用试剂①③,则应选择的装置是________.
(2)若选用试剂③④,则应选择的装置是________.
(3)若要快速制备氯化氢,应选择的装置是________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
丙酮(CH3COCH3)和碘在酸性溶液中发生如下反应:
CH3COCH3+I2![]() CH3COCH2I+H++I-
CH3COCH2I+H++I-
25℃时,该反应的速率由下式决定:
v=k·c(CH3COCH3)·c(H+)
上式中k=2.73×10-5 L·mol-1·s-1.已知开始时,c(I2)=c(H+)=0.01 mol·L-1,c(CH3COCH3)=0.1 mol·L-1.当碘反应了一半时,反应速率________(填“大于”“小于”或“等于”)开始时的反应速率,通过计算说明原因.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3,请完成下列问题.
(1)该化合物是由________键形成的.
(2)Na3N与盐酸反应生成________种盐,其化学式是________.
(3)Na3N与水的反应属于________反应.
(4)比较Na3N中两种粒子的半径:r(Na+)________r(N3-)(填“>”“=”或“<”).
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
在NaNO3、KOH、CH4、MgO、CH3COOH、CaF2、N2中,属于离子化合物的是________,属于共价化合物的是________,含有离子键的有________,含有共价健的有________.
查看答案和解析>>
科目: 来源:导学大课堂必修二化学鲁科版 鲁科版 题型:022
已知:A、B、C、D分别是中学化学中常见的四种不同粒子,它们之间有如下的反应关系:

(1)如果A、B、C、D均是10电子粒子,请写出:A的化学式________.
(2)如果A和C是18电子的粒子,B和D是10电子粒子,请写出:
①A与B在溶液中反应的离子方程式:________.
②根据上述离子方程式,可以判断C与B结合质子的能力大小是(用化学式或离子符号表示):________>________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com