
科目: 来源:2010年高二“每周一练”系列(15)化学试题 题型:022
烷烃A只可能有三种一氯取代产物B、C和D.C的结构简式是(CH3)2C(CH3CH2)CH2Cl.B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如下图所示.
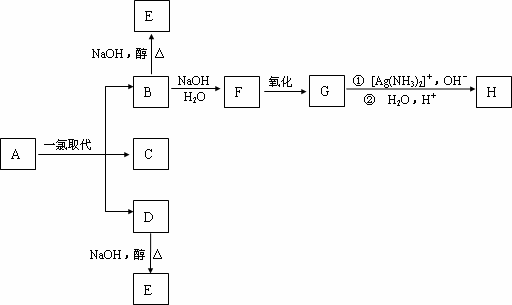
请回答:
(1)A的结构简式是________.
(2)H的结构简式是________.
(3)B转变为F的反应属于________反应(填反应类型名称).
(4)B转变为E的反应属于________反应(填反应类型名称).
(5)1.16 g H与足量NaHCO3作用,标准状况下可得CO2的体积是________mL.
查看答案和解析>>
科目: 来源:浙江省温州中学2011届高三年级上学期10月月考化学试题 题型:022
磷单质及其化合物有广泛应用.白磷(P4)是磷的单质之一,易氧化,与Cl2单质反应通常生成PCl3或PCl5.
(1)6.20 g白磷在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为________L.上述燃烧产物溶于水配成100.0 mL磷酸(H3PO4)溶液,需要的玻璃仪器除烧杯,玻璃棒外,还需要________,该磷酸溶液的物质的量浓度为________.
(2)含0.300 mol H3PO4的水溶液滴加到含0.500 mol Ca(OH)2的悬浮液中,反应恰好完全,生成l种难溶盐和16.2 g H2O.该难溶盐的化学式可表示为________.
(3)同磷灰石[主要成分Ca5(PO4)3F(s)]在高温下制备P4的化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)![]() 3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)上述反应中,副产物矿渣可用来________.
3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)上述反应中,副产物矿渣可用来________.
(4)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子产物,其结构式为________.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为________
.
(5)次磷酸钠(NaH2PO2)可用于化学镀镍.
化学镀镍的溶液中含有
Ni2+和H2PO2-,在酸性条件下发生下述反应,请配平该离子方程式.________Ni2++________H2PO2-+________→________Ni++________H2PO3-+________
查看答案和解析>>
科目: 来源:浙江省温州中学2011届高三年级上学期10月月考化学试题 题型:022
硝酸铜受热易分解:2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO
2CuO+4NO2↑+O2↑,当温度达到800℃时,CuO开始分解:4CuO![]() 2Cu2O+O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2
2Cu2O+O2↑,至1000℃以上,CuO完全分解(加热过程中忽略2NO2![]() N2O4,2NO2=2NO+O2等反应).
N2O4,2NO2=2NO+O2等反应).
现取5.64 g Cu(NO3)2无水晶体,在一定温度下使其分解,将生成的气体及时导出并用足量的NaOH溶液充分吸收.
(1)若该质量的无水硝酸铜经加热完全分解,其中的铜元素全部转化为氧化铜,则氧化铜的质量是________g.
(2)若该质量的无水硝酸铜完全分解,铜元素全部转化为氧化亚铜,反应过程中生成的气体被足量的NaOH溶液充分吸收后,还有多余的气体,则多余的气体是________(填分子式),其体积(标准状况)是________L.
(3)若该质量的无水硝酸铜分解后的残留固体中含有1.60 g CuO,则残留固体的质量可能是________g.
查看答案和解析>>
科目: 来源:浙江省金华一中2011届高三10月月考化学试卷 题型:022
美国科学家最近研究发现阿司匹林可降低患哮喘的风险.这项研究成果发表在《美国呼吸系统疾病护理医学杂志》上.阿司匹林(乙酰水杨酸)的合成原理是:
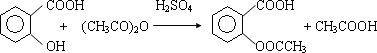
试回答下列问题:
(1)该反应的类型是________.
(2)反应中的4种有机物,遇FeCl3溶液显紫色的是(填名称)________.
(3)1 mol阿司匹林最多可与________mol NaOH溶液反应.
(4)同时符合下列3个条件的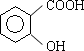 的同分异构体有________种.
的同分异构体有________种.
①遇FeCl3溶液显紫色
②苯环上含有两个取代基
③不能与NaHCO3反应产生气体,能发生银镜反应
查看答案和解析>>
科目: 来源:浙江省金华一中2011届高三10月月考化学试卷 题型:022
(1)请将下列5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式.
+________+________+________+H2O
(2)反应物中发生氧化反应的物质是________,被还原的元素是________.
(3)反应中1 mol氧化剂________(填“得到”或“失去”)________mol电子.
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中.
查看答案和解析>>
科目: 来源:浙江省杭州市西湖高级中学2011届高三上学期10月月考化学试题 题型:022
将固体FeC2O4·2H2O放在一个可称量的容器中加热灼烧,固体质量随温度升高而变化,测得数据如下:

根据计算分析推理,完成下列填空:
(1)写出25~300℃时固体发生变化的反应方程式________判断的理由是________.
(2)350~400℃发生变化得到的产物是________,物质的量之比为________.
(3)500℃时产物的含氧质量分数为________.
(4)写出600~900℃时发生变化的化学方程式________.
查看答案和解析>>
科目: 来源:浙江省杭州市西湖高级中学2011届高三上学期10月月考化学试题 题型:022
根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
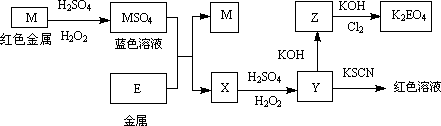
(1)写出M溶于稀H2SO4和H2O2混合液的化学方程式:________.
(2)某同学取X的溶液,酸化后加入KI、淀粉溶液,变为蓝色.写出与上述变化过程相关的离子方程式:________、________.
(3)写出Cl2将Z氧化为K2EO4的化学方程式:________.
查看答案和解析>>
科目: 来源:四川省成都外国语学校2011届高三10月月考化学试题 题型:022
(1)
在25℃时,浓度均为1 mol/L的①(NH4)2SO4、②(NH4)2CO3、③(NH4)2Fe(SO4)2溶液中,c(NH4+)由小到大的顺序是________(填编号)(2)
常温下将0.010 mol CH3COONa和0.004 mol HCl溶于水,配制成0.5 L混合溶液,判断:溶液中共有________种微粒(包括分子和离子);溶液中有两种微粒的物质的量之和一定等于0.010 mol,它们是________和________.溶液中n(CH3COO-)+n(OH-)-n(H+)=________.查看答案和解析>>
科目: 来源:山西省山大附中2011届高三10月月考化学试题 题型:022
某化学反应的反应物和产物如下:
KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(1)该反应的氧化剂是________.
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是________.
②在下面的化学式上标出电子转移的方向和数目
KMnO4+KI+H2SO4→(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组.原因是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com