
科目: 来源:山东省济南外国语学校2011届高三第一次质量检测化学试题 题型:022
(Ⅰ)实验室有贮存以下物质的方法,其中正确的是________(填序号)
①氢氟酸保存在细口玻璃瓶中
②浓硝酸用棕色瓶盛放,贮存在阴凉处
③少量液溴可用水封存,防止溴挥发
④氢氧化钠溶液贮存在带磨口玻璃塞的玻璃试剂瓶中
⑤在实验室少量的金属钠保存在煤油中
(Ⅱ)实验室制取0.5 mol/L的NaCl溶液500 mL,有以下仪器:
①烧杯
②100 mL量筒
③1000 mL容量瓶
④500 mL容量瓶
⑤玻璃棒
⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有________(填序号),还缺少的仪器是________.
(2)实验两次用到玻璃棒,其作用分别是________、________.
查看答案和解析>>
科目: 来源:山东省济南外国语学校2010-2011学年高二第一次质量检测化学试题 题型:022
下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
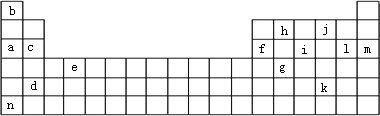
(1)e元素在周期表中的位置为________.画出g的原子结构示意图________.
(2)在上面元素周期表中画出金属元素与非金属元素的分界线.
(3)将元素a、f、h、b按原子半径从小到大的顺序排列________.(填元素符号)
(4)比较i和j形成的气态氢化物的稳定性________.(用化学式表示)
(5)比较i和l形成的最高价氧化物对应水化物的酸性________.(用化学式表示)
查看答案和解析>>
科目: 来源:山东省济南外国语学校2010-2011学年高二第一次质量检测化学试题 题型:022
已知A、B、C、D是中学化学中常见的四种不同微粒,它们之间存在如图所示的转化关系.
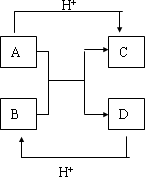
(1)如果A、B是10电子离子,C、D是10电子分子,A、B、C、D均含有两种元素.请写出A、B、C、D四种不同微粒的化学式:
A________、B________、C________、D________
.查看答案和解析>>
科目: 来源:山东省济南外国语学校2010-2011学年高二第一次质量检测化学试题 题型:022
(1)把卷成螺旋状的铜丝在酒精灯的火焰上加热,使表面变黑,然后速伸到无水酒精中,有什么现象________;写出有关反应的方程式________.由此可见,铜丝在反应中起________的作用.
(2)某元素R气态氢化合物的化学式RH3,其最高氧化物中含氧7/27,已知该元素的原子核中中子数和质子数相等,则该元素的相对原子质量是________,元素名称是________,请写出实验室制备RH3的化学方程式________,请写出RH3做还原剂所发生反应的化学方程式________.
查看答案和解析>>
科目: 来源:山东省济南外国语学校2010-2011学年高二第一次质量检测化学试题 题型:022
用下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是________
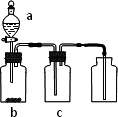

查看答案和解析>>
科目: 来源:山东省高青一中2009-2010学年度高一上学期期末模块检测考试化学试题 题型:022
阅读下面的元素周期表,按要求回答问题:

(1)在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)元素⑨在元素周期表中位于________周期________族,它属于________元素(填写“主族”、“副族”或“过渡”).
(3)元素①、④、⑤所形成的化合物中含有的化学键类型是________.
(4)比较元素⑥与元素⑦的金属性:⑥________⑦(填“<”“>”“=”),并设计一个实验加以证明:________
查看答案和解析>>
科目: 来源:山东省高青一中2009-2010学年度高一上学期期末模块检测考试化学试题 题型:022
铁是人类较早使用的金属之一.运用铁的有关知识,回答下列各题.
(1)据有关报道,目前已能冶炼出纯度高达99.999%的铁,下列关于纯铁的叙述中,正确的是________.
A.耐腐蚀性强,不易生锈
B.不能与盐酸反应
C.与不锈钢成分相同
D.在高温条件下能与水蒸气反应
铁的冶炼方法,除高炉炼铁外,还可以用金属铝将铁从其化合物中还原出来,请写出铝和Fe2O2反应的化学方程式:________.
(2)向沸水中逐滴滴加1 mol·L-1 FeCl2溶液,至液体呈透明的红褐色,形成该分散系的微粒直径的范围是________;向所得分散系中逐滴加入稀盐酸,现象是先产生红褐色沉淀;接着沉淀又逐渐溶解,生成棕黄色溶液,试解释此现象,并写出有关的化学方式.________.
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板.请写出
FeCl3溶液与铜反应的离子方程式:________;检验反应后的溶液中存在Fe3+的试剂是________.
(4)向氯化铁和氯化铜的混合溶液中,加入过量的Fe粉,若充分反应后溶液的质量没有改变,则原混合溶液中Fe3+和Cu2+物质的量浓度之比为________.
查看答案和解析>>
科目: 来源:山东省高青一中2009-2010学年度高一上学期期末模块检测考试化学试题 题型:022
已知:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在该反应中,________是氧化剂(填化学式,下同);________元素被氧化;氧化产物电子式是________;氧化剂和还原剂的物质的量之比为________;若有1 mol KMnO4参加了反应,则转移电子的数目是________.查看答案和解析>>
科目: 来源:宁夏银川二中2011届高三第一次月考化学试题 题型:022
根据下面物质间转换的框图,回答有关问题:

(1)由反应①产生的A、B混合物的工业名称是________.
(2)写出框图中D、E的化学式:D________;E________
(3)如果2 mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是多少________L,同时反应中转移电子总数是________.(NA表示阿佛加德罗常数)
(4)请设计一个简单易行的小实验,证明反应⑤是放热反应.实验方法是________
(5)如果A、B混合气体7.8 g(平均摩尔质量10 g·mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重________g,并得到O2________mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com