
科目: 来源:福建省三明一中2011届高三上学期第三次月考化学试题 题型:022
25℃时,①氢氟酸、②醋酸、③次氯酸的电离常数分别是3.5×10-4、1.8×10-5、3.0×10-8.请推测:它们的酸性由强到弱的顺序为________(填序号,下同),相同浓度的溶液中,氢离子浓度最大的是________,电离程度最小的是________;相同浓度的④氟化钠溶液、⑤醋酸钠溶液、⑥次氯酸钠溶液pH的从大到小顺序:________.
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高一上学期第二次月考化学试题 题型:022
下图是实验室制SO2并验证某些性质的装置图,试回答:
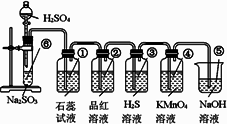
(1)⑥中发生的化学反应方程式为________.
(2)①中实验现象为________,证明SO2是________气体.
(3)②中品红溶液可观察到现象________,证明SO2有________.
(4)③中现象是________,证明SO2有________性.
(5)④中现象是________,证明SO2有________性.
(6)⑤的作用是________.反应的化学方程式为________.
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高一上学期第二次月考化学试题 题型:022
二氧化碳的过量排放,严重影响人类的生存环境,处理和利用二氧化碳是全球关注的重大问题,回答以下问题.
(1)大气中二氧化碳增加的原因有(答出一种即可)________.
(2)钟乳石和石笋的主要成分是碳酸钙.随着旅游人数的增加,潮湿溶洞中的钟乳石和石笋受到二氧化碳侵蚀,其化学反应方程式为:________.
(3)某学生提出一个修复溶洞底部受损石笋的研究方案,由以下五步组成,正确的实验步骤依次是________.修复时发生的离子反应方程式为________.
①将盛有碱溶液的容器置于石笋的上部;
②配制一定浓度的碱溶液;
③选择合适的碱;
④调节碱溶液下滴的速度;
⑤观察石笋表面复原情况
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高二上学期第二次月考化学试题 题型:022
用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取4.1 g烧碱样品,所用主要仪器是________.
(2)将样品配成250 mL待测液,需要的仪器有________.
(3)取10 mL待测液,用________量取.
(4)用0.2010 mol·L-1标准盐酸滴定待测烧碱溶液,滴定时________手旋转________式滴定管的玻璃活塞,________手不停地摇动锥形瓶,两眼注视________,直到滴定终点.
(5)根据下表数据,计算待测烧碱溶液的浓度:________.

(6)根据上述各数据,计算烧碱的纯度:________.
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高二上学期第二次月考化学试题 题型:022
在T℃下,某Ba(OH)2稀溶液中c(H+)=10-a mol/L,c(OH-)=10-b mol/L,已知a+b=12,向该溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如下表所示:

(1)依据题意判断,T℃________25℃(填“大于”、“小于”或“等于”),该温度下水的离子积KW=________.
(2)x=________,原Ba(OH)2稀溶液的物质的浓度为________.
(3)该温度下,向1 L硫酸与硫酸钠的混合溶液中加入3 L该Ba(OH)2稀溶液时,沉淀正好达到最大值,从所得溶液中取出4 mL并加水稀释至20 mL,测得溶液的pH为7,则原硫酸与硫酸钠混合溶液的pH为________,Na2SO4的物质的量浓度为________.
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高二上学期第二次月考化学试题 题型:022
一瓶溶液可能含有OH-、Cl-、CO32-、NO3-和SO42-离子中的一种或几种,取少许溶液分装于三支试管中,进行如下实验操作:
①第一支试管里滴加酚酞试液,溶液变红;加热浓缩、冷却.加足量浓H2SO4和铜片后加热,产生红棕色气体.
②第二支试管里逐滴加入稀硝酸,放出无色气体,该气体能使澄清石灰水变浑浊;继续加稀硝酸到溶液显酸性;加入硝酸钡或AgNO3溶液都不生成沉淀.
③第三支试管中加入Ba(NO3)2溶液,生成白色沉淀.
(1)写出上述三支试管中所发生反应的离子反应式.
①________;
②________;
③________.
(2)该试剂中肯定存在的阴离子是________,肯定不存在的离子是________.
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高二上学期第二次月考化学试题 题型:022
物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡.请根据所学知识回答:
(1)0.1 mol/L
的(NH4)2SO4溶液中各种离子浓度大小顺序为:________(2)0.1 mol/L NaHCO3溶液中存在的平衡有(用离子方程式表示):________
实验测得NaHCO3溶液的PH>7,请分析NaHCO3溶液显碱性的原因(用语言描述).
________
(3)将足量的BaCO3分别加入:
①30 mL H2O
②50 mL 0.01 mol/L氯化钡溶液
③100 mL 0.01mol/L盐酸中溶解.
请确定以上溶液中Ba2+的浓度最大的是________最小的是________(填写序号)
查看答案和解析>>
科目: 来源:福建省三明一中2010-2011学年高二上学期第二次月考化学试题 题型:022
如图所示,组成一种原电池.试回答下列问题(灯泡功率合适):
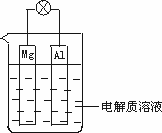
(1)电解质溶液为稀H2SO4时,灯泡________(填“亮”或“不亮”).若灯泡亮,则Mg电极上发生的反应为:________;Al电极上发生的反应为:________.若灯泡不亮,其理由为:________.
(2)电解质溶液为NaOH(aq)时,灯泡________(填“亮”或“不亮”).若灯泡亮,则Mg电极上发生的反应为:________;Al电极上发生的反应为:________.若灯泡不亮,其理由为:________.
查看答案和解析>>
科目: 来源:福建省古田一中2011届高三上学期期中考试化学试题 题型:022
某些化学反应可用下式表示
A+B→C+D+H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且氯在A的化合价介于C与D之间,写出该反应的离子方程式:________.
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,则A与B的组合是:
________或________.(写名称)
(3)若A为黑色固体,C是黄绿色的单质气体,写出该反应的离子方程式:________.
(4)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是________(写名称)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com