
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:022
已知元素的电负性和原子半径等内容一样,也是元素的一种基本性质.下面给出14种元素的电负性:
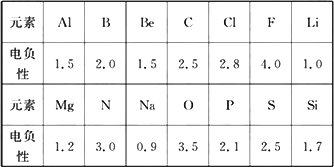
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是________;
(2)根据你的理解,元素的电负性指________;
(3)预测Br和I元素电负性的大小关系.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:022
氧化锑是一种新型的阻燃材料,运用于纺织、塑料工业.其中锑元素与氮元素同族.
(1)锑在元素周期表中的位置是第________周期第________族.
(2)锑的最高价氧化物的化学式是________,若该化合物中锑的质量分数为75.30%,则锑的相对原子量是________(保留4位有效数字).
(3)锑跟同周期的锡和碲相比较,元素的非金属性按照由强到弱的顺序排列是(用元素符号填空):________>________>________.
(4)硫化锑分散在水中可形成橙黄色的胶体,当用一束光线平射它时,发现有一条光亮的“通路”,这个现象叫做________现象.
(5)如在硫化锑胶体里插入两根石墨电极,通直流电后,在阳极附近颜色逐渐变深,这种现象叫做________,硫化锑胶体微粒带________电荷.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:022
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种元素为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________.
(2)ZW2的电子式是________.
(3)工业生产单质Y的原理是________(用化学方程式表示).
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是:________.
(5)0.1 mol的单质W与50 mL 1.5 mol/L的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是:________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:022
根据下表,用化学式或元素符号回答下列问题:
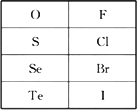
(1)还原性最强的离子是________;
(2)H2Te的稳定性比HI________;
(3)已知:2F2+2H2O![]() 4HF+O2,Cl2+H2S
4HF+O2,Cl2+H2S![]() 2HCl+S↓,完成下列化学方程式:
2HCl+S↓,完成下列化学方程式:
Br2+H2Se![]() ________;
________;
I2+H2Te![]() ________.
________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.3元素周期表及其应用(苏教版必修2) 题型:022
下表为元素周期表的一部分,请回答有关问题:
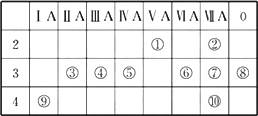
(1)⑤和⑧的元素符号是________和________;
(2)表中最活泼的金属是________,非金属性最强的元素是________(填写元素符号);
(3)表中能形成两性氢氧化物的元素是________,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应水化物反应的化学方程式:________,________;
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.2元素周期律(苏教版必修2) 题型:022
(思维拓展题)有A、B、C、D四种元素,其原子序数大小关系为A>B>C>D.已知:将0.5 mol A元素的最高价离子还原成中性原子时,需得到6.02×1023个电子.当A的单质同盐酸充分反应时可放出0.02 g氢气,用去0.4 g A单质.B元素原子的核外电子层数和A相同,并知B元素的原子半径比A大.C元素形成的氧化物既能溶于强酸,也能溶于强碱.D元素与氢气生成的化合物的化学式为DH3,其最高价氧化物中氧元素的质量分数为74.07%.试回答:
(1)元素符号:A________,B________,C________,D________.
(2)鉴定某物质中含有B元素的最简单的实验是________.
(3)A、B、C三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是(用化学式表示)________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.2元素周期律(苏教版必修2) 题型:022
根据周期表对角线规则,金属Be与Al单质及其化合物性质相似.试回答下列问题:
(1)写出Be与NaOH溶液反应生成Na2BeO2的离子方程式________.
(2)Be(OH)2与Mg(OH)2可用________试剂鉴别,其反应离子方程式为________.
(3)Li和Mg根据对角线规则,性质也相似,则Li在空气中燃烧,主要产物的化学式是________;同时还有少量________生成.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.2元素周期律(苏教版必修2) 题型:022
■有下列四种微粒:①![]() 、②
、②![]() 、③
、③![]() 、④
、④![]() .
.
(2)微粒中质子数小于中子数的是________.
(3)在化合物中呈现的化合价的数值最多的是________.
(4)能形成X2Y2型化合物的是________,能形成X3Y2型化合物的是________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.2元素周期律(苏教版必修2) 题型:022
A元素原子M电子层上有7个电子,B元素与A元素具有相同的电子层数,B元素的原子最外电子层只有1个电子.
(1)画出B元素的原子结构示意图________.
(2)A的最高价氧化物对应的水化物的化学式为________.
(3)实验室制取A的单质时,可以用B的最高价氧化物对应的水化物吸收尾气,该反应的化学方程式是________.
(4)B与水反应的离子方程式________.
查看答案和解析>>
科目: 来源:高一化学 专题1 微观结构与物质的多样性 1.1.1原子核外电子的排布(苏教版必修2) 题型:022
(思维拓展题)甲、乙、丙、丁是1~18号元素,乙元素原子有3个电子层,第一层与最外层电子数相等;甲元素原子的核外电子数比乙元素原子的核外电子数少1;丙元素原子的最外层电子数是次外层电子数的2倍;丁元素原子核电荷数比丙元素原子核电荷数多2.请回答:
(1)甲的单质与水反应的化学方程式为________;
(2)乙元素的原子结构示意图为________;
(3)丙元素的最高价氧化物可以和甲与丁两种元素形成的某种化合物反应生成丁单质,每生成1 mol丁单质,转移电子的数目约为________.
(4)写出一个能够证明乙单质的还原性比丙单质的还原性强的化学方程式________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com