
科目: 来源:安徽省蚌埠二中2011-2012学年高二第一次质检化学试题 题型:022
A、B、C、D、E均为有机化合物,它们之间的关系如图所示(提示:RCH=![]() 在酸性高锰酸钾溶液中反应生成RCOOH和
在酸性高锰酸钾溶液中反应生成RCOOH和![]() COOH,其中R和
COOH,其中R和![]() 为烷基).
为烷基).

回答下列问题:
(1)直链化合物A的相对分子质量小于90,A分子中碳、氢元素的总质量分数为0.814,其余为氧元素,则A的分子式为________;
(2)已知B与NaHCO3溶液完全反应,其物质的量之比为1∶2,请写出此反应的化学方程式是________.
(3)A可以与金属钠作用放出氢气,能使溴的四氯化碳溶液褪色,则A的结构简式是________.
(4)D的同分异构体中,能与NaHCO3溶液反应放出CO2的有________种.
查看答案和解析>>
科目: 来源:安徽省蚌埠二中2011-2012学年高二第一次质检化学试题 题型:022
有原子序数依次增大的四种短周期元素A、B、C、D.已知:
①A元素有三种同位素A1、A2、A3.其中自然界里最多的一种同位素A1的质量数分别是A2的1/2、A3的1/3.
②常温下,B元素的气态氢化物的水溶液pH>7.
③C元素的质子数等于A元素与B元素两者的质子数之和.
④金属元素D的原子核内质子数比上一周期同主族元素多8个,且单质D不能从硫酸铜溶液中置换出铜.
请回答下列问题:
(1)C元素在周期表中的位置是________.
(2)比较B、C、D相应的简单离子的半径,由大到小的顺序为________.
(3)请写出单质D与硫酸铜溶液反应的化学方程式________.
(4)A、B两种元素可以形成多种化合物,其中有一种离子化合物A中两元素的原子个数比为1∶5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构.写出A的电子式________.A物质与水反应生成一种碱和无色气体,写出有关的化学方程式________.
查看答案和解析>>
科目: 来源:浙江省温州中学2010-2011学年高一下学期期末考试化学试题 题型:022
以淀粉A为原料可以制得有茉莉花香味的H,现按以下方式进行合成该香料(方框中A、B、C、D、E、F均为有机物,同时方框中某些无机产物省略)
已知
:CH3CH2Cl+NaOH CH3CH2OH+NaCl
CH3CH2OH+NaCl
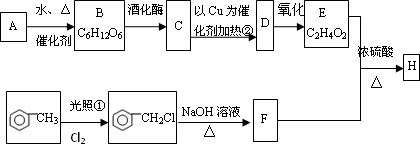
(1)A的化学式________,B的名称________.
(2)请写出①②的反应类型:①________,②________.
(3)C→D的化学方程式________,
(4)F+E→H的化学方程式________.
(5)写出C的两种同分异构体________.
查看答案和解析>>
科目: 来源:浙江省温州中学2010-2011学年高一下学期期末考试化学试题 题型:022
(1)某温度下,在一密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如下图所示.分析有关数据,写出X、Y、Z反应的化学方程式________.
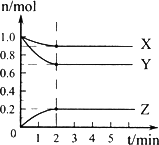
(2)下列情况可以证明(1)中的反应已达到平衡状态的是________(填序号).
A.物质的量浓度:c(X)=c(Y)=c(Z)
B.温度和体积一定时,某一生成物浓度不再变化
C.温度和体积一定时,容器内的压强不再变化
D.温度和体积一定时,混合气体的平均相对分子质量不再变化
(3)某温度下,在另一体积为2 L的密闭容器中充入2 mol X和3 mol Y,然后按(1)中的化学方程式进行反应,当达到化学平衡时,测得Z的物质的量的百分含量为25%,则平衡时X的物质的量浓度为________.
查看答案和解析>>
科目: 来源:浙江省温州中学2010-2011学年高一下学期期末考试化学试题 题型:022
能源是人类社会生活和社会发展的基础.请阅读以下材料,回答有关问题:
(1)在农村推广建造沼气池,不仅能有效地利用________能,还能为农业生产提供优良的肥料.已知标准状况下11.2 L甲烷完全燃烧生成液态水时放出445 kJ的热量,请写出甲烷燃烧的热化学方程式________.
(2)某研究人员设计了如图甲所示的甲烷燃料电池.则该燃料电池的负极是
________(填a或b).若以该电池为电源,石墨为电极电解CuCl2溶液(如图乙所示),则Y极上发生的电极反应式为________.若电解过程中共消耗标准状况下甲烷0.56 L,则理论上可析出金属铜________g(假设电解过程中总能量利用率为75%).
查看答案和解析>>
科目: 来源:浙江省温州中学2010-2011学年高一下学期期末考试化学试题 题型:022
下图是元素周期表的框架,依据元素周期表回答下列问题:

(1)周期表中的元素⑤和元素⑥的最高价氧化物的水化物碱性强弱顺序是________(用化学式表示),周期表中的元素④和元素⑦的氢化物的沸点高低顺序是________(用化学式表示).
(2)请写出②的氢化物的电子式________,③的氢化物的结构式________.
(3)①~⑦元素的单质,在常温下化学性质稳定,通常可用作保护气的是________(填写分子式).
(4)请写出工业上制备⑦单质的化学方程式________.
查看答案和解析>>
科目: 来源:浙江省效实中学2010-2011学年高一下学期期末考试化学试题 题型:022
下图中A~G均为中学化学中常见的物质,它们之间有如下转化关系.其中A、G为非金属单质,A为黑色固体、G为气态;D、F都是大气![]() 污染物,主要来源于汽车尾气,而且D为红棕色.请回答以下问题:
污染物,主要来源于汽车尾气,而且D为红棕色.请回答以下问题:
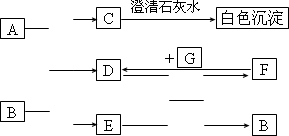
(1)A元素在元素周期表中位于________周期________族,C的化学式是________.
(2)写出D与E反应转化为F和B的化学方程式________.
(3)在常温下,B的稀溶液也可与Cu反应生成F.此反应的离子方程式:________.
查看答案和解析>>
科目: 来源:浙江省效实中学2010-2011学年高一下学期期末考试化学试题 题型:022
下表为元素周期表的一部分,请参照元素

①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑧的原子结构示意图为________.
(2)②的气态氢化物分子的结构式为________.
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是________.(填化学式)
(4)⑤、⑥元素的金属性强弱依次为________.(填“增大”、“减小”或“不变”)
(5)④、⑤、⑥的形成的简单离子半径依次________.(填“增大”、“减小”或“不变”)
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:________,形成的晶体是________晶体.
查看答案和解析>>
科目: 来源:江西省安福中学2011-2012学年高二上学期第一次月考化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:吉林省长春市十一中2011-2012学年高一上学期开学考试化学试题 题型:022
合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3.
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为________.
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为________(用小数表示,保留2位小数).
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉,发生如下反应:2Fe2O3+C 4FeO+CO2↑.为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为________g.
4FeO+CO2↑.为制得这种活性最高的催化剂,应向480 g Fe2O3粉末中加入炭粉的质量为________g.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com