
科目: 来源:河南省许昌四校2011-2012学年高二第一次联考化学试题 题型:022
现有反应:mA(g)+nB(g)?pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为________热反应,且m+n________p(填“>”、“=”“<”).
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”).
(3)若加入B(体积不变),则A的转化率________(填“增大”“减小”或“不变”).
(4)若升高温度,则平衡时B、C的浓度之比![]() 将________(填“增大”“减小”或“不变”).
将________(填“增大”“减小”或“不变”).
(5)若加入催化剂,平衡时气体混合物的总物质的量________(填“增大”“减小”或“不变”).
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色________(填“变深”、“变浅”或“不变”);而维持容器内压强不变,充入氖气时,混合物颜色________(填“变深”、“变浅”或“不变”).
查看答案和解析>>
科目: 来源:河南省许昌四校2011-2012学年高二第一次联考化学试题 题型:022
一定温度下,某2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:

(1)该反应的化学方程式为:________
(2)0~10 s时,平均反应速率v(Z)=________.
(3)0~10 s时,平均反应速率v(X)________v(Y)(填“>”、“<”、“=”)
查看答案和解析>>
科目: 来源:河北省正定中学2012届高三第三次月考化学试题 题型:022
A、B、C、D、E为短周期的五种元素,它们原子序数依次递增,B是构成有机物的主要元素;A与C可形成10电子化合物W,它可使紫色石蕊试液变蓝;D元素的原子最外层电子数是其次外层电子数3倍;E是同周期元素中原子半径最大的元素;A、B、C、D可形成化合物X,在X晶体中阳离子与阴离子个数比为1∶1;A、D、E可形成化合物Y.A、C、D可形成离子化合物Z.回答下列问题:
(1)Y的电子式:_________;W的空间构型:_________;
(2)写出Z的水溶液中各离子浓度由大到小的顺序:_________;
(3)写出常温下X与足量的Y在溶液中反应的离子方程式:_________;
(4)写出由A、B、D形成的化合物在一定条件下制取常见果实催熟剂的化学方程式:
(5)用石墨为电极电解Y的水溶液时,阳极的电极反应式为_________,一段时间后溶液的pH_________(从“增大”“减小”或“不变”中选填).
查看答案和解析>>
科目: 来源:江苏省江阴市一中2011-2012学年高二上学期期中考试化学(选修)试题 题型:022
某液态一卤代烃RX13.7 g与足量的NaOH醇溶液充分共热后,冷却并加入HNO3酸化,再滴入过量的AgNO3溶液,得到淡黄色沉淀18.8 g.则该卤代烃的分子式是________,其可能的结构有________种.
查看答案和解析>>
科目: 来源:江苏省江阴市一中2011-2012学年高二上学期期中考试化学(选修)试题 题型:022
白藜芦醇(如下图)广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性.能够跟1 mol该化合物起反应的Br2或H2的最大用量分别是________和________.
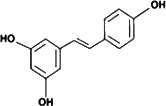
查看答案和解析>>
科目: 来源:江苏省江阴市一中2011-2012学年高二上学期期中考试化学(选修)试题 题型:022
某种混合物中可能含有甲酸、乙酸、甲醇及甲酸乙酯这些物质中的一种或几种.在检验时有以下现象:
(1)有银镜反应;
(2)加入新制Cu(OH)2悬浊液,无变澄清的现象;
(3)与含碱的酚酞溶液共热,发现溶液中红色逐渐变浅以至无色.
根据上述现象,可以判断:
此混合物中一定含有________,可能含有________,一定没有________.(填结构简式)
查看答案和解析>>
科目: 来源:江苏省江阴市一中2011-2012学年高二上学期期中考试化学(选修)试题 题型:022
下图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式:

(1)与足量的金属钠反应________
(2)与足量的氢氧化钠溶液反应________
(3)与足量的碳酸氢钠溶液反应________
查看答案和解析>>
科目: 来源:湖南省浏阳一中2011-2012学年高二第一次阶段性考试化学试题 题型:022
在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应.各物质的起始加入量如下:A、B和C均为4.0摩、D为6.5摩、F为2.0摩,设E为x摩.当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置.请填写以下空白:

(1)右侧反应的平衡常数表达式为K=________.
(2)若x=4.5,则右侧反应在起始时向________(填"正反应"或"逆反应")方向进行.欲使起始反应维持向该方向进行,则x的最大取值应小于________.
(3)若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量不相等,其理由是:________.
查看答案和解析>>
科目: 来源:湖南省浏阳一中2011-2012学年高二第一次阶段性考试化学试题 题型:022
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇.已知H2(g)和CH3OH(l)的燃烧热ΔH分别为-285.8 kJ·mol-1和-726.5 kJ·mol-1.请回答下列问题:
(1)用太阳能分解5 mol水消耗的能量是________kJ;
(2)ΔH表示甲醇燃烧热的热化学方程式为:________;
(3)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变得情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
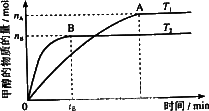
下列说法正确的是________(填序号)
①温度为T2时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=nB/tB mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的大
③该反应为吸热反应
④该反应为熵增加的反应
(4)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容器中,充分反应达到平衡后,若容器内的压强与起始压强之比为0.8,则平衡时甲醇的体积分数为________;
查看答案和解析>>
科目: 来源:浙江省嘉兴一中2011-2012学年高一10月月考化学试题 题型:022
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3中的一种或几种,现按下列步骤进行实验.
(1)将该粉末溶于水得无色溶液和白色沉淀.
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体.
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色的钴玻璃观察,未见紫色火焰.
由上述现象推断:该混合物中一定含有________;一定不含有________;可能含有________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com