
科目: 来源:福建省厦门六中2011-2012学年高二上学期期中考试化学理科试题 题型:022
下列八种晶体:
A.水晶、
B.冰、
C.氧化镁、
D.白磷、
E.晶体氩、
F.氯化铵、
G.铝、
H.金刚石.(用字母填空)
(1)属于原子晶体的化合物是________,由原子直接构成的分子晶体是________.
(2)由极性分子构成的晶体是________,含有离子键、共价键的化合物是________.
(3)在一定条件下能导电而不发生化学变化的是________,受热熔化需克服共价键的是________,含有氢键的是________.
查看答案和解析>>
科目: 来源:湖北省孝感高级中学2011-2012学年高一上学期期中考试化学试题 题型:022
现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠四瓶失去标签的溶液,将其编号为A、B、C、D.每次取少量溶液两两混合,所观察到的现象记录在下表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成).
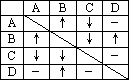
(1)据此推断这四瓶溶液中的溶质分别为(写化学式):
A________;B________;C________;D________;
(2)写出上述实验过程中有关物质间反应的离子方程式:
A+B:________
A+C:________
查看答案和解析>>
科目: 来源:河南省开封高中2011-2012学年高二上学期期中考试化学试题 题型:022
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)

根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=________,升高温度,K值________(填“增大”、“减小”或“不变”).
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是________
A.氢气的浓度减少
B.正反应速率加快,逆反应速率也加快
C.甲醇的物质的量增加
D.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:________(用化学方程式表示)
查看答案和解析>>
科目: 来源:河南省开封高中2011-2012学年高二上学期期中考试化学试题 题型:022
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
①该反应能否自发进行与________有关;
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是________(填字母,下同).
A.容器中的压强不变
B.1 mol H-H键断裂的同时断裂2 mol H-O键
C.
v正(CO)=v逆(H2O)D.c(CO)=c(H2)
(2)
将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)
①实验1中以v(CO2)表示的反应速率为________.
②该反应的逆反应为________(填“吸”或“放”)热反应
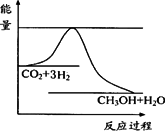
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化.在体积为1 L的
CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化.在体积为1 L的
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1 mol CO2和3 mol H2
查看答案和解析>>
科目: 来源:河南省开封高中2011-2012学年高二上学期期中考试化学试题 题型:022
25℃时,50 mL 0.1 mol/L醋酸中存在下述平衡:________.若分别作如下改变,对上述平衡有何影响?
(1)加入少量冰醋酸,平衡将________,溶液中c(H+)将________(增大、减小、不变);
(2)加入一定量蒸馏水,平衡将________,溶液中c(H+)将________(增大、减小、不变)
(3)加入少量0.1 mol/L盐酸,平衡将________,溶液中c(H+)将________(增大、减小、不变)
(4)加入20 mL 0.10 mol/L NaCl,平衡将________,溶液中c(H+)将________(增大、减小、不变)
查看答案和解析>>
科目: 来源:江苏省栟茶高级中学2011-2012学年高二上学期期中考试化学试题 题型:022
2010年第41届世博会将在上海举办,世博会的主题是“城市,让生活更美好”.回答下列问题:
(1)①世博园地区的改造提升了上海的环境质量,位于规划区的一座大型钢铁厂搬迁后,附近居民将不再受到该厂产生的红棕色烟尘的困扰.你认为棕红色烟尘是________.
A.CaCO3粉尘
B.P2O5粉尘
C.Fe2O3粉尘
D.SiO2粉尘
②上海白龙港污水处理厂升级改造,处理废水时加入明矾可作为混凝剂以吸附水中的杂质,明矾的化学式为________;明矾净水的原理是(用离子方程式表示)________.
③世博会期间,为了确保空气质量的优良率,人们需要定时测定空气中各种污染物的浓度来计算出空气污染指数.因此,人们需要监测的空气污染物除了可吸入颗粒物(PM10)、二氧化硫以外,还有________.
(2)世博会中国馆“东方之冠”,它由钢筋混凝土、7000多块红色铝板和1200多块玻璃等建成.
①钢筋混凝土________(选填“是”或“不是”)复合材料.
②生产硅酸盐水泥和普通玻璃都需要用到的主要原料是________.
③石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是________;有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种________(选填“橡胶”或“纤维”或“塑料”),有机玻璃是由甲基丙烯酸甲酯在一定条件下通过________反应合成的有机高分子材料.
(3)低碳经济是以低能耗、低污染、低排放为基础的经济模式,上海世博会的亮点之一是实现“二氧化碳零排放”.
①现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为________;人们已尝试使用________作为汽车燃料可真正实现“二氧化碳零排放”.
②世博停车场,安装有汽车尾气催化光解设施,它能将汽车尾气中CO和NOx反应生成可参与大气生态环境循环的无毒气体,写出CO和NOx在一定条件下反应的化学方程式:________.
③世博会期间将用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会证件及胸卡,目的是为了防止产生________污染.
查看答案和解析>>
科目: 来源:山西省忻州一中2011-2012学年高二上学期期中考试化学理科试题 题型:022
反应2A(g)+B(g)![]() 3C(g),起始时按5∶2的体积比把A、B两气体混合后,充入一体积不变的密闭容器中,在恒定温度下使之反应,达平衡时混合气体中C的体积分数为60%.(已知A、B的相对分子质量分别为a、b)则:
3C(g),起始时按5∶2的体积比把A、B两气体混合后,充入一体积不变的密闭容器中,在恒定温度下使之反应,达平衡时混合气体中C的体积分数为60%.(已知A、B的相对分子质量分别为a、b)则:
(1)该反应的平衡常数表达式为________
(2)A的转化率________;B的转化率________
(3)平衡时混合气体的平均相对分子质量________
(4)平衡时的压强与起始的压强相比________(填:较大、较小或相等)
查看答案和解析>>
科目: 来源:山西省忻州一中2011-2012学年高二上学期期中考试化学理科试题 题型:022
下图表示A~J之间的转化关系,E为常见的气体单质,G为金属单质,F的浓溶液在实验室常用做气体干燥剂,B、E反应t0~t3时刻物质的量及放出热量关系如下表所示(部分产物已略去):
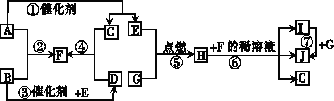
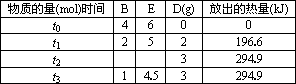
(1)写出F和J的化学式:F________,J________.
(2)不加限制地向大气中排放B,会造成的全球性环境问题是________(填一种),A适应绿色化工要求,常常被考虑用做绿色氧化剂,其原因是________
(3)①~⑥中不属于氧化还原反应的是________(填编号).
(4)反应③的热化学方程式为________.
查看答案和解析>>
科目: 来源:山西省忻州一中2011-2012学年高二上学期期中考试化学理科试题 题型:022
物质的量浓度相同的等体积的两份溶液A和B,A为盐酸,B为醋酸,分别和等质量的Zn反应,则下列说法正确的是:________
①产生的H2质量一定相同
②产生H2的质量一定不同
③仅有一份溶液中存在锌,则一定是盐酸
④等倍数稀释后的反应速率A>B
⑤产生等量H2所需时间A>B
⑥产生等量H2,盐酸和醋酸一定都有剩余
查看答案和解析>>
科目: 来源:山西省忻州一中2011-2012学年高二上学期期中考试化学理科试题 题型:022
在20 mL 0.1 mol/L CH3COOH溶液中逐滴加入0.1 mol/L NaOH溶液.
(1)当加入10 mL
NaOH溶液时,溶液呈酸性,则溶液中四种离子的浓度由大到小的顺序为:________.(2)当溶液呈中性时,加入的NaOH溶液的体积:VNaOH(aq)________20 mL(填:“>”或“<”或“=”).
(3)
当加入20 mL NaOH溶液时,c(CH3COOH)+c(CH3COO-)=________mol/L.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com