
科目: 来源:四川省南山中学2011-2012学年高一3月月考化学试题 题型:022
已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
①A+H2O→B+C
②C+F→D
③D+NaOH![]() F+E+H2O
F+E+H2O
(1)写出它们的化学式:A________、B________、D________、E________、F________;
(2)写出各步反应的离子方程式,并指反应①的氧化剂和还原剂物质的量比.
①________、氧化剂与还原剂物质的量比为:________.
②________.
③________.
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式________.
查看答案和解析>>
科目: 来源:四川省南山中学2011-2012学年高一3月月考化学试题 题型:022
(Ⅰ)A、B、C、D、E五种元素在周期表里的位置如下表所示:

A、B、C为同主族元素,A为该族中原子半径最小的元素;D、B、E为同周期元素,E为该周期中原子半径最小的元素.D元素名称是________,在周期表第________周期,第________族,其原子结构示意图________.
(Ⅱ)A、B、C、D、E、F六种短周期元素的原子序数依次增大.已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的次外层电子数比最外层电子数多3个.试回答:
(1)写出下列元素的符号A________,D________,E________.
(2)A、C两种元素最高价氧化物的水化物之间反应的离子方程式________.
查看答案和解析>>
科目: 来源:四川省南山中学2011-2012学年高一3月月考化学试题 题型:022
下表是周期表中的一部分,根据A-I在周期表中的位置,用元素符号或化学式回答下列问题:

(1)表中元素,化学性质最不活泼的是________,只有负价而无正价的是________,氧化性最强的单质是________,还原性最强的单质是________;
(2)最高价氧化物的水化物中碱性最强的是________,酸性最强的是________,呈两性的是________;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的________;
(4)在B、C、D、E、F、G、H中,原子半径最大的是________.最小的是________.
查看答案和解析>>
科目: 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
化合物H是一种香料,存在于金橘中,可用如下路线合成:
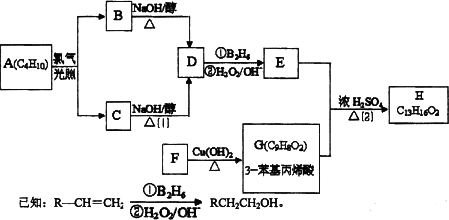
完成下列各题:
1.C4H10的一氯代烷的同分异构体有________种、九氯代烷的同分异构体有________种.
2.F的结构简式是________;反应(1)的反应类型是________;
3.反应(2)的化学方程式为________;
4.与G具有相同官能团的G的芳香类同分异构体共有________种(不包括G).
查看答案和解析>>
科目: 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
氮的氧化物和SO2是常见的化工原料,但也是大气的主要污染物.综合治理其污染是化学家研究的主要内容.根据题意完成下列各题:
1.用甲烷催化还原一氧化氮,可以消除一氧化氮对大气的污染.反应方程式如下:CH4(g)+4NO(g)![]() 2N2(g)+2H2O(g)+CO2(g)该反应平衡常数表达式为________.
2N2(g)+2H2O(g)+CO2(g)该反应平衡常数表达式为________.
2.硫酸生产中,接触室内的反应:2SO2(g)+O2(g)![]() 2SO3(g);SO2的平衡转化率与体系总压强的关系如图所示.某温度下,将2.0 mol SO2和1.0 mol O2置于30 L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是________mol·L-1·min-1.
2SO3(g);SO2的平衡转化率与体系总压强的关系如图所示.某温度下,将2.0 mol SO2和1.0 mol O2置于30 L刚性密闭容器中,30秒反应达平衡后,体系总压强为2.70MPa.用氧气表示该反应的平均速率是________mol·L-1·min-1.
3.下图平衡状态由A变到B时,改变的外界条件是________.
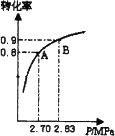
a.又加入一些催化剂
b.又加入一些氧气
c.降低了体系的温度
d.升高了外界的大气压
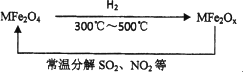
4.新型纳米材料氧缺位铁酸盐MFe2Ox在常温下,能将氮的氧化物和SO2等废气分解除去.转化流程如图所示,若x=3.5,M为Zn,请写出ZnFe2O3.5分解SO2的化学方程式________
查看答案和解析>>
科目: 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
________SiO2+________C+________N2![]() ________Si3N4+________CO
________Si3N4+________CO
根据题意完成下列各题:
1.配平上述化学反应方程式(若计量数为1不要填).
2.为了保证石英和焦炭尽可能的转化,氮气要适当过量.某次反应用了20 mol氮气,反应生成了5 mol一氧化碳,则反应中转移电子为________NA,此时混合气体的平均相对分子质量是________.
3.分析反应可推测碳、氮气的氧化性________>________(填化学式).
4.氮化硅陶瓷的机械强度高,硬度接近于刚玉(Al2O3),热稳定性好,化学性质稳定.以下用途正确的是________.
A.可以在冶金工业上制成坩埚、铝电解槽衬里等热工设备上
B.在电子工业上制成耐高温的电的良导体
C.研发氮化硅的全陶发动机替代同类型金属发动机
D.氮化硅陶瓷的开发,将受到资源的限制,发展前途暗淡
查看答案和解析>>
科目: 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
硅单质及其化合物应用范围很广.三氯硅烷(SiHCl3)还原法是目前工业制高纯度硅的主要方法,生产过程如下图:
根据题意完成下列备题:
1.硅在元素周期表的位置________,其最外层有________种能量不同的电子.
2.硅的气态氢化物为SiH4,其空间构型为________;三氯硅烷中某些元素最高价氧化物对应水化物的酸性________>________(填化学式).
3.写出三氯硅烷与氢气反应的化学反应方程式:________.
4.自然界中硅酸盐种类多,结构复杂,通常用二氧化硅和金属氧化物的形式来表示其组成.如正长石(KALSi3O8),氧化物形式为:________.
查看答案和解析>>
科目: 来源:上海市十三校2012届高三第二次联考化学试题 题型:022
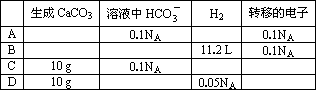
100 mL 1 mol·L-1的Ca(HCO3)2溶液中,放入2.3 g金属钠充分反应后,有关物质的物理量正确的是(NA表示阿伏加德罗常数)________
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011-2012学年高一上学期期末考试化学试题 题型:022
将标准状况下的11.2 L氨气溶于100 mL水中,得到密度为0.868 g·cm-3的氨水.
(1)该气体的物质的量=________mol;溶液的体积=________L;
所得氨水的物质的量浓度=________mol·L-1.
(2)若取上述氨水30.0 mL与70.0 mL 2.00 mol·L-1的AlCl3溶液相混合,产生白色沉淀的质量是________g.
(3)若取某浓度的NaOH溶液50.0 mL与50.0 mL 2.00 mol·L-1的AlCl3溶液相混合,有白色沉淀产生,测得溶液中铝元素与沉淀中铝元素质量相等,则NaOH溶液的物质的量浓度为________mol·L-1
查看答案和解析>>
科目: 来源:湖北省黄冈中学2011-2012学年高二上学期期中考试化学试题 题型:022
晶体的世界丰富多彩,晶体的结构纷繁复杂.人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、C sCl、CaF2.下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:

(1)描述晶体结构的________单元叫做晶胞,整块晶体可以看作是数量巨大的晶胞________而成的.
(2)某分子晶体的晶胞如上图(B、C球所代表的位置无该分子)所示,则该分子晶体是________;该分子晶体中,一个分子周围紧邻________个分子.
(3)若上图是NaCl的晶胞图,则A球代表________,B球代表________,C球代表________.
(4)若上图是金刚石的晶胞图,则碳原子处于________位置(选填“A球”、“B球”、“C球”).
(5)某金属晶体的晶胞如上图(A、C球所代表的位置无该金属原子)所示,则该金属晶体是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com