
科目: 来源:河北省冀州中学2010-2011学年高二下学期期末考试化学试题(A卷) 题型:022
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质);

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
(1)ⅡA族元素的价电子数( )
(2)ⅦA族元素氢化物的沸点( )
(3)第三周期元素单质的熔点( )
(4)第三周期元素的最高正化合价( )
(5)ⅠA族元素单质熔点( )
(6)F-、Na+、Mg2+、Al3+四种离子的离子半径( )
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一上学期期中考试化学试题(人教版) 人教版 题型:022
有A、B、C、D四种化合物,分别由K+、Ba2+、SO42-、CO32-、OH-中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊.
(1)推断A、B、C、D、E的化学式.
A________;B________;C________;D________;E________;
(2)写出下列反应的离子方程式.
B与盐酸反应________;
C与硫酸反应________;
D与硫酸反应________;
E与澄清石灰水反应________;
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一上学期期中考试化学试题(人教版) 人教版 题型:022
将适当的物质填在下边的横线上
(1)Cu2++________=Fe2++________;
(2)________+H+=________+H2O+CO2↑;
(3)HCO![]() +________=CO
+________=CO![]() +________;
+________;
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一上学期期中考试化学试题(人教版) 人教版 题型:022
下列离子均为中学化学常见的离子:Na+、Ba2+、Mg2+、Al3+、Fe3+、Cu2+、NH![]() 、H+、Cl-、NO
、H+、Cl-、NO![]() 、CO
、CO![]() 、HCO
、HCO![]() 、SO
、SO![]() 、OH-.上述离子中,在强酸性溶液里不可能大量存在的是________;在强碱性溶液中不可能大量存在的离子有________;既不能在强酸性溶液里大量存在,也不能在强碱性溶液里大量存在的是________;无论在强酸性溶液还是强碱性溶液里,都可以大量存在的是________.
、OH-.上述离子中,在强酸性溶液里不可能大量存在的是________;在强碱性溶液中不可能大量存在的离子有________;既不能在强酸性溶液里大量存在,也不能在强碱性溶液里大量存在的是________;无论在强酸性溶液还是强碱性溶液里,都可以大量存在的是________.
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一上学期期中考试化学试题(人教版) 人教版 题型:022
有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管;⑧细口试剂瓶;⑨标签纸.
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸________mL.(小数点后保留1位有效数字)
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是________.
(3)容量瓶使用前检验漏水的方法是________.
(4)若实验遇到下列情况,对所配制硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用以稀释硫酸的烧杯未洗涤________.
②未经冷却趋热将溶液注入容量瓶中________.
③摇匀后发现液面低于刻度线再加水________.
④容量瓶中原有少量蒸馏水________.
⑤定容时俯视观察液面________.
查看答案和解析>>
科目: 来源:福建省福建师大附中2011-2012学年高二上学期期中考试化学试题(人教版) 人教版 题型:022
现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为________热反应,且m+n________p(填“>”“=”“<”).
(2)减压时,A的质量分数________.(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率________,B的转化率________.
(4)若升高温度,则平衡时B、C的浓度之比![]() 将________.
将________.
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色________;而维持容器内压强不变,充入氖气时,混合物颜色________(填“变深”“变浅”或“不变”).
查看答案和解析>>
科目: 来源:福建省福建师大附中2011-2012学年高二上学期期中考试化学试题(人教版) 人教版 题型:022
按要求对下图中两极进行必要的链接并填空:
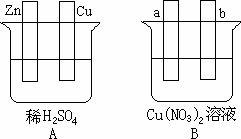
(1)在A图中,使铜片上冒H2气泡.请加以必要连接,则连接后的装置叫________.电极反应式:锌极:________;铜极:________.
(2)在B图中,a、b均为惰性电极,若a极析出铜,则b析出________.加以必要的连接后,该装置叫________.电极反应式,a极:________ b极:________.经过一段时间后,停止反应并搅均溶液,溶液的H+浓度________(升高、降低、不变),加入一定量的________,溶液能恢复至与电解前完全一致.
查看答案和解析>>
科目: 来源:河南省南阳市2010-2011学年高一春期期末考试化学试题(人教版)(人教版) 人教版 题型:022
不同元素的原子在分子内吸引电子的能力大小可用x表示,x越大,其原子吸引电子的能力越强,在所形成的分子中成为带负电荷的一方.下面是某些短周期元素的x值.
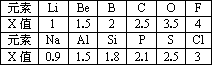
(1)通过分析x值的变化规律,确定Mg、N的x值范围
Mg:________、N:________.
(2)短周期元素x值的变化特点体现了元素性质的________变化规律.
(3)某有机物分子中含有S-N键,你认为电子对偏向________原子(填元素符号).
(4)经验规律告诉我们,当成键的两原子相应元素的x差值Δx大于1.7时一般形成离子键,Δx小于1.7时一般形成共价键,试预测:AlBr3中化学键的类型是________.
设计实验验证你的预测________.
查看答案和解析>>
科目: 来源:河南省南阳市2010-2011学年高一春期期末考试化学试题(人教版)(人教版) 人教版 题型:022
短周期的五种主族元素A、B、C、D、E原子序数依次变小.A的单质在常温下为气态,B、D属于同一主族,C为自然界含量最多的金属元素,D的最外层电子数为次外层的2倍,E为周期表中原子半径最小的元素.
(1)A、B的元素名称分别为________、________.
(2)D、E可以形成多种化合物,其中一种化合物的相对分子质量为28.写出其结构简式________.
(3)自然界中B元素多以氧化物的形式存在,请写出工业上制取B单质的化学方程式________.
(4)写出实验量制取A气体的化学方程式________.
(5)a克C单质和氧化铁的混合物分为两等份,向其中一份中加入足量NaoH溶液,测得生成气体(标况,下同)体积为mL;另一份在高温下恰好完全反应,将产物冷却后加入足量HCl溶液,测得生成气体体积为nL.则m∶n=________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com