
科目: 来源:湖北省公安三中2011-2012学年高二3月考试化学试题 题型:022
现有S2-、SO32-、NH4+、Al3+、、Na+、SO42-、Fe3+、HCO3-、Cl-等离子,请按要求填空:
(1)在水溶液中,该离子水解呈碱性的是________.
(2)在水溶液中,该离子水解呈酸性的是________.
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子有________.
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子有________.
查看答案和解析>>
科目: 来源:湖北省公安三中2011-2012学年高二3月考试化学试题 题型:022
现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中水电离出的H+浓度由大到小的顺序是(填序号)________.
(2)④、⑤、⑦、⑧四种溶液中NH![]() 浓度由大到小的顺序是(填序号)________.
浓度由大到小的顺序是(填序号)________.
(3)将①和⑧等体积混合后,混合液中各离子浓度关系正确的是________.
A.c(H+)>c(SO![]() )>c(NH
)>c(NH![]() )>c(OH-)
)>c(OH-)
B.c(H+)=c(SO![]() )=c(NH
)=c(NH![]() )>c(OH-)
)>c(OH-)
C.c(NH![]() )>c(H+)=c(SO
)>c(H+)=c(SO![]() )>c(OH-)
)>c(OH-)
D.c(OH-)>c(H+)>c(NH![]() )=c(SO
)=c(SO![]() )
)
查看答案和解析>>
科目: 来源:甘肃省天水一中2011-2012学年高二下学期第一学段考试化学试题(兰天班) 题型:022
把由
NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中,有1.16 g白色沉淀析出,向所得的浊液里,逐渐加入0.5 mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
(1)
写出mn段反应的离子方程式________.(2)
混合物中NaOH的物质的量是________,AlCl3的物质的量是________,MgCl2的物质的量是________.(3)P
点所表示的加入盐酸的体积是________mL.查看答案和解析>>
科目: 来源:甘肃省天水一中2011-2012学年高二下学期第一学段考试化学试题(兰天班) 题型:022
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1 mol/L的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:

(1)写出OA段所发生反应的离子方程式________.
(2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况)
(3)原混合物中Na2CO3的质量分数为________.
查看答案和解析>>
科目: 来源:安徽省蚌埠二中2011-2012学年高二下学期期中考试化学试题 题型:022
向等体积pH=a的盐酸和pH=b的醋酸溶液中分别加入100 mL pH=12的NaOH溶液,充分反应后,两溶液均呈中性.则:
(1)a与b的关系为a________b(填“大于”、“小于”或“等于”,下同).
(2)向等体积的该盐酸和醋酸溶液中分别加入足量的锌粉,充分反应后,产生H2的体积关系为V(H2)盐酸________V(H2)醋酸;反应完成所需时间t(HCl)________t(CH3COOH).
(3)若盐酸的体积为10 mL,则盐酸的物质的量浓度为________.
查看答案和解析>>
科目: 来源:安徽省蚌埠二中2011-2012学年高二下学期期中考试化学试题 题型:022
煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数随温度的变化如下表:
CO2(g)+H2(g)的平衡常数随温度的变化如下表:
试回答下列问题
(1)上述反应的正反应是________反应(填“放热”或“吸热”).
(2)某温度下,上述反应达到平衡后,保持容器体积不变升高温度,正反应速率________(填“增大”、“减小”或“不变”),容器内混合气体的压强________(填“增大”、“减小”或“不变”).
(3)830℃时,在恒容反应器中发生上述反应,按下表中的物质的量投入反应混合物,其中向正反应方向进行的有________(选填A、B、C、D).
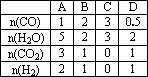
(4)830℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是________.
查看答案和解析>>
科目: 来源:安徽省蚌埠二中2011-2012学年高二下学期期中考试化学试题 题型:022
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的ΔH表示生成1 mol产物的数据).

根据上图回答下列问题:
(1)PCl3分解成P(s)和Cl2(g)的热化学方程式是________.
(2)P和Cl2分两步反应生成1 mol PCl5的ΔH1=________,与P和Cl2一步反应生成1 mol PCl5的ΔH2的关系是:ΔH2________ΔH1(填“大于”、“小于”或“等于”).
查看答案和解析>>
科目: 来源:安徽省蚌埠二中2011-2012学年高二下学期期中考试化学试题 题型:022
(1)某温度下,纯水中c(H+)=5×10-7 mol·L-1,则此时纯水中的c(OH-)=________mol·L-1;若温度不变,滴入稀硫酸使c(H+)=5.0×10-3 mol·L-1,则c(OH-)=________mol·L-1.
(2)已知室温下pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液呈酸性,则高碘酸的电离方程式是________.
查看答案和解析>>
科目: 来源:贵州省瓮安二中2011-2012学年高一下学期第一次月考化学试题 题型:022
已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大.A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳.
(1)请写出B、D元素的名称:B________,D________.
(2)画出C元素的离子结构示意图________.
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式________
(4)A、B、C三种元素形成的化合物为________,所含的化学键类型为________.
(5)B、C、D三种元素的离子半径由大到小的排列顺序为________(用离子符号表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com