
科目: 来源:黑龙江省哈师大附中2011-2012学年高二下学期第一次月考月考化学试题 题型:022
完成下列化学方程式
(1)实验室制乙炔:________
(2)乙醇的催化氧化:________
(3)甲苯的硝化:________
(4)苯酚钠溶液中通入少量二氧化碳:________
查看答案和解析>>
科目: 来源:黑龙江省哈师大附中2011-2012学年高一4月月考化学试题 题型:022
有A、B、甲、乙、丙、丁、戊代表的物质有如下转化关系.
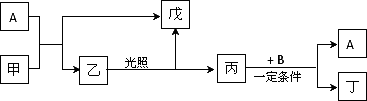
A是三核10电子的分子,B是四核10电子的分子.戊的浓溶液与一种黑色粉末共热可得甲.
请填写下列空格:
(1)戊为________,乙为________,A为________(填化学式).
(2)戊和B形成的化合物中化学键类型为________,其中阳离子的电子式是________.
(3)B和丁在一定条件下反应生成两种无污染的物质,是一种治理污染的好办法,写出该反应的化学方程式,并用双线桥标明电子转移情况:________.
查看答案和解析>>
科目: 来源:黑龙江省哈师大附中2011-2012学年高一4月月考化学试题 题型:022
下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白:

(1)③和⑧的氢化物沸点高的是________(填化学式),原因是________.
(2)第三周期的元素形成的单原子离子半径最大的是________(填化学式).
(3)①和②按质量比3:8形成的化合物A的电子式为________,将过量A通入由②和⑤形成的阴离子的盐溶液的的离子方程式为________.
(4)用电子式表示元素④与⑦的化合物的形成过程:________,该化合物属于________(填“共价”或“离子”)化合物.
查看答案和解析>>
科目: 来源:福建省厦门六中2011-2012学年高二下学期期中考试化学试题 题型:022
(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+.在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________.
A.KMnO4
B.H2O2
C.Cl2水
D.HNO3
然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的________.
A.NaOH
B.NH3·H2O
C.CuO
D.Cu(OH)2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为________,Fe3+完全沉淀时溶液的pH为________,通过计算确定上述方案________(填“可行”或“不可行”).(已知:lg2=0.3;lg5=0.7)
查看答案和解析>>
科目: 来源:福建省厦门六中2011-2012学年高二下学期期中考试化学试题 题型:022
在水溶液中的反应:2I-(aq)+2Fe3+(aq)![]() 2Fe2+(aq)+I2.(aq)反应的平衡常数表达式为KC=________.当上述反应达到平衡后,加入CCl4萃取I2且温度不变,上述平衡向________(填“向左”“向右”或“不变”)移动.
2Fe2+(aq)+I2.(aq)反应的平衡常数表达式为KC=________.当上述反应达到平衡后,加入CCl4萃取I2且温度不变,上述平衡向________(填“向左”“向右”或“不变”)移动.
上述反应的正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)·cn(Fe3+),且已知下列数据(浓度与反应速率的关系,k为常数)
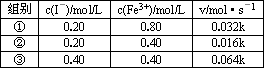
通过所给的数据计算得知;在v=kcm(I-)·cn(Fe3+)中,m、n的值为________
A.m=1;n=1
B.m=1;n=2
C.m=2;n=1
D.m=2;n=2
结论:I-浓度对反应速率的影响________(填“>”、“<”、“=”)Fe3+浓度对反应速率的影响.
查看答案和解析>>
科目: 来源:山东省济宁市泗水一中2011-2012学年高二3月月考化学试题 题型:022
现有S2-、SO32-、NH4+、Al3+、、Na+、SO42-、Fe3+、HCO3-、Cl-等离子,请按要求填空:
(1)在水溶液中,该离子水解呈碱性的是________.
(2)在水溶液中,该离子水解呈酸性的是________.
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子有________.
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子有________.
查看答案和解析>>
科目: 来源:山东省济宁市泗水一中2011-2012学年高二3月月考化学试题 题型:022
某有机化合物A的相对分子质量(分子量)大于110,小于150.经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧.请回答:
(1)该化合物分子中含有几个氧原子,为什么?
(2)该化合物的相对分子质量(分子量)是________.
(3)该化合物的化学式(分子式)是________.
(4)该化合物分子中最多含________个![]() 官能团.
官能团.
查看答案和解析>>
科目: 来源:山东省济宁市泗水一中2011-2012学年高一3月月考化学试题 题型:022
铜和浓硫酸发生反应的化学方程式为:
Cu+2H2SO4(浓)(1)浓H2SO4作________剂,具有________性.
(2)在该反应中,若消耗了32 g Cu,则转移了________mol电子,还原了________mol H2SO4,生成________L SO2(标准状况)气体.
(3)以下三种物质的氧化性由强到弱的顺序为:________(写出序号)
①浓H2SO4
②稀H2SO4
③CuSO4
查看答案和解析>>
科目: 来源:安徽省铜陵市一中2011-2012学年高一下学期期中考试化学试题 题型:022
A、B两种酸式含氧酸盐的相对分子量均为120,且都溶于水;D气体能使品红溶液褪色;F固体为淡黄色;E是不溶于水和盐酸的白色沉淀,它们之间的转化关系如图所示:

(1)写出化学式:F________;G________;D________;H________.
(2)写出反应②的离子方程式:②:________.
(3)写出一个由I生成D的化学方程式:________.
查看答案和解析>>
科目: 来源:安徽省铜陵市一中2011-2012学年高一下学期期中考试化学试题 题型:022
[Ⅰ]将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:
3A(g)+B(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol,则:
(1)用C表示10 s内正反应的化学反应速率为________;
(2)反应前A的物质的量浓度是________;
[Ⅱ]某温度下,在一个体积为2 L的固定不变的密闭容器中充入0.3 mol SO2和0.2 mol O2,发生2SO2+O2![]() 2SO3反应.几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90%,则该反应达到平衡时SO2的转化率为________.
2SO3反应.几分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90%,则该反应达到平衡时SO2的转化率为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com