
科目: 来源:福建省安溪梧桐中学、俊民中学2011-2012学年高二下学期期末联合质检化学试题 题型:022
A、B、C、D是四种短周期元素,它们的原子序数依次增大.其中A、D元素同主族,B、C元素同周期,由A、B、C、D中的两种元素可形成原子个数比为1∶1的多种化合物,甲、乙、丙、丁为其中的四种,它们的元素组成如下表所示:
通常状况下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质和丁物质为固体且都为离子化合物.请填写下列空白:
(1)甲物质的结构式为________,丙物质的电子式为________,丁物质中阴离子与阳离子的个数比为________.
(2)若标准状况下5.6 L甲气体完全燃烧生成稳定氧化物时放出的热量为325 kJ,试写出表示甲物质燃烧热的热化学方程式________.
(3)研究表明乙物质具有弱酸性,则乙物质在水中的电离方程式为________.
查看答案和解析>>
科目: 来源:黑龙江省鹤岗一中2011-2012学年高一下学期期末考试化学试题 题型:022
如下图装置闭合电键时,电流计A的指针将发生偏转.试回答下列问题.

(1)A池是________;Zn的电极名称是________B池是________;Pt的电极名称是________.(填电解池、原电池、阴、阳、正、负极等)
(2)写出下列有关反应:Cu极上电极反应:________,C极上电极反应:________.
(3)B池中的总反应的化学方程式为________
(4)如果要用B池给铁片上镀上一层Cu,则B池应作何改进________.
查看答案和解析>>
科目: 来源:黑龙江省鹤岗一中2011-2012学年高一下学期期末考试化学试题 题型:022
25℃时,有下列四组溶液
①0.1 mol/L醋酸溶液,
②0.1 mol/L的盐酸,
③pH=13的氢氧化钠溶液,
④pH=13的氨水
(1)溶液中的c(H+)大小关系是________(填序号,下同).
(2)其中水的电离程度最大的是________.
(3)取等体积的③和④的溶液分别稀释100倍,稀释后溶液的pH关系为③________④(填“>”、“=”、“<”).
查看答案和解析>>
科目: 来源:黑龙江省鹤岗一中2011-2012学年高一下学期期末考试化学试题 题型:022
现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)m+n________p(填“>”“=”“<”).
(2)若加入B(体积不变),则A的转化率________,B的转化率________.(填“增大”“减小”或“不变”,下同)
(3)若升高温度,则平衡时B、C的浓度之比![]() 将________.
将________.
查看答案和解析>>
科目: 来源:江苏省阜宁县中学2011-2012学年高一下学期期中调研考试化学试题 题型:022
下表是元素周期表的一部分,回答下列有关问题:
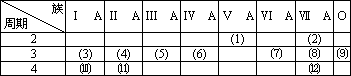
(1)在这些元素中,最活泼的非金属元素是________,最不活泼的元素是________,常作半导体材料元素是________.(以上均填元素符号)
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的酸是________,碱性最强的碱是________,呈两性的氢氧化物是________.(以上均填物质的名称)
(3)在(3)与(4)中,化学性质较活泼的是________(填元素符号),证明该结论的化学实验是________.
(4)在(8)和(12)中,化学性质较活泼的是________(填元素符号),证明该结论的化学实验是________.
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:022
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体.顺铂的结构式为 ,具有抗癌作用;反铂的结构式为
,具有抗癌作用;反铂的结构式为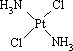 ,无抗癌作用.
,无抗癌作用.
(1)C、N、O三种元素的电负性由大到小的顺序是________;
(2)顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由:________.
(3)金属铂的原子堆积方式为与铜型(面心立方堆积),一个金属铂的晶胞中含有________个铂原子.
(4)NH3还能与很多化合物通过配位键发生相互作用.例如:科学家潜心研究的一种可作储氢材料的化合物X是NH3与第二周期另一种元素的氢化物相互作用的产物,X是乙烷的等电子体;加热化合物X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体.
①化合物X的结构式为________(必须标明配位键).
②化合物X、Y分子中,N元素分别发生了________杂化.
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:022
已知A、B、C均为短周期元素形成的单质,且元素A、B同周期,A元素原子半径大于B元素原子半径,在一定条件下单质A和单质B.单质A和C都按物质的量2∶1反应,分别生成X和Y,在产物中B、C两元素呈负价.
分别取3份完全相同且质量均为1.52 g由单质A和单质B组成的混和物进行下列实验:
①在第一份样品中加入过量盐酸,充分搅拌后在标准状况下放出0.896 L H2残留不溶于酸的固体0.56 g
②在第二份样品中加入过量浓NaOH溶液,微热充分反应后在标准状况下放出0.896 L H2残留不溶于碱的固体0.96 g
③将第三份样品隔绝空气加强热生成化合物X,将X投入稀盐酸中,X溶解且放出在空气中能自燃的气体a L
根据上述题给信息和实验记录解答下列问题
(1)写出下列元素的名称:A:________;B:________;C:________;
(2)混和物中B的质量分数是:________;
(3)写出实验③中有关反应的化学方程式________,a的值为________.
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:022
人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测为钛(22Ti),它被誉为“未来世纪的金属”.试回答下列问题:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基态原子的价电子排布为_________.
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定;
①偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如下图,它的化学式是________;
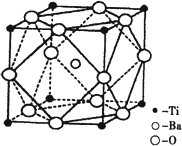
②已知Ti3+可形成配位数为6的配合物.现有含钛的两种颜色的晶体,一种为紫色,另一为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O.为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的![]() .则绿色晶体配合物的化学式为________,绿色晶体中含有化学键类型是________.
.则绿色晶体配合物的化学式为________,绿色晶体中含有化学键类型是________.
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:022
C、Si、Ge、Sn是同族元素,该族元素单质及其化合物在材料、医药等方面有重要应用.请回答下列问题:
(1)Ge的原子核外电子排布式为________.
(2)CO可以和很多金属形成配合物,如Ni(CO)4,Ni与CO之间的键型为________.
(3)Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)5晶体属于________.(填晶体类型)
(4)碳氧键的红外伸缩振动频率与键的强度成正比,已知Ni(CO)4中碳氧键的伸缩振动频率为2060 cm-1,CO分子中碳氧键的伸缩振动频率为2143 cm-1,则Ni(CO)4中碳氧键的强度比CO分子中碳氧键的强度________.(填字母)
A.强
B.弱
C.相等
D.无法判断
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:022
下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
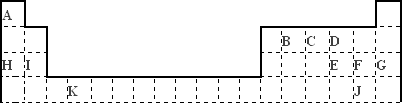
(1)表中用字母标出的元素中,属于过渡元素的是________(该空用字母表示),在周期表中铁的位置:________.
(2)D、F、B气态氢化物中以________最不稳定(填化学式).B的气态氢化物中B元素采取________方式杂化,其空间构型为________.
(3)王水可溶解不能与硝酸反应的金属如Au、Pt等,其原因是王水中不仅含有HNO3、还有反应生成的Cl2和NOCl,假设NOCl中所有原子都达到了8电子稳定结构,试写出NOCl的电子式________.
(4)EBC-和A2D2反应生成了ED42-和可参加大气循环的两种无毒无害气体,试写出该反应的离子方程式________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com