
科目: 来源:高一化学(通用各科奥林匹克ABC卷及解析) 题型:022
120℃、101.3 kPa条件下,有2L ![]() 、2L CO、1L
、2L CO、1L ![]() 、0.5L
、0.5L ![]() 和1L
和1L ![]() 组成的混合气体.将混合气体通过分别放有足量Cu粉、C粉和CuO粉的三个灼热的反应管.假设气体通过每个反应管都能充分反应,且不论三个反应管以何种顺序排列,问:
组成的混合气体.将混合气体通过分别放有足量Cu粉、C粉和CuO粉的三个灼热的反应管.假设气体通过每个反应管都能充分反应,且不论三个反应管以何种顺序排列,问:
(1)尾气是否有可能是单一气体?________(填“可能”或“不可能”).若可能,该气体是________.
(2)原气体中是否有几种(或一种)不可能再存在于尾气之中?________(填“有”或“没有”).若有,它们(或它)是________.
(3)原气体中是否有几种(或一种)肯定存在于尾气中(填“有”或“没有”).若有,它们(或它)是________.
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(1)-化学 题型:022
已知:五种短周期元素A、B、C、D、E的原子序数依次增大.其中,元素B原子的最外层电子数是次外层电子数的2倍,元素A与D、C与E分别同主族;A、B、D、E的单质都能在C的单质中燃烧,分别生成化合物X、Y、Z、P;化合物X在常温下是一种液体,化合物Y是一种有毒气体,单质E和化合物Z都是淡黄色固体.
请回答列下问题:
(1)在周期表中,元素B位于________周期________族;
E元素原子形成的简单离子的结构示意图________;
(2)将A、B、C、D、E五种元素的原子半径按由小到大顺序排列(用元素符号表示)________;
(3)物质P可以使溴水褪色,写出该反应的离子方程式________;
(4)化合物X、Y、Z、P中的某两种能发生反应,生成A、B、C、D、E中的一种单质.试写出符合上述条件的两个化学方程式:
①________;
②________.
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(1)-化学 题型:022
A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化.

试回答下列问题:
(1)A是________B是________D是________E是________.
(2)检验F中金属阳离子的常用方法是________.
(3)写出F与B发生反应的离子方程式________.
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(1)-化学 题型:022
针对下面10种元素,完成以下各小题.
(1)地壳中含量最多的元素是________(填名称).
(2)化学性质最不活泼的元素是________(填元素符号).
(3)Mg的原子结构示意图为________.
(4)C与N相比,原子半径较小的是________.
(5)最高价氧化物对应的水化物碱性最强的是________(填化学式).
(6)MgO和Al2O3中,属于两性氧化物的是________.
(7)S和Cl相比,元素非金属性较强的是________.
(8)可用来制造光导纤维的物质是????,晶体硅的主要用途是???(写出一种).
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(1)-化学 题型:022
完成下反应的化学方程式或离子方程式
(1)铝与四氧化三铁在高温下反应(铝热反应)________;
(2)工业上用焦炭和二氧化硅反应制得粗硅(Si)________.
(3)炒菜时,经常加入少量的料酒(含乙醇)和醋,可使菜变得香醇可口,请用化学方程式表示该反应的原理:________.
(4)医学上,用(胃舒平)氢氧化铝治疗胃酸过多,写出反应的离子方程式________
(5):氯化铝溶液中加入过量氨水的离子方程式________.
(6):醋酸溶液和碳酸钠溶液混合的离子方程式________.
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(2)-化学 题型:022
通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品.试根据下图回答有关问题:
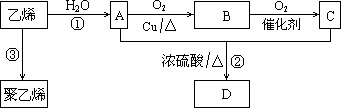
(1)有机物A是________,B是________C是________(填名称).
(2)写出图示反应①③的化学方程式,并指明反应类型:①;反应类型:________.②;反应类型:________.
查看答案和解析>>
科目: 来源:福建省厦门市2012-2013学年高一下学期期末考试模拟试题(2)-化学 题型:022
元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素.请依据这9种元素回答下列问题.
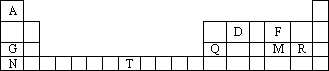
(1)表中R的元素符号为________,金属性最强的元素是________(填元素符号).
(2)元素的非金属性:M________R(填“>”或“<”).
(3)R的最高价氧化物对应水化物的化学式是________.
(4)F、G两元素形成的淡黄色固体物质含有的化学键的类型是________.
(5)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是________(填离子符号).
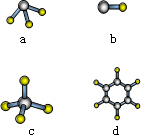
(6)A与D形成分子的空间结构可能是(填序号)________.
查看答案和解析>>
科目: 来源:四川省攀枝花市2012-2013学年高一下学期期末调研监测化学试题 题型:022
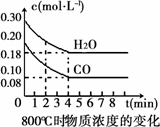
在一体积为10 L的容器中,通入一定量的CO和H2O,在800℃时发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0.
CO2(g)+H2(g) ΔH<0.
(1)在800℃时,CO和H2O浓度变化如下图,0~4 min的平均反应速率v(CO)=________mol/(L·min).该反应的平衡常数是________.
(2)在相同容器中发生上述反应,当温度高于800℃时,容器内各物质的浓度变化如下表.

①表中3 min~4 min之间反应处于________状态;c1数值________0.08 mol/L(填大于、小于或等于).
②反应在4 min~5 min间,平衡向逆方向移动,可能的原因是________.
a.增加水蒸气
b.降低温度
c.使用催化剂
d.增加氢气浓度
(3)在相同温度下(800℃),若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,请你对此时该反应是否达到平衡状态作出判断并写出你的判断依据________.
查看答案和解析>>
科目: 来源:四川省攀枝花市2012-2013学年高一下学期期末调研监测化学试题 题型:022
下列化合物:
①HCl
②NaOH
③CH3COOH
④NH3·H2O
⑤CH3COONa
⑥NH4Cl
(1)属于弱电解质的是________(填序号),溶液呈酸性的有________(填序号).
(2)25℃时,0.10 mol/LCH3COONa溶液pH=11,该溶液中离子浓度按由大到小的顺序为________.
(3)将等pH等体积的HCl和CH3COOH分别稀释m倍和n倍,若稀释后两溶液的PH仍相等,则m________n(填“大于、等于、小于”).
(4)25℃时,在20 mL0.1 mol/L醋酸溶液加入VmL0.1 mol/LNaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是________.
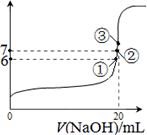
A.pH=3的醋酸溶液和pH=11的醋酸钠溶液中,水的电离程度相同
B.①点时pH=6,此时溶液中,c(CH3COO-)-c(Na+)=9.9×10-7 mol/L
C.②点时,溶液中的c(CH3COO-)=c(Na+)
D.③点时V=20 mL,此时溶液中c(CH3COO-)>c(Na+)
查看答案和解析>>
科目: 来源:四川省攀枝花市2012-2013学年高一下学期期末调研监测化学试题 题型:022
写出下列反应的化学方程式
(1)在加热条件下,木炭与浓硫酸反应________.
(2)在加热条件下,铜与浓硫酸反应________.
(3)在催化剂存在下,氨与氧气反应生成NO和水________.
(4)在AgCl的悬浊液中加Na2S溶液,生成黑色Ag2S沉淀________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com