
科目: 来源: 题型:022
过氧化氢(H2O2)俗名双氧水,医疗上可作外科消毒剂。
(1)H2O2的电子式为________,固态时H2O2为________晶体。
(2)将双氧水加入酸性KMnO4溶液中,溶液的紫红色消褪了,此时双氧水表现出________性。若用H218O2的双氧水与KMnO4酸性溶液反应,18O将存在于生成物________里。
(3)向含有酚酞的Na2CO3溶液中滴入双氧水,溶液由红色褪至无色。再向该溶液中加入足量的0.1mol·L-1NaOH溶液,始终不再显红色。这是因为双氧水具有________性。
查看答案和解析>>
科目: 来源: 题型:022
唐代孤刚子的炼胆石提精华法,实际上是在炼丹炉里干馏胆矾,除得到硫酸外,还有黑色粉末生成。写出有关的化学方程式:
(1)________________。 (2)________________。 (3)________________。
查看答案和解析>>
科目: 来源: 题型:022
在铁粉和过量热硝酸反应的溶液中,加入过量的Cu粉,反应后溶液中滴加氢氧化钠溶液,立即产生沉淀,①此沉淀物为( ),②放置一段时间后,沉淀物是( )
A.Fe(OH)2 B.Fe(OH)3
C.Fe(OH)3、Cu(OH)2 D.Fe(OH)2、Cu(OH)2
查看答案和解析>>
科目: 来源: 题型:022
常温下有一混合气体,可能是由H2,O2,N2,Ar,Cl2,NO,HCl,NH3,CO2等气体中的两种或多种组成,取此混合气体160mL进行实验
(1) 混合气通过浓H2SO4,体积减小15mL;
(2) 剩余气体通过足量Na2O2固体,充分反应后,体积又减小30mL;
(3) 剩余气体点燃后冷至室温,体积又减小75mL;
(4) 剩余气体通过灼热的铜丝网后,冷至室温体积又减小10mL;
最后剩余气体30mL整个操作过程中无任何颜色变化,试推断混合气中
①肯定有的气体是:___________________,各占________________mL;
②肯定没有的气体是:__________________;
③可能存在的气体是:__________________,占_____________mL 。
查看答案和解析>>
科目: 来源: 题型:022
某短周期元素的气态氢化物在高温下分解生成固态物质和氢气。在相同情况下,气体体积是原来的1.5倍,分解前后气体密度比为17∶1。该元素原子核内质子数比中子数少1个。
(1)该元素的原子量为_________,元素符号为____________
(2)该元素的电子式为_________,气态氢化物的电子式为____________。
(3)该元素的气态氢化物的稳定性比NH3的稳定性_________,键能比N–H的键能__________
(4)该元素最高氧化物的水化物的酸性比H2SO4的酸性__________。
查看答案和解析>>
科目: 来源: 题型:022
A元素的最高价离子0.5mol被还原成中性原子时得到6.02×1023个电子。当它与盐酸充分反应时放出0.02g氢气,消耗A单质0.4g。B元素的原子核外电子层数与A相同,且B元素的单质常温下为深棕红色液体。
(1)画出A、B元素常见离子的结构示意图________________,________________。
(2)用电子式表示A、B形成化合物的过程__________,化学键为__________。
查看答案和解析>>
科目: 来源: 题型:022
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
依据工艺流程图,完成下列填空。
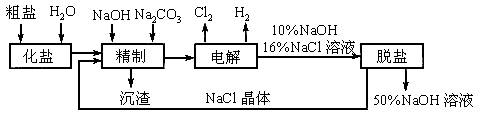
(1)在电解过程中,与电源正极相连的电极上发生反应的电极方程式为_______________,
与电源负极相连的电极附近,溶液pH________;(填“不变”、“升高”或“下降”)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________________,
________________;
(3)如果粗盐中![]() 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去![]() ,该钡试剂可以是________;(填序号)
,该钡试剂可以是________;(填序号)
a.Ba(OH)2 b.Ba(NO)2 c.BaCl2
(4)为了有效去除Ca2+、Mg2+、![]() ,加入试剂的合理顺序为________;(填序号)
,加入试剂的合理顺序为________;(填序号)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl;
(6)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应。采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________________________________。
查看答案和解析>>
科目: 来源: 题型:022
以苯、硫酸、氢氧化钠、亚硫酸钠为原料,经典的合成苯酚的方法可简单表示为

(1)写出第②、③、④步反应的化学方程式:
②________________________________________________________________;
③________________________________________________________________;
④________________________________________________________________。
(2)根据上述反应判断苯磺酸、苯酚、亚硫酸等三种物质的酸性强弱。
查看答案和解析>>
科目: 来源: 题型:022
拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。
|
气体 |
A |
B |
c |
d |
|
C2H4 |
乙醇 |
浓H2SO4 |
NaOH溶液 |
浓H2SO4 |
|
Cl2 |
浓盐酸 |
MnO2 |
NaOH溶液 |
浓H2SO4 |
|
NH3 |
饱和NH4Cl溶液 |
消石灰 |
H2O |
固体NaOH |
|
NO |
稀HNO3 |
铜屑 |
H2O |
P2O5 |
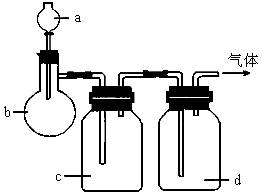
(1)上述方法中可以得到干燥、纯净气体的是________;
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体________,理由是________________________________________________;
②气体________,理由是________________________________________________;
③气体________,理由是________________________________________________;
④气体________,理由是________________________________________________。
查看答案和解析>>
科目: 来源: 题型:022
在密闭容器中充入一定量的SO3气体,在500℃、1.01´105Pa下分解:
2SO3(g)ƒ2SO2(g)+O2(g);测得平衡混合气对氢气的相对密度为38.8,则SO3的分解率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com