
科目: 来源: 题型:022
在0.2mol/L氨水中存在下列平衡:H2O+NH3![]() NH3·H2O
NH3·H2O![]()
![]() +OH-,当改 变条件填写表中各项内容。
+OH-,当改 变条件填写表中各项内容。
|
改变条件 |
平衡移动方向 |
PH |
C( |
|
(1)通入NH3至饱和 |
|
|
|
|
(1)加少量盐酸 |
|
|
|
|
(3)加少量NaOH |
|
|
|
|
(4)加水稀释 |
|
|
|
|
(5)加少量NH4Cl固体 |
|
|
|
|
(6)加少量AlCl3固体 |
|
|
|
查看答案和解析>>
科目: 来源: 题型:022
对可逆反应aA(g)+bB(g)![]() cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
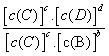 =K(为一常数),K称为化学平衡常数,其反应的K值只与温度有 关。现有反应:
=K(为一常数),K称为化学平衡常数,其反应的K值只与温度有 关。现有反应:
CO(g)+H2O(g)=CO2(g)+H2(g)△H<0,在850℃时,K=1。
(1)若升高温度到950℃时,达到平衡时K________1(填“大于”“小于”或“等于”)。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO,3.0molH2O1.0molCO2 和xmolH2,则 ①当x=5.0时,上述平衡向________。(填“正反应”或“逆反应”)方向移动。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是________。
查看答案和解析>>
科目: 来源: 题型:022
等量的Na、Mg、Al与含等物质的量的HCl的盐酸作用产生H2,产生H2的体积会出现下列四种情况:
①V(Na)>V(Mg)=V(Al) ②V(Na)=V(Al)=V(Mg) ③V(Mg)=V(Al)>V(Na) ④V(A1)>V(Mg)>V(Na)
若盐酸中含HCl为1mol,将满足上述四种情况所需x、y的量填入下表:
等量的Na、Ng、Al ① ② ③ ④
物质的量x(mol)
质量y(g)
查看答案和解析>>
科目: 来源: 题型:022
为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。
乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊,推测在制得的乙炔中还可能含有少量还原性的杂质气体,由此他提出必须先除去之,再与溴水反应。请你回答下列问题:
(1)写出甲同学实验中两个主要的化学方程式________________,________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙炔与溴发生加成反应,其理由是________(多选扣分)。
A. 使溴水褪色的反应,未必是加成反应
B. 使溴水褪色的反应,就是加成反应
C. 使溴水褪色的物质,未必是乙炔
D. 使溴水褪色的物质,就是乙炔
(3)乙同学推测此乙炔中必定含有的一种杂质气体是________,它与溴水反应的化学方程式是________,在验证过程中必须全部除去。
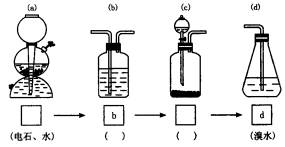
(4)请你选用下列四个装置(可重复使用)来实现乙同学的实验方案(见图),将它们的编号填人方框,并写出装置内所放的化学药品。
(5)为验证这一反应是加成而不是取代,丙同学提出用pH试纸来测试反应后溶液的酸性,理由是_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:022
(1)今有反应2H![]() +O
+O![]()
![]() 2H
2H![]() O构成了燃料电池,则负极通的应是________,
O构成了燃料电池,则负极通的应是________,
正极通的应是________。电极反应式为:负极________,正极________。
(2)如把KOH改为稀H2SO4作电解质,则电极反应式为:负极________,正极 ________。两电极附近溶液的PH各有何变化?(3)如把H2改为CH4、KOH作导电物质,则电极反应式为:负极________,正极 ________。
查看答案和解析>>
科目: 来源: 题型:022
Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气为阴极燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
阳极反应式:2CO+2CO32-→4CO2+4e—阴极反应式:________。
总电池反应式:________。
查看答案和解析>>
科目: 来源: 题型:022
在a、b两支试管中,分别装上形态相同、质量相等的一颗锌粒,然后向两支 试管中分别加入相同物质的量、相同体积的稀盐酸和稀醋酸。填写下列空白:
(1)a、b两支试管中的现象:相同点是________;不同点是________。原因是(2)a、b两支试管中生成气体的体积开始时是a________b,反应完毕后生成气体的总 体积是a________b(填“大于”“小于”或“等于”),原因是________。
查看答案和解析>>
科目: 来源: 题型:022
已知多元弱酸在水溶液中的电离是分步进行的,且第一步电离程度大于第二步 电离程度,第二步电离程度远大于第三步电离程度今有HA、H2B、H3C三种一元、 二元、三元弱酸,根据“较强酸+较弱酸盐=较强酸盐+较弱酸”的反应规律,它们 之间能发生下列反应:
①HA+HC2-(少量)=A—+H2C- ②H2B(少量)+2A-=B2-+2HA ③H2B(少量)+H2C-=HB-+H3C 回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是________(2)A-、B2—、C3—、HB-、H2C—、HC2-六种离子中,最易结合质子的是________,
最难结合质子的是________。
(3)判断下列反应的离子方程式中正确的是(填写标号)________。
( )
A. H3C+3A-![]() 3HA+C3-
3HA+C3-
B. HB-+A-![]() HA+B2-
HA+B2-
C. H3C+B2-![]() HB-+H2C-
HB-+H2C-
(4)完成下列反应的离子方程式。
( )
A. H3C++OH-(过量)![]() ________;
________;
B. HA(过量)+C3—![]() ________。
________。
查看答案和解析>>
科目: 来源: 题型:022
(2004年湖北八校联考)某化学课外活动小组,设计了如右图所示的装置,进行实验:
![]()
(一)若用该装置来制取NO2气体,实验步骤如下:
(1)气密性检查,请回答该装置气密性检查的最简单的方法:________________(2)加入固体试剂Cu片,打开阀门K,拔出注射器活塞,加入一小片Cu片将注射器 活塞装上并压至底部,排出里面的空气。
(3)吸取浓HNO3,将注射器尖嘴导管插入浓HNO3,中,并向上拉注射器活塞吸取少 量的浓HNO3,然后迅速关闭阀门K,请回答此时可能观察到的实验现象:________,
当生成的NO2气体体积接近最大刻度时,迅速打开阀门K,将反应液放入NaOH溶液中后关闭K。
(二)验证NO2性质实验。
(1)观察收集到的气体呈________色,若向下用力压活塞,发现气体的颜色先变深,后变浅,原因是________________。
(2)进行实验(1)后,为验证NOs气体与H2O的反应,将注射器尖嘴导管插入水中,打开活塞K,然后吸取少量的水,关闭阀门K,振荡后发现气体变为无色,且气体的 体积缩小,请写出发生反应的离于方程式。
(3)为了验证进行实验(2)后注射器中的气体,请设计一实验方案加以验证:____________(三)用该装置还可制取中学化学中哪些常见的有毒、有污染的气体?
查看答案和解析>>
科目: 来源: 题型:022
(重组提高)已知0.1mo1·L-1的KHCO3溶液的pH约为8,同浓度的NaAlO2溶液的pH约为11,将两种溶液等体积混合,结果产生沉淀。请用一个离子方程式表示该反应。所以水解产物除了Al(OH)3,还有CO32-。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com