
科目: 来源:物理教研室 题型:022

(1)写出A、B两种盐的化学式:A________;B_______。
(2)写出A、B等物质的量反应的离子方程式:______ __。
(3)写出E、F混合通入水中反应的化学方程式:___ ____。
(4)电解C的无色溶液,阴、阳两极所得气体的体积比理论值为1∶1,而实际收集到的气体的体积比却大于1∶1,原因是_____ ___。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
请参照物质的溶解度表回答下列问题:
(1)写出制取过程中反应的化学方程式。
(2)若提供100 g水,则需NaOH的物质的量为多少?
(3)简述实验的操作过程。
(4)在右图中反映上述实验过程的图象中,标出A点(即当![]() =
=![]() ,且n(
,且n(![]() )=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。
)=0.125 mol时)的位置,并判断此时所得盐的组成及其物质的量。

查看答案和解析>>
科目: 来源:物理教研室 题型:022

图中:1.空气;2.某溶液;3.纯碱;4.稀H2SO4;6.碱石灰
实验步骤是:
A.按下图所示仪器,组装好实验装置,并检查其气密性;
B.准确称量盛有碱石灰的干燥管D的质量(设为m1 g);
C.准确称量一定量的纯碱(设为n g),并将其放进广口瓶内;
D.从分液漏斗中缓缓滴人一定量的稀硫酸,并从“1”处缓缓鼓入空气,至B反应器中不再产生气体时为止;
E.准确称量干燥管D的总质量(设为m2 g)。
根据上述实验,回答下列问题:
(1)该实验进行至操作d时,要缓缓鼓人空气,鼓入空气的作用是________。装置A中盛装的液体“2”应选用________。装置A的作用是________。如果撤去装置A,直接向装置B中缓缓鼓人空气,则会导致实验测定结果________(填“偏大”、“偏小”或“不变”)。
(2)在空白格内画出装置C及试剂。装置C盛放的试剂“5”是________。装置C的作用是________;如果撤去装置C,则会导致实验测定结果________(填“偏大”、“偏小”或“不变”。)
(3)根据此实验,计算纯碱中Na2CO3的质量分数的数学式为________。(用m1,m2,n表示)
(4)装置E的作用是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)有关Na2O2起反应的化学方程式是______________________________________。
(2)CH4、O2、Na2O2的物质的量之比是______________________________________。
(3)取0.1 mol CH4,向残余固体加足量的酸,能放出________mol气体。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(2)市售“家用消毒液发生器”是以精盐和自来水为原料,通过电解时电极板上的大量气泡与电解液接触,所制得的混合液具有强烈的杀菌消毒能力,且不致对人体产生伤害。该发生器配制消毒液所涉及的化学反应(条件略)有:___________________________________;_____________________________________。
(3)电解饱和食盐水时,若去掉隔膜,同时升高温度,此时电解产物间将发生如下反应:6NaOH+3C12 = NaClO3+5NaCl+3H2O,假设该反应进行完全,则在该条件下电解最后得到的产物的物质的量之比是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
打开活塞(1)(3)时,D中蜡烛火焰熄灭;当打开活塞(1)(2)时,D中蜡烛火焰明亮,关闭活塞(1)时,A中反应可自行停止。试根据上述实验事实。回答以下问题:
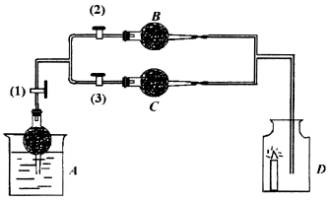
(1)A中发生的化学反应方程式:_____________________________________________
(2)在装置B中的淡黄色粉末是________,发生的化学反应方程式是________________。
(3)在干燥管C中的白色固体应为________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)刚用小刀切开的金属钠断面呈什么颜色?在空气中放置几分钟又有什么变化?
(2)切下来的金属钠块要用滤纸擦净后方可放入水中实验,这是为什么?
(3)金属钠块必须用镊子夹取,为什么不能用手指拿取?
(4)金属钠块投入水中后,为什么很快会熔成银白色小球并浮于水面上?
(5)钠小球为什么会在水面上往返游动?
(6)如果水中在未加钠之前已滴入酚酞试液,反应后颜色会有什么变化?为什么
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com