
科目: 来源:物理教研室 题型:022
(1)宇宙飞船上的氢氧燃料电池,其电极反应为:2H2 + 4OH――4e- = 4H2O,O2 + 2H2O + 4e- = 4OH-,正极发生的是________反应(填氧化或还原),总反应方程式是:____________________________.
(2)燃料电池在发电的同时还合成了水,这正好解决了宇航员在太空中饮水的问题.若电池输出的电流强度为533 A,则每小时能合成多少克水?
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)在电解过程中,与电源正极相连的电极上所发生的电极反应式为________.
(2)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO![]() 等杂质离子,使用的试剂有:a.Na2CO3溶液;b.Ba(OH)2溶液;c.稀盐酸.其合理的加入顺序为___________________.(填试剂序号)
等杂质离子,使用的试剂有:a.Na2CO3溶液;b.Ba(OH)2溶液;c.稀盐酸.其合理的加入顺序为___________________.(填试剂序号)
(3)如果在容积为10 L的离子交换膜电解槽中,1min在阴极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变)______________.
(4)Cl2常用于自来水的消毒杀菌,现在有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需Cl2和ClO2的物质的量之比为__________________.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
650℃下工作的燃料电池.试回答:
(1)负极反应式;
(2)正极反应式;
(3)总电池反应.
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)常温下有颜色的气体单质是________。
(2)除稀有气体外,原子半径最大的元素是________;原子半径最小的元素是________。
(3)气态氢化物中最稳定的是________,含氢的质量分数最大的是________,其氢化物水溶液呈碱性的元素是________。
(4)在最高价氧化物中呈最高正价的元素是________。
(5)地壳中含量最多的元素是________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)把X的单质放入水中,有何现象?写出反应的化学方程式。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是:________和________;________和________。
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。
在短周期元素组成的物质中,与![]() 为等电子体的分子有:________、________。
为等电子体的分子有:________、________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
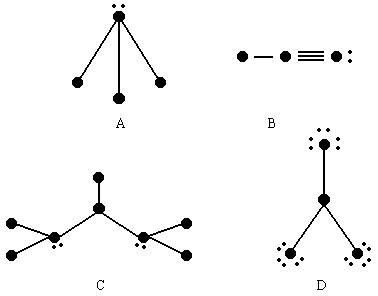
根据各图表示的结构特点,写出该分子的化学式:
A:________B:________C:________D:________
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用→表示,例如,硫酸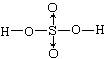 ,硝基甲烷
,硝基甲烷 ,写出三硝酸甘油酯的结构式:________________。
,写出三硝酸甘油酯的结构式:________________。
(已知三硝酸甘油酯的结构简式是 ,要求表示出原子间成键情况)
,要求表示出原子间成键情况)
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)写出各元素符号:X________、Y________、Z________。
(2)X离子的结构简图为________。X与Y形成的离子化合物的电子式为________,Z和氢形成的化合物的电子式为________________。
(3)Y单质在空气中燃烧的化学方程式为____________________________________,生成物与水反应的化学方程式为_________________________________________________。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
(1)114X元素位于元素周期表第________周期________族,为________(填“金属”、“非金属”)元素。
(2)其最高价氧化物及其对应水化物的分子式分别是________、________(用含X的式子表示),并估计后者为________性(填“酸”、“碱”或“两性”)。
(3)它与氯生成化合物的分子式:________、________(用含X的式子表示)。
查看答案和解析>>
科目: 来源:物理教研室 题型:022
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com