
科目: 来源: 题型:022
二氧化硫可使一种叫品红的试剂(红色)褪色,也可以使澄清的石灰水变浑浊。某同学为验证木炭和浓硫酸在加热条件下反应生成的产物,设计了如图所示的实验装置。

根据实验现象回答下列问题:
(1)B中的品红溶液褪色,证明有_______生成;
(2)C中的品红溶液不褪色,D中的石灰水变浑浊,证明有_______生成;
(3)A中现象证明产物中还有另一种物质是水,写出木炭和浓硫酸反应的化学方程式_______;
(4)若B、C中品红溶液均褪色,且D中的石灰水变浑浊,分析对实验结论的影响_______。
查看答案和解析>>
科目: 来源: 题型:022
实验设计:自然界矿物中一种重晶石矿的主要成分是BaSO4,它不溶于任何酸、碱和水,纯净的BaSO4可供医疗等方面应用。某课外活动小组同学用重晶石矿和焦炭为原料制取纯净BaSO4的(设矿物中杂质不与焦炭反应,也不溶于水)部分流程如下:
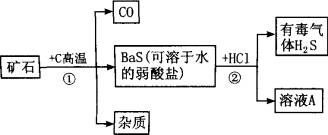
按要求填空:
(1)在步骤①中,________元素的化合价升高了,________元素的化合价降低了。
(2)写出步骤②中溶液A的溶质的化学式________。
(3)写出利用A溶液制取Ba(OH)2的化学方程式________。
(4)有同学指出,上述步骤②产生有毒气体 H2S,应将方法加以改进,请你提出改进意见,使该实验既不产生H2S,又能获得纯净BaSO4。请写出有关化学方程式。
查看答案和解析>>
科目: 来源: 题型:022
某铝合金中含有镁、铜、硅,为了测定该合金中铝的含量,设计如下实验,请回答有关问题:
(1)称取样品ag,应该使用的主要仪器名称是________。
(2)将样品溶解于足量的稀盐酸,过滤,滤液中主要含有________,滤渣中含有________,溶解、过滤用到的玻璃仪器是________。
(3)滤液中加过量氢氧化钠溶液,过滤。有关的离子方程式是________。
(4)步骤(3)的滤液中通入足量二氧化碳气体,过滤。有关的离子方程式是________。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称重,质量为bg。有关的化学方程式是________,原样品中铝的质量分数是________。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏________(高、低、不影响,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏________;若滤渣灼烧不充分,则实验结果偏________。
查看答案和解析>>
科目: 来源: 题型:022
有20.6gNH4HCO3和NaHSO3的干燥粉状混合物,用加热分解的实验方法来测定NH4HCO3的质量分数。根据如图所示的仪器和所盛试剂填空:
(1)按照气流由左→右的方向连接仪器的顺序用a~h表示为________;
(2)仪器B的名称为________,E装置中放碱石灰仪器的名称为________,A和E装置中都用到的仪器名称为________;
(3)D的作用是________;
(4)C的作用是________;若C瓶中溶液颜色有变化,则测定结果可能将会偏________;
(5)B的作用是________;
(6)若碱石灰增重8.8g,则混合物中NH4HCO3的质量分数为________。

查看答案和解析>>
科目: 来源: 题型:022
长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:
①称量ag样品,置于烧杯中。
②加入适量蒸馏水,使样品溶解。
③加入稀盐酸,使溶液呈强酸性,再加过量的BaCl2溶液。
④过滤,用蒸馏水洗涤沉淀。
⑤加热干燥沉淀物。
⑥将沉淀物冷却至室温后,称量。
⑦重复⑤⑥操作直到合格,最后得到bg固体。
回答下面问题:
(1)本实验中是否能用Ba(NO3)2代替BaCl2________。其理由是________。
(2)步骤③中加盐酸使溶液呈强酸性的目的是________。
(3)步骤⑦的“合格”标准是________。
(4)实验测得样品中无水亚硫酸钠的质量分数是:________(列出算式,不需化简)。
查看答案和解析>>
科目: 来源: 题型:022
某石灰石块状样品中含有不溶于酸的杂质,拟用图所示装置测定其中CaCO3的质量分数。

回答下列问题:
(1)写出检验A装置气密性的一种简单操作方法________。
(2)将样品加入试管A的正确操作方法是________。
(3)用托盘天平称取样品Wg,若所用天平游码标尺最大量程为5g,则与此天平配套的砝码中最小的砝码质量是(选填编号字母)________。
A.1g B.2g C.5g D.10g
(4)在读取量筒内液面读数时应注意(选填编号字母)________。
A.视线与凹液面最低处相平
B.视线与凹液面弧线相切
C.读数时应使试剂瓶内液面与量筒内液面相平
D.读数时不一定使试剂瓶内液面与量筒内液面相平
查看答案和解析>>
科目: 来源: 题型:022
某学生用邻苯二甲酸氢钾(
相对分子质量为204.0)测定NaOH溶液的浓度,若NaOH溶液的浓度在0.1mol•L-1左右,滴定终点时溶液的pH约为9.1。该生用托盘天平称量邻苯二甲酸氢钾时,在左盘放有一个1g砝码,游码位置如图所示:

(1)将称好的邻苯二甲酸氢钾放于锥形瓶中,加适量水溶解,溶液无色,再加入指示剂________(从甲基橙、酚酞、石蕊中选择)1~2滴,用NaOH溶液滴定至终点,现象是________。
(2)该生进行三次实验,所取固体质量均相同,填写下表:
实验编号 邻苯二甲酸氢钾质
量/g 待测NaOH溶液体
积/mL
1 18.20
2 17.10
3 16.90
(3)滴定中误差较大的是第________次实验,造成这种误差的可能原因是(只填三种即可):a________b________c________
(4)NaOH溶液的物质的量浓度为(只列出计算式,不必求出结果)。
查看答案和解析>>
科目: 来源: 题型:022
现有甲、乙、丙、丁、戊、己、庚、辛8种无机气体分别置于8个容器中,根据下列实验事实判断各是什么气体,并写出有关的化学方程式,若是离子反应只写离子方程式。
(1)甲、乙、辛三种无色气体难溶于水,其他气体溶于水,特别是戊和己易溶于水;
(2)若把各种气体通入硫酸铜溶液中,丙立即生成黑色沉淀;
(3)若把各种气体通入酸化的硝酸银溶液,丙、丁、戊立即生成沉淀;
(4)甲、乙在一定条件下反应生成己;
(5)甲、丁混合,在光照下发生爆炸,生成戊;
(6)丙充分燃烧可发出淡蓝色火焰,生成庚;
(7)辛在空气中立即生成棕红色气体;
(8)己与空气混合,在催化剂作用下并加热生成辛。试写出8种气体的化学式。
查看答案和解析>>
科目: 来源: 题型:022
有一无色透明溶液,欲确定是否含有下列离子: Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO32-、Cl-、 I-、HCO3-,取该溶液实验如下:
实验步骤 实验现象
①取少量该溶液,加几滴甲基橙 溶液变红色
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热
有无色气体产生,后在空气中又变成红色
③取少量该溶液,加
BaCl2溶液 有白色沉淀生成
④取③中上层清液,加AgNO3溶液 有白色沉淀生成,且不溶于HNO3
⑤取少量该溶液,加
NaOH溶液 有白色沉淀生成,当
NaOH过量时沉淀部分溶解。
(1)溶液中肯定存在的离子是________。
(2)溶液中肯定不存在的离子是________。
(3)为进一步确定其他离子,应该补充的实验是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com