
科目: 来源:江西省定南中学2010届高三年级八月考试化学试题 题型:022
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)
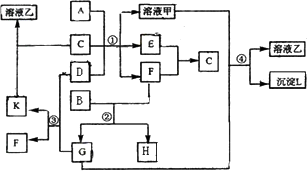
(1)A、B、D代表的物质分别为________、________、________(填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是________;
(3)反应②中,若B与F物质的量之比为4∶3,G、H分别是________、________(填化学式);
(4)反应③产物中K的化学式为________;
(5)反应④的离子方程式为________.
查看答案和解析>>
科目: 来源:湖北黄石二中2010届高三年级八月考试化学试题 题型:022
某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应物或生成物已略去):

已知:①图中每个小三角形的三种物质中至少含有一种相同元素,K与L含有完全相同的元素.②D、J为固体单质,R为气体单质,其余物质为常见化合物.③A能使品红溶液褪色,也能使澄清石灰水变浑浊.④E为淡黄色化合物,E与C或L反应都能生成R.⑤I为氧化物,I与F或C都能反应;G和L反应生成难溶物H,H具有较强的吸附性.根据以上信息,回答下列问题:
(1)写出下列反应的化学方程式:
①C→A:___________________
②L→R:___________________.
(2)写出下列反应的离子方程式:
①E→F:________
②I→G:___________________.
(3)常温下,测得一定浓度G溶液的pH=10,试用离子方程式表示其原因:
___________________________.
查看答案和解析>>
科目: 来源:安徽师大附中2009-2010学年高二开学检测化学试卷 题型:022
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现图所示的物质之间的变化:
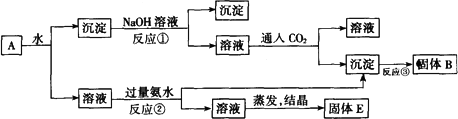
据此判断:
(1)固体B所含物质的化学式为________.
(2)固体E所含物质的化学式为________.
(3)反应①的离子方程式为________.
(4)反应②的离子方程式________.
查看答案和解析>>
科目: 来源:浙江省杭州高中2010届高三上学期第一次月考化学试题 题型:022
以下是某课题组设计的合成聚酯类高分子材料![]() 的路线:
的路线:

已知:①A的相对分子质量小于110,其中碳的质量分数约为0.9;
②同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮:
③C可发生银镜反应.
请根据以上信息回答下列问题:
(1)A的分子式为________;
(2)由A生成B的化学方程式为________,反应类型是________;
(3)由B生成C的化学方程式为________,该反应过程中生成的不稳定中间体的结构简式应是________;
(4)D的结构简式为________,D的同分异构体中含有苯环且水解产物之一为乙酸的有________(写结构简式).
查看答案和解析>>
科目: 来源:腾冲天津中学2010届高三第一次月考化学试卷 题型:022
电解原理在化学工业中有广泛应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为________;在X极附近观察到的现象是________.
②Y电极上的电极反应式为________;检验该电极反应产物的方法是________.
(2)如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是________,电极反应式为________.
②Y电极的材料是________,电极反应式为________.
(说明:杂质发生的电极反应不必写出)
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.
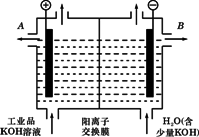
①该电解槽的阳极反应式是________.
②通电开始后,阴极附近溶液pH会增大,请简述原因________.
③除去杂质后的氢氧化钾溶液从溶液出口________(填写“A”或“B”)导出.
查看答案和解析>>
科目: 来源:山东省兖州市2010届高三上学期9月模块检测化学试题 题型:022
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜的反应情况,回答下列问题:
(1)①在100 mL 18 mol/L的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是________
A.40.32 L
B.30.24 L
C.20.16 L
D.6.72 L
②有同学提出,若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,请判断该方案是否可行?若不可行,请说明原因.若可行,请写出反应的离子方程式________.
(2)若将过量铜粉与一定量浓硝酸反应,当反应完全停止时,共收集到的气体1.12 L(标准状况),则该气体的成分是________.则反应中所消耗的硝酸的物质的量可能为________
A.0.1 mol B.0.15 mol C.0.2 mol D.0.25 mol
(3)①甲同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水.则在该反应中,H2O2的作用是________剂,该反应的化学方程式为________.
②乙同学提出,设计一个常见的实验装置,在一定条件下,不需再外加化学试剂,就能将铜溶解在盐酸中.请写出该反应的化学方程式:________,画出相应的装置图并指明电极材料.

查看答案和解析>>
科目: 来源: 题型:022
两种气态物质Am和Bn,已知2.4gAm和2.1gBn所含的原子个数相等,而分子个数之比为2∶3,A、B两种元素的原子核中质子数与中子数相等,A原子的L层电子数是K层电子数的3倍。则:
(1)A、B分别是什么元素?A________,B________。
(2)Am中的m值是________。
查看答案和解析>>
科目: 来源: 题型:022
将白净细砂与Mg混合,灼烧到反应物转变为灰黑色的化合物A和白色的化合物B后,冷却,再向其中滴加盐酸,立即有气体逸出,并迅速自燃,则化合物A和B各是什么?写出有关的化学方程式。
查看答案和解析>>
科目: 来源: 题型:022
钛(Ti)因为具有神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应。红热时却可与常见非金属单质反应。钛是航空、军工、电力等方面的必需原料,地壳中含钛矿石之一称金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合在高温条件下通入Cl2制TiCl4和一种可燃性气体。该反应的化学方程式为___________________,该反应的还原剂是_____________________________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛
(1)写出此反应的化学方程式_______________________________。
(2)如何由上述所得产物中获取金属钛?简述步骤并写出有关反应的化学方程式。________________________________。
查看答案和解析>>
科目: 来源: 题型:022
溶液A可能含有等物质的量浓度的Cl-,AlO2-,S2-,SiO32-,SO32-,PO43-中的几种,现进行如下实验。①取5mLA溶液,往其中通入定量的CO2,得到白色沉淀B,B可完全溶于盐酸;②另取5mLA溶液,往其中加入盐酸,生成气体C,将C通入CuSO4溶液中,有黑色沉淀D生成。根据上述实验,回答下列问题:
(1)溶液A中肯定存在_________离子;
(2)溶液A中肯定不存在___________离子,其理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com