
科目: 来源:辽宁省大连市第三十六中学2009-2010学年高二6月月考化学试题 题型:022
已知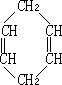 可简写为
可简写为![]() .现有某化合物W的分子结构可表示为:
.现有某化合物W的分子结构可表示为:![]() .
.
(1)W的分子式为________;
(2)W的一氯代物有________种.
(3)下列有关W的说法不正确的是________(填编号);
a.能发生还原反应
b.能发生氧化反应
c.能发生加聚反应
d.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
(4)写出W的芳香族同分异构体(能发生聚合反应)的结构简式________,该聚合反应的化学方程式为________.
(5)W属于________(填编号).
a.芳香烃
b.环烃
c.不饱和烃
d.炔烃
查看答案和解析>>
科目: 来源:江西省吉安一中2010-2011学年高三开学模拟考试化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江西省吉安一中2010-2011学年高三开学模拟考试化学试题 题型:022
已知在同一碳原子上连有两个羟基的化合物是极不稳定的,它会自动脱去一分子水生成含有羰基的化合物.化合物A为苯的同系物,aLA的蒸汽完全燃烧消耗相同状况下O2 9a L.关于A的一系列转化关系如图所示.
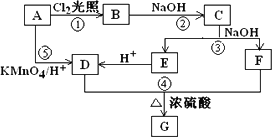
其中C能发生银镜反应,并且C在浓碱条件下可以发生自身氧化还原反应生成E和F.回答有关问题
(1)反应①②③④⑤中,不属于取代反应的有________(填序号).
(2)B是反应①的产物之一,写出反应①的其他可能产物中摩尔质量为195.5 g/mol的结构简式________.
(3)写出反应④的化学方程式________.
(4)G属于芳香酸苯酚酯类的同分异构体有________种,写出其中任意一种的结构简式________.
查看答案和解析>>
科目: 来源:黑龙江省五大连池市高级中学2009-2010学年高一下学期期末理科化学试题 题型:022
已知W、X、Y、Z为四种短周期元素,原子序数逐渐增大.其中W形成的单质是自然界中最轻的气体;X原子的最外层电子数是次外层电子数的2倍;元素是地壳中含量最多的元素;Z元素是短周期中原子半径最大的元素.回答下列问题:
(1)X6W6的结构简式为________,分子空间构型为________.
(2)Y与Z形成的两种常见化合物的电子式分别为________和________
(3)由W、X、Y三种元素形成的最简式为XW2Y的化合物有A和B两种,其中A的相对分子质量是60,是日常生活中的一种调味品的主要成分,则A的结构简式为________;B的相对分子质量是A的3倍,在正常人的血液里含有0.1%的B,则B的分子式________.将B物质的溶液与新制的Cu(OH)2悬浊液共热,观察到得现象是________.
(4)将B在酒化酶的作用下可制得另外一种具有特殊香味的液态有机物C,同时得到一种能导致温室效应的气体.写出该反应的化学方程式________
(5)C是一种可以再生的清洁燃料,写出其燃烧的化学方程式________.
C还可以在Cu或Ag的催化作用下被氧气氧化成具有刺激性气味的液体,该反应的化学方程式为____________.
查看答案和解析>>
科目: 来源:河北省蔚县一中2009-2010学年高一下学期期末考试化学试题 题型:022
现有下列短周期元素性质的相关数据:

请回答下列问题:
(1)②和③形成的化合物类型为________(填“离子”或“共价”)化合物;
(2)元素①的金属性比元素⑥要________(填“强”或“弱”),试从原子结构方面解释其原因:________________;
(3)在自然界中,元素④的存在形态为________,工业上粗制该元素单质的化学方程式为________________;
(4)⑥的单质与浓NaOH溶液反应的离子方程式是________________;
(5)实验室现有元素①的单质和某未知金属单质M,请简要写出比较两者金属性强弱的一种实验方案________________.
查看答案和解析>>
科目: 来源:河北省蔚县一中2009-2010学年高一下学期期末考试化学试题 题型:022
已知:乙醛在一定条件下可被氧气氧化为乙酸.A是石油裂解主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志.下列是有机物之间的转化关系:
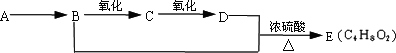
查看答案和解析>>
科目: 来源:福建省漳州市华安一中2009-2010学年高二下学期期末考试化学试题 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
科目: 来源:福建省漳州市华安一中2009-2010学年高二下学期期末考试化学试题 题型:022
氮及其化合物在生活、生产和科技等方面有重要的应用.请回答下列问题:
(1)氮元素基态原子的价电子排布式为________;
(2)在氮气分子中,氮原子之间存放着________个σ键和________个π键;
(3)N2分子中氮氮键的键长________(填“大于”、“小于”或“等于”)
F2分子中氟氟键的键长;
(4)氮元素的氢化物——NH3是一种易液化的气体,该气体易液化的原因是________.
(5)配合物[Cu(NH3)4]C12中含有4个配位键,若用2个N2H4代替其中2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]C12中含有配位键的个数为________.
查看答案和解析>>
科目: 来源:福建省晋江市季延中学2009-2010学年高一下学期期末考试化学试题 题型:022
A是一种重要的化工原料,其产量可以用来衡量一个国家的石油化工水平,D是一种酸性物质,E是具有果香气味的烃的衍生物.A、B、C、D在一定条件下存在如下转化关系(石蜡油含17个碳原子以上的液态烷烃,部分反应条件、产物被省略).

(1)工业上,由石油获得汽油、煤油、石蜡油等成份的方法是________,
(2)写出A、B的结构简式________;
(3)A→B的反应类型是________;B+D→E的反应类型是________反应方程式为:________
(4)实验室常用如图所示装置制取D,请在下图所示方框中补充画出有关仪器,并标明所盛药品的名称.
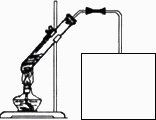
查看答案和解析>>
科目: 来源:福建省晋江市季延中学2009-2010学年高二下学期期末考试化学试题 题型:022
| |||||||||||||||||||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com