
科目: 来源:浙江省杭州学军中学2011届高三第一次月考化学试题 题型:022
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省苍南县钱高、灵溪二高2011届高三上学期第一次月考联考化学试题 题型:022
下图中的甲、乙、丙和丁分别代表一种反应物或生成物,相互转化关系中部分反应条件略.请根据题目要求回答下列问题.

(1)若甲和乙均为含有10个电子的带电粒子,丙和丁均为含有10个电子的分子,写出甲和乙共热时的离子方程式________;
若将丙溶入丁物质中,应选择的吸收装置为________.(填序号).
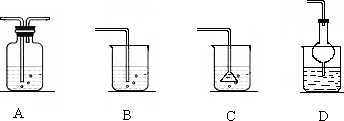
(2)若甲和乙均为含有18个电子的共价化合物,丁为黄色固体,则甲的电子式为________.
(3)若甲是含有10个电子的化合物,乙是含有18个电子的单质分子,写出甲和乙反应的化学方程式________;当乙发生反应时,转移0.1 mol电子,则标况下有________L单质气体乙参加反应.
(4)若甲、乙中均含有常见金属元素,甲为单质,乙中两元素原子的质量比为21∶8,则甲、乙发生反应的化学方程式为________.
(5)若甲和丁为非金属单质,乙和丙为非金属氧化物,则甲和丁可能为________、________(列出常见的两组的名称).
查看答案和解析>>
科目: 来源:辽宁省宽甸第二中学2011届高三第一次月考试化学试题 题型:022
一种用于治疗高血脂的新药灭脂灵(Hepronicate)是按如下路线合成的:

已知:(1)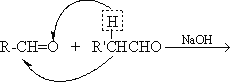 RCHOHCH
RCHOHCH![]() CHO
CHO
(2)![]()
![]() RCHO
RCHO
其中G的分子式为C10H22O3,试回答:
(1)写出结构简式:B________ E________;
(2)上述反应中属于取代反应的是________(填序号);
(3)写出反应方程式:
Ⅰ、反应②________
Ⅱ、反应⑤________
Ⅲ、F与银氨溶液反应:________
查看答案和解析>>
科目: 来源:河北省魏县第一中学2011届高三上学期第一次月考化学试题 题型:022
A、B、C、D、E、X、Y为中学常见的七种物质,它们有如下转化关系(部分产物与反应条件略去):

(1)若A为金属单质,B为氢气,X为盐酸,Y为强碱溶.则A物质的名称是________;D与Y反应的离子方程式为________;
(2)若A、C为同主族元素组成的单质,通常状况下,A为气体,C为液体,Y为金属单质.则A→C的反应类型是________;将X通入A的溶液中,可观察到的现象是________;C→D的化学反应方程式为________.
(3)若A、C为为短周期不同主族元素组成的单质,通常状况下,A、C均为固体,X、Y为气体.则A→C的反应方程式是________;该反应发生时盛有X的装置________(填是、否)需要做什么处理中,如需要怎么处理________(如不需要此问不需作答).为什么:________.
查看答案和解析>>
科目: 来源:河北省魏县第一中学2010-2011学年高二上学期第一次月考化学试题 题型:022
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:福建省三明一中2011届高三第二次月考化学试题 题型:022
铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3![]() Cu(NO3)2+NO↑+NO2↑+H2O.
Cu(NO3)2+NO↑+NO2↑+H2O.
(1)硝酸在该反应中的作用是________,该反应的还原产物是________.
(2)1.2 mol Cu被硝酸完全溶解后,Cu失去的电子数是________,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是________,若用排水法收集这些气体,可得标准状况下的气体体积________.
(3)如果参加反应的Cu和HNO3的物质的量之比是3∶10,写出已配平的该反应的离子方程式:________.
查看答案和解析>>
科目: 来源:浙江省杭州市西湖高级中学2010-2011学年高一上学期开学考试化学试题 题型:022
下图是一些常见物质的转化关系,其中
C是无色无刺激性的气体,且能使澄清石灰水变浑浊;E是一种元污染的清洁能源,其燃烧产物是H.
请根据上图,回答下列有关问题:
(1)红棕色粉末A和气体C、E的化学式分别为:A________、C________、E:________.
(2)G转化为H和A的反应类型是________反应;B转化成E和D的反应类型是________反应.
(3)①A与盐酸反应的化学方程式为:________;
②D和氯气化合生成F的化学方程式为:________.
(4)以上图中无色气体C为中心,延展如下图:

①请写出实现这两个转化的另一反应物J、K的化学式:J________、K________.
②请完善由CO和CaCO3分别转变成无色气体C的转化关系图,在箭号上注明必要的反应条件和其它反应物.
![]()
查看答案和解析>>
科目: 来源:安徽省合肥八中2011届高三第二次月考化学试题 题型:022
X、Y、Z、L、M、N六种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.回答下列问题:
(1)L的原子结构示意图为________;M在元素周期表中的位置为________;前五种元素的原子半径从大到小的顺序是________(用元素符号表示).Z、L两元素的第一电离能大小关系为:________>________(填写元素符号),原因是________.
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,A的分子构型为________,B的结构式为________.
(3)N是人体必需的微量元素,与L同一主族,N原子比L原子多两个电子层,则N的电子排布式为________,其最高价氧化物对应的水化物化学式为________.该族2~5周期元素单质分别与H2反应生成1 mol气态氢化物的反应热如下,表示生成1 mol H2N反应热的是________(填字母代号).
A.+99.7 mol·L-1
B.+29.7 mol·L-1
C.-20.6 mol·L-1
D.-241.8 kJ·mol-1
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q.写出阳极生成R的电极反应式:________;由R生成Q的化学方程式:________.
查看答案和解析>>
科目: 来源:海南省嘉积中学2011届高三上学期教学质量检测化学试题(一) 题型:022
反应①②是重要的化工反应,D、E、F、G为单质,D、E、G、H为气体,且只有E为有色气体,F是常见的金属单质,G是空气中主要成分之一,K是白色胶状沉淀,C的焰色反应为黄色,其物质间的转化关系如下,虚框内是需设计的内容,反应物只能用A~J中的物质:

(1)A的电子式________,H的结构式是________;
(2)A溶液的电解方程式是________;
C+B→J的离子方程式是________;
(3)请设计F→K的最佳途径

(4)按设计得到1 mol K,电解B时转移的电子数目是________,至少需要另加试剂的物质的量是________:________mol,________:________mol,________:________mol(可不填满).
查看答案和解析>>
科目: 来源:广东省高州一中2009-2010学年高二学科竞赛化学试题 题型:022
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为无色液体.反应生成的水均已略去.它们有如下图所示的关系.
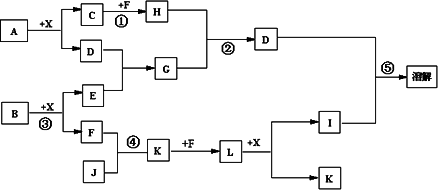
(1)写出化学式:A________ B________ J________.
(2)反应③中每生成1 mol F,转移电子的数目为:________.
(3)反应④的化学方程式为:________.
(4)写出离子方程式分别为:反应②________;⑤________.
(5)反应①中,每1.00 g C与足量的F作用,恢复到25℃放出55.6 kJ热量,写出反应①的热化学方程式 ________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com