
科目: 来源:江西省会昌中学2010-2011学年高二第一次月考化学试题 题型:022
一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
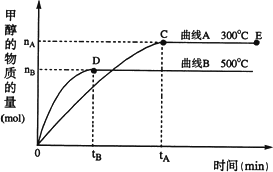
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=________,升高温度,K值________(填“增大”、“减小”或“不变”).
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是(填序号)________
a氢气的浓度减少
b正反应速率加快,逆反应速率也加快
c甲醇的物质的量增加
d重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:________(用化学方程式表示)
查看答案和解析>>
科目: 来源:江西省横峰中学2011届高三第二次月考化学试题 题型:022
X、Y都是芳香族化合物,均为常见食用香精,广泛用于化妆品、糖果及调味品中.1 mol X水解得到1 mol Y和1 mol CH2CH2OH,X、Y的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O.且x分子中碳和氢元素总的质量百分含量约为81.8%.
(1)1个Y分子中应该有________个氧原子.
(2)X的分子式是________.
(3)G和X互为同分异构体,且具有相同的官能团,用芳香烃A合成G路线如下:

①写出A的结构简式________.
②E→F的反应类型是________反应,该反应的化学方程式为________.
③写出所有符合下列条件的F的同分异构体的结构简式:________.
ⅰ.分子内除了苯环无其他环境结构,且苯环上有2个对位取代基.
ⅱ.一定条件下,该物质既能与银氨溶液发生银镜反应也能和FeCl3溶液发生显色反应.
查看答案和解析>>
科目: 来源:江西省横峰中学2011届高三第二次月考化学试题 题型:022
下列各图中的纵坐标表示沉淀的物质的量,横坐标表示加入x的物质的量,请将各图一一对应的反应的代号填入每图下方的括号内.

A.Ca3(PO4)2悬浊液中滴入H3PO4
B.NaAlO2溶液中通入HCl
C.Ba(OH)2溶液中通入SO2
D.石灰水中通入CO2
E.AlCl3溶液中滴入氨水
F.AlCl3溶液中滴入NaAlO2溶液
G.SO2溶液中通入H2S气体
H.稀硫酸中滴入Ba(OH)2溶液
I.AlCl3、MgSO4的混合溶液中加入过量NaOH溶液
J.在盐酸酸化的AlCl3溶液中,滴入KOH溶
K.AlCl3溶液中滴入NaOH溶液
查看答案和解析>>
科目: 来源:江西省白鹭洲中学2011届高三第二次月考化学试题 题型:022
A、B、C、D、E、F、G、H、I、J均为有机化合物,根据以下框图,回答问题:

(1)B分子内有3种等效氢,则B的结构简式为________;C分子结构中具有支链,在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为________.
(2)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为________.
(3)写出⑤的化学反应方程式________.⑨的化学反应方程式________.
(4)①的反应类型________,④的反应类型________,⑦的反应类型________.
(5)与H具有相同官能团的H的同分异构体的结构简式为________.
查看答案和解析>>
科目: 来源:江西省安福中学2011届高三上学期第一次月考化学试题 题型:022
| |||||||||||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:江苏泰兴重点中学2011届高三第一次检测化学试题 题型:022
A.(1)CH3+.CH3-.CH3-都是重要的有机反应中间体,有关它们的说法正确的是________.
A.它们均由甲烷去掉一个氢原子所得
B.它们
互为等电子体,碳原子均采取sp2杂化C.CH3-
与NH3.H3O+互为等电子体,几何构型均为三角锥形D.CH3+
中的碳原子采取sp2杂化,所有原子均共面E.
两个CH3-或一个CH3+和CH3-结合均可得到CH3CH3(2)
锌是一种重要的金属,锌及其化合物有着广泛的应用.①指出锌在周期表中的位置:________周期,________族,________区.
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式________;葡萄糖分子中碳原子杂化方式有________.
③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于________(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在下图中表示[Zn(NH3)4]2+中Zn2+与N之间的化学键.
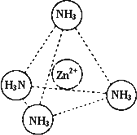
④下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为________;该化合物的晶体熔点比干冰高得多,原因是________.

查看答案和解析>>
科目: 来源:江苏泰兴重点中学2011届高三第一次检测化学试题 题型:022
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2).导电乙炔黑(一种炭黑).铝箔以及有机粘接剂.某回收工艺流程如下:

(1)上述工艺回收到的产物有________.
(2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是________.
(3)碱浸时主要反应的离子方程式为________.
(4)酸浸时反应的化学方程式为________.如果用盐酸代替H2SO4和H2O2的混合液也能达到溶解的目的,但不利之处是________.
(5)生成Li2CO3的化学反应方程式为________.已知Li2CO3在水中的溶解度随着温度升高而减小,最后一步过滤时应________.
查看答案和解析>>
科目: 来源:江苏省常州市横山桥高级中学2011届高三第一次调研考试化学试题 题型:022
某学生课外兴趣小组为了测定镁铝合金中铝的含量,进行了如下实验.将合金3.0克投入足量的100 mL 1.5 mol·L-1烧碱溶液中,充分反应后分离出未反应的镁,然后在溶液中滴加1.0 mol·L-1盐酸,加入盐酸的体积与得到沉淀的数据如下表:

(1)从开始加入盐酸到生成最大量沉淀,溶液中发生反应的离子方程式依次为:
________.
(2)开始沉淀时加入的盐酸体积必须大于________mL,若得到沉淀的量最大时,加入的盐酸体积为________mL.
(3)合金中铝的质量分数为________.
查看答案和解析>>
科目: 来源:吉林省长春外国语学校2011届高三第一次月考化学试题 题型:022
合金A由4种单质组成,经过一系列反应分别进入了沉淀或气体中.
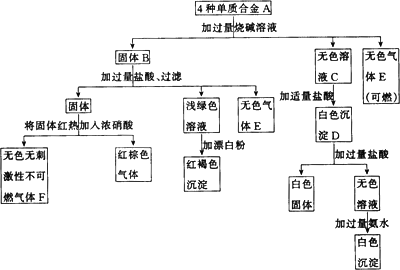
(1)合金A由哪4种元素的单质组成?________、________、________、________.
(2)写出E、F的化学式:E________、F________.
(3)写出合金A中的有关组成与过量烧碱溶液反应生成无色气体E的化学反应方程式:________、________.
(4)写出向无色溶液C加适量盐酸生成白色沉淀D有关反应的离子方程式:
________、________.
查看答案和解析>>
科目: 来源:吉林省长春外国语学校2011届高三第一次月考化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com