
科目: 来源:北京市日坛中学2010-2011学年高一下学期期中考试化学试题 题型:022
(1)在下面元素周期表中全部是金属元素的区域为________.
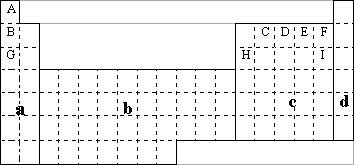
(A)a
(B)b
(C)c
(D)d
(2)G元素与E元素形成的化合物的化学式是________、________,它们都是________(填“共价化合物”或“离子化合物”).表格中十种元素的最高价氧化物对应的水化物中,碱性最强的是________(用化合物的化学式表示,下同),酸性最强的是________,属于两性氢氧化物的是________.
(3)C的氢化物的空间构型为________,请写出这个氢化物与氯气发生取代反应的方程式(只写第一步)________.
(4)现有甲.乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
①用元素符号将甲.乙两元素填写在上面元素周期表中对应的位置.
②甲.乙两元素相比较,金属性较强的是________(填名称),可以验证该结论的实验是________.(填编号)
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目: 来源:黑龙江大庆铁人中学2010-2011学年高二下学期期中考试化学试题 题型:022
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC形成的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为29.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)AC2在H2C(C的氢化物)中的溶解度不大,其主要原因是________.
(2)B的氢化物的分子空间构型是________,其中心原子采取________杂化.
(3)写出化合物AC2的电子式________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为________.
(4)向ESO4中逐滴加氨水至氨水过量,其现象为________;产生此现象的原因(用离子方程式表示)________;________.
查看答案和解析>>
科目: 来源:黑龙江大庆铁人中学2010-2011学年高二下学期期中考试化学试题 题型:022
X、Y、Z、W、N五种元素中,X原子核外的M层中只有两个成对电子,Y原子的外围电子排布式为nsnnpn+1,Z是地壳内含量(质量分数)最高的元素,W的核电荷数是X与Z的核电荷数之和,N在元素周期表的各元素中电负性最大.
(1)Z元素基态原子的电子排布图为________.
(2)W的元素符号是________,在周期表中的位置是________,在形成化合物时它的最高化合价为________.
(3)Y的氢化物的VSEPR模型是________,属于________分子(填极性或非极性),
(4)X的氢化物的沸点________Z的氢化物的沸点(填高于、低于或等于)
原因是________.
(5)用氢键表示式写出N的氢化物分子间存在的氢键________.
查看答案和解析>>
科目: 来源:浙江省杭州学军中学2010-2011学年高二下学期期中考试化学试题 题型:022
| |||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省杭州学军中学2010-2011学年高一下学期期中考试化学试题(实验班) 题型:022
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子甲、乙、丙.
(1)元素F在周期表中的位置是________.
(2)写出元素A、C形成分子C2A4的电子式:________.
(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):________.
(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出其和酸性KMnO4反应的离子方程式:________.
(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.盐X显酸性原因(用离子方程式表示)________.
查看答案和解析>>
科目: 来源:浙江省杭州学军中学2010-2011学年高一下学期期中考试化学试题(实验班) 题型:022
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示.请针对以下三种不同情况回答:

(1)若A、B、C中均含同一种常见金属元素,将A、C的水溶液混合可得B的沉淀
①A、B、C中含有的同一种常见金属元素为________.
②写出A、C的水溶液混合生成沉淀B的离子反应方程式为________.
(2)若A为固态非金属单质,A与X同为第三周期元素,常温常压下C为白色固体,B分子中各原子最外层均为8e-结构.
①B的电子式为________.
②C能与水剧烈反应,生成磷酸和盐酸,反应的化学方程式为________.
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生.
①A中所含有的化学键是________.
②将过量X通入水玻璃溶液中,写出反应的离子方程式________.
③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100 mL溶液,测得溶溶中金属阳离子的浓度为0.5 mol/L.若取相同质量的固体加热至恒重,剩余固体的质量为________g.
查看答案和解析>>
科目: 来源:河北省保北十二县市2010-2011学年高二下学期期中联考化学试题s 题型:022
已知物质A显酸性,请根据以下框图回答问题

F为七原子组成的环状结构,分子式为C6H8O4
(1)A的结构简式为_________
(2)①②③的反应类型分别为_________、_________、_________
(3)化合物B中含有官能团的名称是_________
(4)D和E生成F的化学方程式_________
(5)G生成H的化学方程式_________
(6)写出C的同分异构体中属于酯类物质的结构简式_________(至少写3个)
查看答案和解析>>
科目: 来源:河北省保北十二县市2010-2011学年高一下学期期中联考化学试题 题型:022
元素X、Y、Z、W均为短周期元素,且原子序数依次增大.已知Y原子最外层电子数占核外电子总数的3/4,W-、Z+、X+的离子半径逐渐减小,化合物XW常温下为气体,Z是本周期中除稀有气体元素外,原子半径最大的元素.据此回答下列问题:
(1)W在元素周期表中的位置_________,实验室制取W单质的离子方程式是_________;
(2)A、B均由上述四种元素中的三种组成的强电解质,A是一种强碱,B是某种家用消毒液的有效成分,则A、B的化学式分别为_________、_________;
(3)C是由Y和Z两种元素组成的一种化合物,其中Y和Z的原子个数比为1∶1,则C的电子式是_________.
查看答案和解析>>
科目: 来源:山东省泗水一中2010-2011学年高一下学期期末考试化学试题 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
科目: 来源:山东省泗水一中2010-2011学年高一下学期期末考试化学试题 题型:022
某人设计的糖厂甘蔗渣利用方案如下图所示:

其中:A能催熟水果,B是高分子化合物,D是有水果香味的物质.
请回答以下问题:
(1)“C6H12O6”所示的物质的名称是________,A的电子式为________.
(2)写出下列转化的化学方程式并指出反应类型:
A→B________,反应类型________.
C→D________,反应类型________.
CH3CH2OH→CH3CHO:________,反应类型________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com