
科目: 来源:浙江省浙大附中2012届高三上学期期中考试化学试题 题型:022
单质A、B、C在常温下均为气态,分别由甲、乙、丙三种短周期元素组成;已知丙元素的原子结构中次外层电子数比最外层电子数多1,化合物D在常温下呈液态,G是常见的金属单质,H是常见的蓝色沉淀,各物质间的转化关系如图所示(反应条件多数已略去):

请回答:
(1)在反应①中,已知1 g B完全燃烧生成液态D时,放出142.9 kJ的热量,则表示B的燃烧热的热化学方程式是________.
(2)反应①也可以设计成原电池装置进行,当用铂作电极,用KOH溶液作电解质溶液时,负极的电极反应式是________.
(3)反应③④在通常情况下不能自发进行,框图中的条件a是________,在使反应③④能够发生的装置中,有一个电极材料必须相同,写出该电极反应式________.
(4)反应⑥的离子方程式是________.
(5)甲、乙两元素除形成化合物D外,还可形成一种含有4个原子核和18个电子的化合物,该化合物的电子式是________.
查看答案和解析>>
科目: 来源:浙江省浙大附中2012届高三上学期期中考试化学试题 题型:022
有一瓶澄清溶液,其中可能含有NH![]() 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO![]() 、CO
、CO![]() 、SO
、SO![]() 、AlO
、AlO![]() .取该溶液进行以下实验:
.取该溶液进行以下实验:
①用PH试纸检验,溶液呈强酸性;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝;
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成.
根据上述实验现象,回答下列问题.
(1)由①可以排除________的存在.
(2)由②可以证明________的存在;同时排除________的存在;理由是________.
(3)由③可以证明________的存在;
写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
C________;d________.
(4)由④可以排除________的存在,同时证明________的存在.
查看答案和解析>>
科目: 来源:浙江省杭师大附中2012届高三第三次月考化学试题 题型:022
某研究小组在实验室探究氨基甲酸胺(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)将一定量纯净的氨基甲酸胺固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)![]() 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
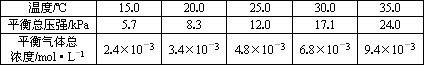
①可以判断该分解反应已经达到平衡的是________.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数:________
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0℃下达到分解平衡.若在恒温下压缩容器体积、氨基甲酸固体的质量________(填“增加”、“减少”、或“不变”)
④氨基甲酸铵分解反应的焓变△H________0(填“>”“=”或“<”=)焓变△S________0(填“>”“=”或“<”=)
(2)
已知:NH2COONH4+2H2O该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率得到c(NH2COO-1)随时间的变化趋势如图所示.
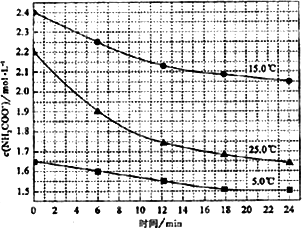
⑤计算25.0℃时,0-6 min氨基甲酸铵水解反应的平均率:________.
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:________.
查看答案和解析>>
科目: 来源:浙江省杭师大附中2012届高三上学期第二次月考化学试题 题型:022
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省东阳中学2012届高三上学期期中考试化学试题 题型:022
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合制备甲醇,该反应的热化学方程式为:CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
(反应1)
该反应的原料CO和H2本身都可作为燃料提供动力,已知这两种物质燃烧的热化学方程式为:
![]() ΔH2=-283 kJ·mol-1
ΔH2=-283 kJ·mol-1
(反应2)
![]() ΔH3=-242 kJ·mol-1
ΔH3=-242 kJ·mol-1
(反应3)
某些化学键的键能数据如下表:
![]()
请回答下列问题:
(1)反应1的焓变ΔH1=________.
(2)CH3OH(g)燃烧生成CO2(g)和H2O(g)的热化学方程式为:
CH3OH(g)+![]() O2(g)
O2(g)![]() CO2(g)+2H2O(g) ΔH4该反应的焓变ΔH4=________.
CO2(g)+2H2O(g) ΔH4该反应的焓变ΔH4=________.
(3)反应1的平衡常数表达式为________.
为提高甲醇的产率,可以采取的措施有________(写出2点).既能提高产率,又能提高反应速率的措施是________.
(4)甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+![]() O2(g)
O2(g)![]() CO2(g)+2H2O(l).其工作原理示意图如下:
CO2(g)+2H2O(l).其工作原理示意图如下:
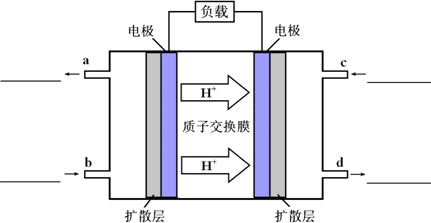
①在上图的横线上标出a、b、c、d四个出入口通入或排出的物质名称(或化学式)________
②负极的电极反应式为________.
查看答案和解析>>
科目: 来源:浙江省东阳中学2012届高三上学期期中考试化学试题 题型:022
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理.常用的处理方法有两种.
方法1:还原沉淀法
该法的工艺流程为:CrO42-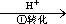 Cr2O72-
Cr2O72-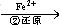 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+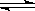 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,该溶液显________色.
(2)能说明第①步反应达平衡状态的是________.
A.Cr2O72-和CrO42-的浓度相同
B.2v(Cr2O72-)=v(CrO42-)
C.溶液的颜色不变
(3)第②步中,还原1 mol Cr2O72-离子,需要________mol的FeSO4·7H2O.
方法2:电解法
该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀.
(4)用Fe做电极的原因为________.
(5)在阴极附近溶液pH升高的原因是(用电极反应解释)________,溶液中同时生成的沉淀还有________.
(6)写出Cr2O72-变为Cr3+的离子方程式________.
查看答案和解析>>
科目: 来源:浙江省东阳中学2012届高三上学期期中考试化学试题 题型:022
工业上用CO生产燃料甲醇.一定条件下发生反应:
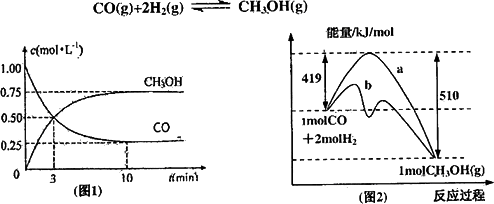
(1)图1是反应时CO和CH3OH(g)的浓度随时问变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=________;
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表使用催化剂后的能量变化.该反应的焓变是________(选填“ΔH<0”或“ΔH>0”)反应,写出反应的热化学方程式________;选择适宜的催化剂,________(填“能”或“不能”)改变该反应的反应热;
(3)该反应平衡常数K的表达式为________,温度升高,平衡常数K________(填“增大”、“不变”或“减小”);
(4)恒容条件下,下列措施中能使![]() 增大的________.
增大的________.
A.升高温度;
B.充入He气
C.再充入1 mol CO和2 mol H2
D.使用催化剂
查看答案和解析>>
科目: 来源:浙江省东阳中学2012届高三12月阶段性检测化学试题 题型:022
现有六种短周期元素A、B、C、D、E、F,其原子序数依次增大,其中B与C、D与F分别位于同一周期,A与D、C与F分别位于同一主族,且A、D两元素原子的质子数之和是C、F两元素原子质子数之和的一半.又知六种元素所形成的常见单质在常温常压下三种是气体,;种是固体.请回答下列问题:
(1)B元素单质的电子式________,F元素氧化物的晶体类型为________.
(2)由A、C两元素可组成X、Y两种化合物,X在MnO2作用下可以分解成Y,写出X转化为Y的化学方程式________.
(3)若E是非金属元素,但能表现出一些金属元素的性质.写出E与D的氧化物的水溶液反应的离子方程式________.
(4)一定条件下,A的单质与B的单质充分反应生成6.8 g W气体时,可放出18.48 kJ热量,写出该反应的热化学方程式________.
查看答案和解析>>
科目: 来源:浙江省东阳中学2012届高三12月阶段性检测化学试题 题型:022
描述弱电解质电离情况可以用电离度和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp).
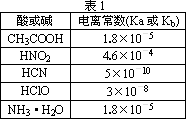
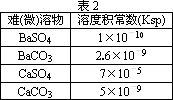
请回答下面问题:
(1)上述四种酸中,酸性最强的是________(用化学式表示).下列能使醋酸溶液中CH3COOH的电离度增大,而电离常数不变的操作是________(填序号).
A.升高温度
B.加水稀释
C.加少量的CH3COONa固体
D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________(选填“酸性”、“中性”、“碱性”),溶液中各离子浓度大小的关系是________.
(3)物质的量1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子的浓度从大到小排列为________.
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2).具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3.现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度达到0.01 mol·L-1以上,则溶液中CO32-物质的量浓度应≥________mol·L-1
查看答案和解析>>
科目: 来源:浙江省东阳中学2011-2012学年高二上学期12月阶段性检测化学试题 题型:022
烯烃通过臭氧化并经锌和水处理得到醛或酮.例如:
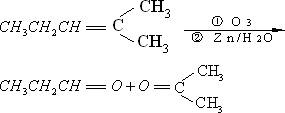
上述反应可用来推断烯烃的结构.一种链状单烯烃A通过臭氧化并经锌和水处理得到B和C.化合物B含碳69.8%,含氢11.6%,B无银镜反应,催化加氢生成D.D在浓硫酸存在下加热,可得到能使溴水褪色且只有一种结构的物质E.反应图示如下:
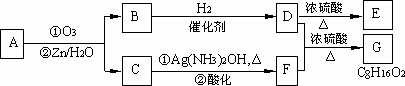
(1)A的结构简式为________.
(2)D→E的反应类型为________;B中含有官能团的名称________.G物质中有无手性碳原子?________.D物质的核磁共振谱图中有几个峰?________.
(3)写出化学方程式:C→F________.D+F→G________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com