
科目: 来源:2001~2002学年度第二学期形成性练习 题型:038
用足量的铜与500mL稀![]() 完全反应后,将溶液小心蒸干,得到
完全反应后,将溶液小心蒸干,得到![]() 晶体90.75g,试计算:
晶体90.75g,试计算:
(1)有多少克铜被氧化?
(2)原稀![]() 的物质的量浓度是多少?
的物质的量浓度是多少?
(3)反应中有多少克硝酸被还原?
查看答案和解析>>
科目: 来源:2001~2002学年度第二学期形成性练习 题型:038
为配制某培养液,需要用![]() 和
和![]() (物质的量之比3∶1)的混合液,每升混合液中含磷元素3.1g.现用4.0mol/L
(物质的量之比3∶1)的混合液,每升混合液中含磷元素3.1g.现用4.0mol/L ![]() 溶液和固体NaOH配制2.0L混合液,问需取该
溶液和固体NaOH配制2.0L混合液,问需取该![]() 溶液多少mL?NaOH多少克?
溶液多少mL?NaOH多少克?
查看答案和解析>>
科目: 来源:2001~2002学年度第二学期形成性练习 题型:038
由![]() 和
和![]() 组成的混合气体10mL,装入试管中,再倒置于盛有水的水槽里,一段时间后,试管内剩余气体为1mL.求原混合气体中
组成的混合气体10mL,装入试管中,再倒置于盛有水的水槽里,一段时间后,试管内剩余气体为1mL.求原混合气体中![]() 和
和![]() 各多少mL(气体体积均为同温同压下测定).
各多少mL(气体体积均为同温同压下测定).
查看答案和解析>>
科目: 来源:高考化学专项练习 题型:038
由人尿分离出来的结晶化合物A,熔点187~188℃.对A做下列实验:
(1)测得A的蒸气密度为8.0g/L(已折合成标准状况).取17.92g A完全燃烧,生成的气体通过浓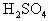 ,增重8.10g;剩余的气体再通过碱石灰,增重39.60g.另取17.92g A完全分解,可得标准状况下的氮气11.2L.试求A的分子式.
,增重8.10g;剩余的气体再通过碱石灰,增重39.60g.另取17.92g A完全分解,可得标准状况下的氮气11.2L.试求A的分子式.
(2)又知A和足量的6mol/L盐酸混合加热,可以完全水解,1mol A水解成1mol B和1mol C,已知A、B、C三物质均含一个羟基,B仅由C、H、O三种元素组成,其物质的量之比为7∶6∶2,C俗名甘氨酸,试推A的结构式.
查看答案和解析>>
科目: 来源:高考化学专项练习 题型:038
有一硝酸盐晶体,分子式为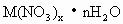 ,经测定分子量为242,将2.42g该晶体溶于水配成200mL溶液,将此溶液置于装有惰性电极的电解池中进行电解,若有0.02mol电子转移给金属离子时,溶液中金属离子全部析出,经称量阴极增重0.64g,试计算:(1)金属M的原子量及x和n值.(2)若电解时溶液体积变化可忽略不计,则电解后溶液的pH是多少?
,经测定分子量为242,将2.42g该晶体溶于水配成200mL溶液,将此溶液置于装有惰性电极的电解池中进行电解,若有0.02mol电子转移给金属离子时,溶液中金属离子全部析出,经称量阴极增重0.64g,试计算:(1)金属M的原子量及x和n值.(2)若电解时溶液体积变化可忽略不计,则电解后溶液的pH是多少?
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:038
某空气污染监测仪是根据SO2和Br2的定量反应来测定空气中SO2含量的:
SO2+Br2+2H2O上述反应的溴,来自一个装有酸性(H2SO4)KBr溶液的电解槽阳极上的氧化反应,电解槽的阳极室与阴极室隔开.当测量某地区空气中SO2的含量时,空气(经过除尘)以1.5×10-4m3/min的流速进入电解槽的阳极室,电流计显示每秒通过电子是8.56×10-11mol,此条件下能保持溴浓度恒定并恰好与SO2反应(空气中不含其他能与溴反应的杂质)
(1)写出监测过程中发生的主要化学反应方程.
(2)计算该地区空气中SO2的含量(g·m-3空气).
(3)该电流计显示的电流强度值为多少安?
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:038
某造纸厂排放的废烧碱水(内含Na2CO3)流量是100mL·s-1,为了测定废碱的浓度,某环保小组取样250mL废碱液,稀释10倍后再取出50mL,平均分成2份,分别用0.1200mol·L-1盐酸滴定.第一份采用甲基橙作指示剂,耗去盐酸24.20mL,第二份用酚酞作指示剂,耗去盐酸17.4mL,试计算:
(1)废烧碱液中CNaOH,![]() 各为多少?
各为多少?
(2)该环保小组想用1.2mol·L-1的废盐酸来中和上述废烧碱液,理论上盐酸的注入流量应为多少?
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:038
钨酸钠Na2WO4和金属钨在隔绝空气的条件下加热得到一种具有金属光泽的、深色的、有导电性的固体,化学式NaxWO3.用x射线衍射法测得这种固体的立方晶胞的边长a=3.80×10-10m,用比重瓶法测得它的密度ρ=7.36g·cm-3.已知相对原子质量:W=183.85、Na=22.99、O=16.00、NA=6.022×1023mol-1,求这种固体的组成中的x值.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:038
在常压和120℃时,在密闭容器中充入H2S和O2的混合气体共100mL,用电火花点燃,经充分反应后,恢复到原状况,测定容器内残留气体体积,经测定,残留气体体积V随原混合气体中O2的体积![]() 增加而变化,其关系如下图所示.
增加而变化,其关系如下图所示.
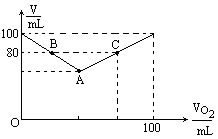
(1)将图中A、B、C各点的数据填入下表.

(2)讨论V和![]() 的关系并用含V和
的关系并用含V和![]() 的函数式表示.
的函数式表示.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com