
科目: 来源:黄冈中学 高一化学(下册)、§7.1 碳族元素(2) 题型:038
有三种不同质量比的氧化铜与炭粉的混合物样品①,②,③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为多少克?
(2)乙取样品②a g强热,生成的气体不能使澄清的石灰水变浑浊。再将反应后的固体与足量的稀硝酸微热,充分反应后,有b g固体剩余,写出该剩余固体的化学式。样品②中氧化铜质量为多少克?(以含a,b的代数式表示)
(3)丙称量样品③强热,剩余的固体质量比原样品减小了c g,若该固体为金属铜,则样品③中氧化铜的物质的量(n)的取值范围是多少。
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§7.1 碳族元素(1) 题型:038
向300mLKOH溶液中缓慢通入一定量的![]() 气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
气体,充分反应后,在减压低温下蒸发溶液,得到白色固体。请回答下列问题:
(1)由于![]() 通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。
通入量不同,所得到的白色固体的组成也不同,试推断有几种可能的组成,并分别列出。
(2)若通入![]() 气体2.24L(标准状况下),得到11.9g的白色固体。通过计算确定此白色固体是由哪些物质组成的,其质量各为多少?所用的KOH溶液的物质的量浓度为多少?
气体2.24L(标准状况下),得到11.9g的白色固体。通过计算确定此白色固体是由哪些物质组成的,其质量各为多少?所用的KOH溶液的物质的量浓度为多少?
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§6.4 环境保护(1) 题型:038
某工厂处理![]() 废气时采用“将
废气时采用“将![]() 转化为
转化为![]() ”的方法。该厂初步处理后的废气中氧气的体积分数为10%,二氧化硫的体积分数为0.2%。使废气在400℃时以
”的方法。该厂初步处理后的废气中氧气的体积分数为10%,二氧化硫的体积分数为0.2%。使废气在400℃时以![]() 的速率通过催化剂层(将二氧化硫氧化)与速率为20L/h的氨气相混合,再喷水使之发生反应:
的速率通过催化剂层(将二氧化硫氧化)与速率为20L/h的氨气相混合,再喷水使之发生反应:![]() ,将所得溶液在结晶装置中处理,可得硫酸铵晶体。将气体都折合成标准状况后进行计算。
,将所得溶液在结晶装置中处理,可得硫酸铵晶体。将气体都折合成标准状况后进行计算。
(1)该工厂为什么将废气以![]() 的速率与速率为20L/h的氨气混合为最佳配比?
的速率与速率为20L/h的氨气混合为最佳配比?
(2)若该厂每天排放![]() 的这种废气,按上述方法该厂每月(若按30天计算)可得硫酸铵多少吨?消耗氨气多少立方米?
的这种废气,按上述方法该厂每月(若按30天计算)可得硫酸铵多少吨?消耗氨气多少立方米?
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§6.4 环境保护(1) 题型:038
某工厂的燃料煤中硫的质量分数为0.32%,该厂每天烧这种煤100t。
(1)有人设计向该厂燃料煤中掺入生石灰,可排除![]() 的污染,试写出有关的化学方程式:________。
的污染,试写出有关的化学方程式:________。
(2)若不采取任何措施,每天该工厂排出的![]() 体积是多少L(标准状况)?________。
体积是多少L(标准状况)?________。
(3)若将煤中的硫转化为硫酸(设硫的转化率为80%),每天可制得98%(质量分数)的硫酸多少吨?
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§6.3 硫酸(2) 题型:038
向铜片中加入115mL某浓度的硫酸,在加热条件下反应,待铜片全部溶解后,将其溶液稀释到500mL,再加入足量锌粉,使之充分反应,收集到2.24L(标准状况)气体。过滤残留固体,干燥后称量,质量减轻了7.5g。求原硫酸的物质的量浓度。
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§5.4 化学键(2) 题型:038
在有机溶剂里若mmol![]() 与mmol
与mmol![]() 定量地完全反应,生成4mmolHCl,同时得到一种白色固体R。R的熔点为113℃,在减压下50℃即可升华,在1Pa下测得R蒸气的密度折算成标准状况下为
定量地完全反应,生成4mmolHCl,同时得到一种白色固体R。R的熔点为113℃,在减压下50℃即可升华,在1Pa下测得R蒸气的密度折算成标准状况下为![]() 。试回答:
。试回答:
(1)通过计算推导R的化学式;
(2)分子结构测定表明,R分子为环状,且同种元素的原子在R分子重化合价相同,用单键“—”和双键“=”把分子里的原子连起来,写出R的结构式。
查看答案和解析>>
科目: 来源:黄冈中学 高一化学(下册)、§5.2 元素周期律(1) 题型:038
元素R的气态氢化物化学式为![]() 。在标准状况下,8.5g
。在标准状况下,8.5g ![]() 气体的体积是5.6L。将5.1g
气体的体积是5.6L。将5.1g![]() 气体通入200mL
气体通入200mL ![]() 的
的![]() 溶液中正好完全反应,并生成黑色沉淀。
溶液中正好完全反应,并生成黑色沉淀。
(1)求![]() 的式量;
的式量;
(2)推断x的值,并确定R元素的名称。
查看答案和解析>>
科目: 来源:全程教与学 题型:038
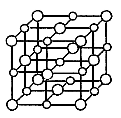
如图所示,食盐(NaCl)晶体是由钠离子和氯离子组成,且都是等距交错排列.已知食盐的摩尔质量为58.5g·![]() ,食盐的密度是 2.2g·
,食盐的密度是 2.2g·![]() ,阿伏加德罗常数为6.0×1023
,阿伏加德罗常数为6.0×1023![]() ,在食盐晶体中两个距离最近的钠离子中心间的距离最接近于下面四个数值中的哪一个
,在食盐晶体中两个距离最近的钠离子中心间的距离最接近于下面四个数值中的哪一个
查看答案和解析>>
科目: 来源:高中化学习题 题型:038
某烷烃和烯烃的混合气2.24L(标准状况),在氧气中点火使其燃烧,燃烧产物通过浓硫酸后,可使浓硫酸质量增加4.05g;再将剩余气体通过碱石灰,可使碱石灰质量增加6.60g.另取等量原混合气,通入足量溴水中,可使溴水质量增加1.05g.试通过计算回答该烷烃和烯烃的分子式和它们的体积比.
查看答案和解析>>
科目: 来源:高中化学习题 题型:038
有一瓶白色固体,取少量置于试管中加热,固体逐渐消失,产生水蒸气和其他两种气体,试管口除少量水珠外,没有任何残留物.取0.350g这种固体跟过量碱液反应,生成一种能使湿润红色石蕊试纸变蓝的气体,这些气体正好能和30.0mL![]() 反应;另取0.350g该固体跟足量盐酸反应,放出一种无色、无臭的气体,将这些气体通入过量的澄清石灰水中,得到0.400g白色沉淀.
反应;另取0.350g该固体跟足量盐酸反应,放出一种无色、无臭的气体,将这些气体通入过量的澄清石灰水中,得到0.400g白色沉淀.
(1)计算0.350g固体中含有的阴离子和阳离子的物质的量.
(2)根据实验及计算结果判断白色固体是什么?写出判断的依据.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com