
科目: 来源: 题型:058
有下列实验装置:
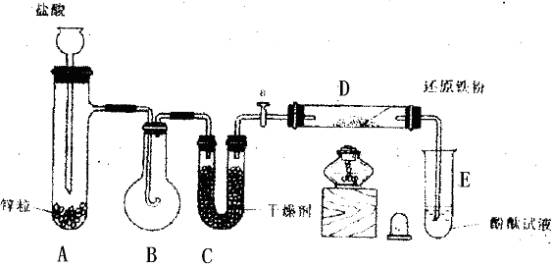
示意图中A是简易的氢气发生器,B是大小适宜的圆底烧瓶,C是装有干燥剂的U形管,a是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞试液的试管。
实验前先检查实验装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A中加入一定量浓度适当的盐酸,发生氢气。经必要的“操作”[见问题(2)]后,在导管的出口处点燃氢气,然后如图所示套上烧瓶B,塞紧瓶塞,氢气在烧瓶中继续燃烧。用酒精灯加热反应管D中的还原铁粉,待B中氢气的火焰熄灭后,打开活塞a,气体通过反应管D进入试管E中,使酚酞试液呈红色;请回答下列问题。
(1)实验前如何检查装置的气密性?
(2)点燃氢气前必须进行操作 ,进行该操作的方法是 。
(3)写出B、D中分别发生的化学反应方程式:
B中:
D中:
(4)C中所盛干燥剂的名称是 ;该干燥剂的作用是 。
查看答案和解析>>
科目: 来源: 题型:058
用Na2SO3和硫粉在水溶液中加热反应,可制得Na2S2O3。10℃和70℃时,Na2S2O3在100 g水中的溶解度分别为60.0 g和212 g。常温下,从溶液中析出的晶体是Na2S2O3•5H2O。Na2S2O3在酸性溶液中立即完全分解:Na2S2O3+2HCl=S↓+SO2↑+H2O+2NaCl。现取15.1 g,溶于80.0 mL水。另取5.00 g硫粉,用少许乙醇润湿后(以使硫能被水浸润),加到上述溶液中。用小火加热至微沸,反应约1小时后过滤。滤液在100℃经蒸发、浓缩、冷却至10℃后析出Na2S2O3•5H2O晶体。
(1)若加入的硫粉不用乙醇润湿,对反应的影响是 。
A.会降低反应速率 B.需要提高反应温度
C.将增大反应体系的PH D.会减少产量
(2)反应1小时后过滤,其目的是 。
(3)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,最可能存在的无机杂质是 。它是由 而产生的。如果滤液中该杂质的含量不很低,其检测的方法是: 。
查看答案和解析>>
科目: 来源: 题型:058
四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃;金属锡的熔点为231℃。拟利用以下仪器,设计组装一套实验装置。用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)。
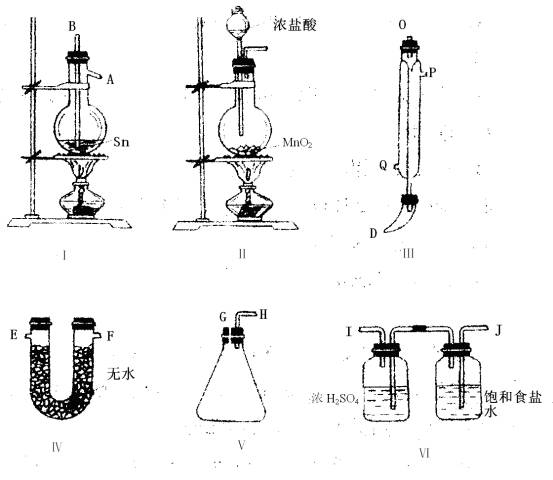
请回答下列各个问题。
(1)用玻璃管(未画出)连接上述装置,正确的顺序是(填各接口的代码字母)( )接( )、( )接( )、( )接( )、( )接( )、( )接( );
(2)装置Ⅵ的作用是 ;装置Ⅳ的作用是 ;
(3)冷凝管里冷却水的流向是从 进入,从 流出;
(4)实验时应先点燃 处酒精灯,加热温度应大于 ℃,待 即可停止加热。
(5)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,那么四氯化锡水解的化学方程式为 ;
(6)如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是 ;
(7)为了防止污染空气,在装置的最后应 。
查看答案和解析>>
科目: 来源: 题型:058
某研究性学习小组在做Na2O2与水反应实验时,发现Na2O2与水反应后的溶液中滴加酚酞试液呈现红色,但红色很快褪去,甲、乙、丙三同学对此现象分别作了如下推测:
甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去。
乙:因为所加水的量较少,红色褪去可能是生成的NaOH溶液浓度较大的影响。
丙:Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲同学的推测是否正确的方法是_______________,验证乙同学的推测是否正确的方法是_______________;当出现________现象时,即可说明丙同学的推测正确。
(2)有同学提出用定量的方法探究丙同学方案中是否含有H2O2,其实验方法为:称取
2.6 g Na2O2固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论。
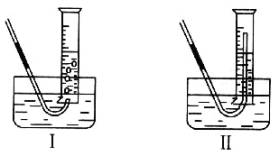
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的________,理由是___________。
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为______(选填“100 m L”、“200 m L”、“500 m L”或“1000 m L”)。
查看答案和解析>>
科目: 来源: 题型:058
怎样除去下列物质中的杂质,要求写出需要加入的试剂名称或方法。
(1)液溴中混有少量氯(Cl2)
(2)食盐中混有少量碘(I2)
(3)氧气中混有少量氢气和氯气(H2、Cl2)
(4)烧瓶内有制氯气的褐色污迹(MnO2)
查看答案和解析>>
科目: 来源: 题型:058
(1)把一小块钠暴露在空气中,观察到以下现象,试在右栏写出对应的化学方程式。
|
主要现象 |
有关化学方程式 |
|
金属钠表面变暗 |
|
|
过些时候有液滴出现 |
|
|
再过些时候出现白色晶体 |
|
|
最后变成白色粉末 |
|
(2)一小块钠在空气中久置后,质量变为原来的62/23倍,则久置后的成分是( )
A.Na2CO3
B.Na2O2
B.NaOH
D.Na2CO3·H2O
(3)钠的用途很广,其中钠钾合金可作原子反应堆的导热剂,简述其原理。
查看答案和解析>>
科目: 来源: 题型:058
回答下面问题:
(1)在进行沉淀反应的实验时,如何认定沉淀已经完全?
_____________________________________________________________________________________________________________________________________________________________________________________________________________________.
(2)中学化学实验中,在过滤器上洗涤沉淀的操作是
_____________________________________________________________________________________________________________________________________________________________________________________________________________.
查看答案和解析>>
科目: 来源: 题型:058
如下图所示,写出各步变化的化学方程式,并回答有关问题:
【注:①KCl ②MnO2 ③石蕊 ④Zn ⑤CuO ⑥Fe(OH)3 ⑦AgNO3 ⑧石灰石 ⑨石蕊 ⑩干红布条 11湿红布条 12H2S溶液 13NaI和CCl4 14KI淀粉
15NaOH溶液】
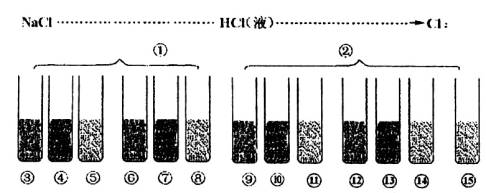
(1)反应方程式________________________体现浓硫酸的________性。
(2)反应方程式________________________体现浓盐酸的________性。
(3)现象______________________________体现盐酸的________性。
(4)现象________反应方程式________体现盐酸的________性,盐酸在反应中做________剂。
(5)现象________反应方程式________。
(6)现象________反应方程式________反应类型________是否氧化还原反应________。
(7)现象________反应方程式________常用于检验________离子。
(8)现象________反应方程式________此反应常用于制取________生成的气体,通入澄清石灰水现象________常用于检验________离子的存在。
(9)现象________说明氯气的水溶液是________性,且具有________性。
(10)现象________________________解释原因________________________________。
(11)现象________________________解释原因________________________________。
(12)现象________________________反应方程式________________,说明氯和硫比较________氧化性较强。
(13)现象_______________解释原因________________________。
(14)现象________________反应方程式________________解释原因________。
(15)现象________________反应方程式________实验室制氯气时,此反应常用于________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com