
科目: 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:058
为了探究HClO的漂白性,某同学设计了如下的实验.
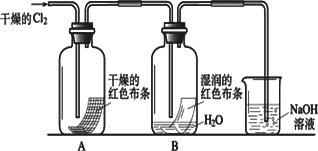
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是________;从集气瓶B中湿润的红色布条的现象可得出的结论是________,其中发生的反应的化学方程式为________.
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是________.
(3)烧杯中溶液所起的作用是________,烧杯中所发生反应的化学方程式为________.
(4)为保证实验安全,当氯气以每分钟1.12 L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2 mol·L-1的NaOH溶液的体积至少应为多少?(写出计算过程)
查看答案和解析>>
科目: 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:058
A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
(1)写出A、B、D的化学式:A.________,B.________,D.________.
(2)写出反应①②的离子方程式
①________.
②________.
(3)检验D的水溶液中的阳离子的方法是:________.将D溶液逐滴加入沸水中会产生一种红褐色的澄清液体.有同学认为该液体中的分散质粒子直径应该在1 nm~100 nm之间,验证这一想法的简单方法是:________.
(4)如图某同学将A的饱和溶液装满大试管倒置于烧杯中,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
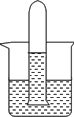
a.你预测气体可能是________.
b.针对你的预测写出验证实验方案:________.
查看答案和解析>>
科目: 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:058
实验室常用以下方法制取氯气:MnO2+4HCl(浓) MnCl2+Cl2
MnCl2+Cl2
(2)在标准状况下生成的Cl2为11.2 L时,参加反应的HCl的物质的量为________,被氧化HCl的质量为________.
查看答案和解析>>
科目: 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:058
有一瓶溶液只含Cl-、CO32-、SO42-、Na+、NH4+、K+、Mg2+七种离子中的某几种.经如下实验:
①原溶液加入过量NaOH溶液,产生白色沉淀;
②将①所得溶液加热,放出使湿润的红色石蕊试纸变蓝的气体;
③原溶液中加BaCl2溶液不产生沉淀.
④原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解.
回答下列问题:
(1)试分析原溶液中一定含有的离子是________,一定不含有的离子是________.
(2)请写出实验①、②、④有关反应的离子方程式:
①产生白色沉淀________;
②产生气体________;
④产生白色沉淀________.
(3)有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)________,并说明理由________.
查看答案和解析>>
科目: 来源:福建省厦门一中2011-2012学年高一上学期期中化学试题 题型:058
用一种试剂除去下列各物质中的杂质(括号内为杂质),写出所用试剂及反应的离子方程式.
(1)BaCl2(HCl):试剂________,离子方程式________;
(2)SO42-(CO32-):试剂________,离子方程式________;
(3)FeCl2(FeCl3):试剂________,离子方程式________.
查看答案和解析>>
科目: 来源:湖南省蓝山二中2011-2012学年高二上学期期中考试化学试题 题型:058
用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
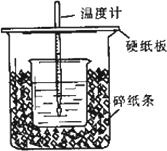
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________.
(2)溶液的密度都是1 g/cm3,实验操作正确,三次测量数据的平均值t2-t1=3.2℃,则实验测得的中和热ΔH=________kJ/mol.(C=4.18 J/g·℃)
(3)大烧杯上如不盖硬纸板,求得的中和热数值________(填“偏大、偏小、无影响”)
(4)如果用60 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量________(填“相等、不相等”),所求中和热________(填“相等、不相等”),简述理由________.
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会________;(填“偏大”、“偏小”、“无影响”).
查看答案和解析>>
科目: 来源:浙江省杭师大附中2012届高三上学期第二次月考化学试题 题型:058
将化学知识系统化,有助于对化学问题的进一步认识和理解.
资料1:化学反应的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应.能引发化学反应的碰撞称之为有效碰撞.
资料2:化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.
资料3:化学反应的能量变化(ΔH)与反应物和生成物的键能有关.在热力学标准态(298 K、1.01×105 Pa)下,由稳定的单质发生反应生成1 mol化合物的反应热叫该化合物的生成热(ΔH).
根据以上资料回答下列问题:
(1)下图是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”);

(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________;

(3)下表是部分化学键的键能数据:
![]()
已知白磷的燃烧热为2378.0 kJ/mol,白磷完全燃烧的产物结构(P4O10)如图所示,则上表中X=________.

(4)下图为氧族元素的氢化物a、b、c、d的生成热数据示意图.请你归纳:非金属元素的氢化物的稳定性与氢化物的生成热(ΔH)之间的关系:________.

查看答案和解析>>
科目: 来源:浙江省台州中学2011-2012学年高一上学期期中化学试题 题型:058
下图是硫酸试剂瓶标签上的内容.

(1)该硫酸的物质的量浓度为________;
(2)实验室用该硫酸配制240 mL 0.46 mol/L的稀硫酸,则
①需要该硫酸的体积为________mL;
②有以下仪器:
A.烧杯
B.100 mL量筒
C.250 mL容量瓶
D.500 mL容量瓶
E.玻璃棒
F.托盘天平(带砝码)
G.10 mL量筒
H.胶头滴管
配制时,必须使用的仪器有________(填代号);
③配制过程中有几个关键的步骤和操作如下图所示:将上述实验步骤A-F按实验过程先后次序排列________.

④该同学实际配制得到的浓度为0.45 mol/L,可能的原因是________
A.量取浓H2SO4时仰视刻度
B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶
D.定容时仰视刻度
查看答案和解析>>
科目: 来源:浙江省东阳中学2011-2012学年高二上学期12月阶段性检测化学试题 题型:058
为了探究苯酚和乙醇分子中羟基上氢原子的活泼性,甲、乙两位同学分别设计如下甲、乙两方案.
方案甲:实验1:取少量无水乙醚于试管中,加入少量金属钠.
实验2:各取3 mL无水乙醚于试管中,分别加入少量等物质的量的苯酚和乙醇,再投入大小相同的钠块.
方案乙:各取少量等物质的苯酚和乙醇于试管中,均在60℃的水浴加热,待苯酚熔化后,各放入相同大小的一小块金属钠.(已知:苯酚的密度为1.07 g/mL)
(1)方案甲设计实验1的目的是________.
(2)方案乙中观察到:在乙醇中,钠很快与乙醇反应产生气体,溶液保持澄清;在苯酚中,钠块表面有少量气泡,且表面产生白色悬浮物,最后白色悬浮物充满苯酚熔融液.
①实验中观察到的白色悬浮物为________;
②苯酚熔融液与钠的反应速率不如无水乙醇与钠的反应快,其可能原因有________.
查看答案和解析>>
科目: 来源:江西省信丰中学2011-2012学年高一上学期第二次月考化学试题 题型:058
实验室里常用Na2O2与H2O反应快速制取少量的O2,下面装置用来制取O2并演示Na在O2中的燃烧实验.

(1)关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管.试判断装置是否漏气________(填“漏气”、“不漏气”或“无法确定”),判断理由是________.
(2)写出A装置中反应的化学方程式并标出电子得失情况:________.
(3)B装置中盛放的试剂是________,其作用是________.
(4)C装置中观察到的现象是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com