
科目: 来源:浙江省宁波市2011-2012学年高一下学期期末考试化学试题 题型:058
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:

请你帮助该同学整理并完成实验报告:
(1)实验目的:________.
(2)实验用品:
仪器:试管、酒精灯、砂纸、镊子、小刀、胶头滴管、滤纸
药品:镁带、钠、铝条、新制氯水、新制饱和硫化氢溶液、2 mol·L-1的盐酸、NaOH溶液、蒸馏水、酚酞、AlCl3溶液
(3)实验内容:(填写题给信息表中的序号)

(4)实验结论:________.
(5)请你补充简单易行的实验方案,证明此周期中另外两种元素的性质递变规律.
________.
查看答案和解析>>
科目: 来源:浙江省瑞安中学2011-2012学年高二下学期期末考试化学试题 题型:058
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑.
步骤2 向处理过的铁屑中加入过量的3 mol·L-1 H2SO4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液.
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体.
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有________(填仪器编号)
①铁架台
②燃烧匙
③锥形瓶
④广口瓶
⑤研钵
⑥玻璃棒
⑦酒精灯
(2)在步骤2中趁热过滤,其原因是________;
(3)在步骤3制的的硫酸亚铁铵晶体常含有Fe3+杂质.检验Fe3+的试剂可以用K4[Fe(CN)6]生成普鲁士蓝沉淀,有关的离子方程式是________.
(4)制得的晶体经过过滤后用无水乙醇洗涤而不用蒸馏水,理由是________;(任说两点)
(5)在25℃时,相同物质的量浓度的(NH4)2CO3、(NH4)2SO4、硫酸亚铁铵三种盐溶液a、b、c,其铵根离子浓度由小到大的排列顺序为________(用a、b、c回答)
查看答案和解析>>
科目: 来源:浙江省瑞安中学2011-2012学年高二下学期期末考试化学试题 题型:058
| |||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省瑞安中学2011-2012学年高二下学期期末考试化学试题 题型:058
某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S等物质,设计了以下实验流程图:
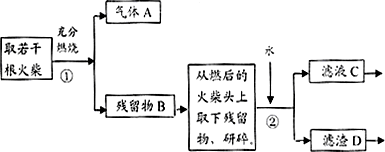
请回答以下问题:
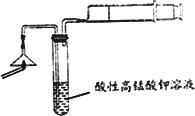
(1)为验证气体A,按下图所示装置进行实验:若能观察到酸性高锰酸钾溶液褪色,即可证明火柴头上含有S元素,请写出气体A使酸性高锰酸钾溶液褪色的离子方程式________.
(2)步骤②的实验操作装置如图所示,该操作的名称是________,其优点是________;

(3)指出图中的错误:
错误①________.
错误②________.
错误③________.
(有几个错误写几个,不一定要填满)
查看答案和解析>>
科目: 来源:甘肃省天水一中2011-2012学年高一下学期第二学段考试化学理科试题 题型:058
| |||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:甘肃省天水一中2011-2012学年高二第二学段测试化学试题 题型:058
某研究性学习小组将一定浓度Na2CO3溶液滴入CuSO4溶液中得到蓝色沉淀.
甲同学认为两者反应生成只有CuCO3一种沉淀;
乙同学认为这两者相互促进水解反应,生成Cu(OH)2一种沉淀;
丙同学认为生成CuCO3和Cu(OH)2两种沉淀.(查阅资料知:CuCO3和Cu(OH)2均不带结晶水)
Ⅰ.按照乙同学的理解Na2CO3溶液和CuSO4溶液反应的化学反应方程式为________;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化.具体操作为①过滤②洗涤③干燥.
Ⅱ.请用下图所示装置,选择必要的试剂,定性探究生成物的成分.

(1)各装置连接顺序为________![]() ________
________![]() ________.
________.
(2)装置C中装有试剂的名称是________.
(3)能证明生成物中有CuCO3的实验现象是________.
Ⅲ.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置进行定量分析来测定其组成.

(1)装置C中碱石灰的作用是________,实验开始时和实验结束时都要通入过量的空气其作用分别是________.
(2)若沉淀样品的质量为m克,装置B质量增加了n克,则沉淀中CuCO3的质量分数为________.
查看答案和解析>>
科目: 来源:甘肃省天水一中2011-2012学年高二第二学段测试化学试题 题型:058
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加KSCN试剂.
(1)若假设1成立,则实验现象是________.
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?________简述你的理由(不需写出反应的方程式)________
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是________,写出发生反应的离子方程式________、________、________.
探究延伸 经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b>a),则混合物中Cu2O的质量分数为
________.
查看答案和解析>>
科目: 来源:天津市天津一中2011-2012学年高二下学期期末考试化学试题 题型:058
用下图所示装置进行实验,将A逐滴加入B中:

(1)若B为CaCO3,C为C6H5ONa溶液,实验观察到小试管内溶液变浑浊,则酸A比碳酸的酸性________(填强、弱).然后往烧杯中加入沸水,可观察到试管C中的现象是________.
(2)若A是浓氨水,B是生石灰,实验中观察到C溶液先形成沉淀,然后沉淀溶解,当溶液恰好澄清时,关闭E,然后向烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则C是葡萄糖与________(写化学式)的混合液,该银镜反应的化学方程式为________,仪器D在此实验中的作用是________.
查看答案和解析>>
科目: 来源:黑龙江省鹤岗一中2011-2012学年高一下学期期末考试化学试题 题型:058
KMnO4溶液与H2C2O4溶液可发生如下反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
(1)该反应速率开始十分缓慢,一段时间后突然加快,这是因为________(填化学式)对该反应具有催化作用.
(2)据此原理,可以利用KMnO4溶液来测定H2C2O4溶液的浓度,具体做法如下:
①准确配制0.10 mol/L的KMnO4溶液
②将KMnO4溶液盛放在________滴定管中(填“酸式”或“碱式”)
③准确量取25.00 mL H2C2O4溶液于锥形瓶中
④进行滴定
滴定终点有什么现象________,是否需要指示剂________(填“是”或“否”)
(3)在下列操作中,会使测定的H2C2O4溶液浓度偏大的是________.
①盛装KMnO4溶液的滴定管用蒸馏水洗净后未用KMnO4溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③盛装H2C2O4溶液的滴定管用蒸馏水洗净后,未用H2C2O4溶液润洗
④滴定后观察滴定管读数时,视线高于刻度线
(4)滴定时所得的实验数据如下,试计算所测H2C2O4溶液的浓度为________mol/L
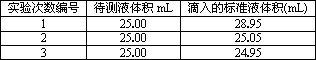
查看答案和解析>>
科目: 来源:江苏省射阳中学2011-2012学年高二下学期期中考试化学试题 题型:058
下表为长式周期表的一部分,其中的编号代表对应的元素.

试填空.
(1)写出上表中元素⑨原子的外围电子排布式________.
(2)请写出与N3-互为等电子体的分子、离子的化学式________,________(各写一种).
(3)在测定①与⑥形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是:________.
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质,写出元素②的氢氧化物与NaOH溶液反应后盐的化学式________.
(5)元素⑩在一定条件下形成的晶体的基本结构单元如下图1和图2所示,则在图1和图2的结构中与该元素一个原子等距离且最近的原子数之比为:________.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com