
科目: 来源:湖南师大附中2011-2012学年高一下学期段考化学试题 题型:058
下表是稀硫酸与某金属反应的实验数据:

分析上述数据,回答下列问题:
(1)实验4和5表明________对反应速率有影响.
(2)在前4次实验中,能表明反应物浓度对反应速率产生影响的实验有________(填实验序号).
(3)其实验6和其实验7表明________对反应速率有影响.
(4)实验中,反应前后溶液的温度变化值(约15℃)相近,推测其原因:________.
查看答案和解析>>
科目: 来源:湖南师大附中2011-2012学年高一下学期段考化学试题 题型:058
某化学课外小组用下图装置制取溴苯.

先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中(A下端活塞关闭).(已知此反应属于放热反应;苯和液溴都易挥发)
(1)写出A中反应的化学方程式________.
(2)A中观察到的现象是出现________色气体.
(3)C中盛放CCl4的作用是________.
(4)要证明苯和液溴发生的是取代反应,而不是加成反应(没有HBr生成),可向试管D中加入AgNO3溶液,产生了淡黄色AgBr沉淀,即得到证明,生成淡黄色AgBr沉淀的离子方程式是________;另一种验证的方法是向试管D中加入紫色石磊溶液,现象是________.
查看答案和解析>>
科目: 来源:黑龙江省大庆铁人中学2011-2012学年高一下学期第一阶段考试化学试题 题型:058
某研究小组探究SO2和Fe(NO3)3溶液的反应.

已知:1.0 mol/L的Fe(NO3)3溶液中c(H+)=0.01 mol/L
请回答:
(1)装置A中反应的化学方程式是________.
(2)为排除空气对实验的干扰,滴加浓硫酸之前应进行的操作是________.
(3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性.
(4)分析B中产生上述白色沉淀的原因可能是:
观点1:________;
观点2:SO2与Fe3+反应;
观点3:在酸性条件下SO2与NO3-反应;
①如果观点2正确,装置B中反应的离子方程式是________.
②如果想验证观点3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验.应选择的试剂是(填序号)________.
a.0.1 mol/L稀硝酸
b.1.5 mol/L Fe(NO3)2溶液
c.6.0 mol/L NaNO3和0.02 mol/L盐酸等体积混合的溶液
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一下学期期末考试化学试题 题型:058
有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20;只有C、E是金属元素;A和E元素原子的最外层电子都只有一个;B和D元素原子的最外层电子数相同,且B元素原子L层电子数是K层电子数的3倍;C元素原子的最外层电子数是D元素原子最外层电子数的一半.由此可知:
(1)C在元素周期表中的位置是________.
(2)D元素最高价氧化物对应水化物的分子式为________,形成E元素最高价氧化物对应水化物的化学键类型________.
(3)D与E形成的化合物属于________(填“离子化合物”或“共价化合物”).
(4)写出C与NaOH溶液反应的离子方程式:________.
查看答案和解析>>
科目: 来源:陕西省长安一中2011-2012学年高一下学期期末考试化学试题 题型:058
某同学为了验证海带中含有碘,拟进行如下实验,请回答相关问题.
(1)第1步:灼烧.操作是将足量海带灼烧成灰烬.该过程中将使用到的硅酸盐质实验仪器除F外还有________(填代号,限填2项).
A.试管
B.瓷坩埚
C.坩埚钳
D.铁三脚架
E.泥三角
F.酒精灯
G.烧杯
H.量筒
(2)第2步:Iˉ溶液的获取.操作是________.
(3)第3步:氧化.操作是依次加入合适的试剂.下列氧化剂最好选用(填代号)________.
A.浓硫酸
B.新制氯水
C.KMnO4溶液
D.H2O2
理由是________.
(4)第4步:碘单质的检验.取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含碘.
查看答案和解析>>
科目: 来源:安徽省铜陵一中2011-2012学年高二6月月考化学试题 题型:058
| |||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:新疆乌鲁木齐市第八中学2011-2012学年高一下学期期中考试化学试题 题型:058
(1)为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内.

①检验的试剂:
A.无水硫酸铜
B.酸性高锰酸钾溶液
C.水
D.氢氧化钠溶液
②除杂试剂:
A.无水硫酸铜
B.乙酸
C.新制的生石灰
D.溴水
③写出除杂时,乙烯发生反应的化学方程式:________________.
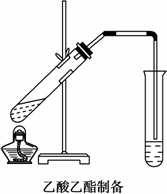
(2)如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀.按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验.
试回答:
在右试管中通常加入________溶液,实验生成的乙酸乙酯,其密度比水________,是有特殊香味的液体.分离右试管中所得乙酸乙酯的操作为(只填名称)________.反应中加入浓硫酸的作用是________.
制备方程式:________
查看答案和解析>>
科目: 来源:新疆乌鲁木齐市第八中学2011-2012学年高一下学期期中考试化学试题 题型:058
用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断________段化学反应速率最快,________段收集的氢气最多.
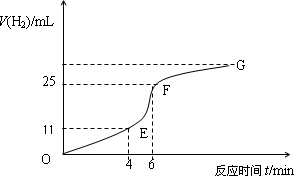
(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是________,一定时间后反应速率逐渐减慢,其原因是________.
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水
B.氯化钠固体
C.氯化钠溶液
D.浓盐酸
E.降低温度
(4)EF段产生H2的反应速率为________mL·min-1.
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2011-2012学年高一下学期期中考试化学试题 题型:058
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
实验一∶他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L),设计实验方案来研究影响反应速率的因素.
甲同学研究的实验报告如下表∶

(1)该同学的实验目的是________;
要得出正确的实验结论,还需控制的实验条件是________.
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验.完成该实验应选用的实验药品可以是(从题中所给药品中挑选)________;

实验二∶
已知∶2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快.从影响化学反应速率的因素看,你的猜想还可能是________的影响.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是________.
A.硫酸钾
B.硫酸锰
C.氯化锰
D.水
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2011-2012学年高一下学期期中考试化学试题 题型:058
用一定浓度的稀盐酸与稀NaOH溶液在下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.已知强酸与强碱的中和热为57.3 KJ/mol,水的比热容为4.2 J/(g·℃),有关热量与比热容的计算公式∶Q=m×c×Δt(Q为热量,m为物质的质量,c为比热容,Δt物质温度的变化值)
回答下列问题∶
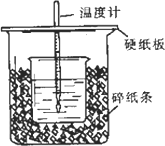
(1)从实验装置上看,图中尚缺少的一种玻璃用品是∶________
(2)将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL).

下列叙述正确的是________
A.做该实验时环境温度为22℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L
D.该实验表明有水生成的反应都是放热反应
(3)V1=30 mL时HCl和NaOH恰好反应,根据题中所给数据算出的温度变化值约为________(保留整数,计算时可将稀溶液的密度及比热容看成与水近似相同,且溶液混合时体积变化忽略不计);而根据上图的温度变化可读出温度变化值约7℃;两者相比所测结果偏低,造成如此现象的原因有∶________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com