
科目: 来源: 题型:058
两种气体A、B分别为0.8mol与0.5mol,在0.4L的密闭容器中反应:2A(g)+3B(g)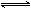 mC(g)+3D(g).经过5min后,测得此时C为0.3mol,D的平均反应速率为
mC(g)+3D(g).经过5min后,测得此时C为0.3mol,D的平均反应速率为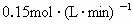 .
.
求:(1)m的值______;(2)A的反应速率________![]() .
.
查看答案和解析>>
科目: 来源: 题型:058
某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:

根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟内时间平均速率为________.
(2)在实验2,A的起始浓度 =________,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________.
=________,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________.
(3)设实验3的反应速率为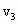 ,实验1的反应速率为
,实验1的反应速率为 ,则
,则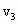 _______
_______ (填“<”、“>”或“=”),且
(填“<”、“>”或“=”),且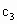 ________1.0mol/L(填“<”“>”或“=”).
________1.0mol/L(填“<”“>”或“=”).
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:058
氧化二氯(Cl2O)是棕黄色的强刺激性气体,沸点3.8℃,溶点-116℃.制备时生成的氧化二氯要及时冷却成固态以便操作和贮存.它与一般有机物接触会发生爆炸;遇水则极易溶解(1∶100),生成次氯酸溶液.制备少量固态氧化二氯可用干燥HgO和Cl2反应,生成物为Cl2O和HgO·HgCl2,装置示意图如图,

回答下列问题:
(1)写出Cl2与HgO反应的化学方程式________.
(2)写出所盛药品的化学式:a是________,b是________.
(3)B中盛的液体c是________,其作用是________.C中盛的液体d是________,其作用是________.
(4)E为冷却装置,其中应盛致冷剂________(干冰、冷水、液态空气).E中所得固体Cl2O中可能含有的杂质是________.
查看答案和解析>>
科目: 来源: 题型:058
20℃时,向足量的硫酸铜饱和溶液中投入1.6g无水硫酸铜,然后蒸去
10g水,再恢复到20℃.问最终可析出硫酸铜晶体(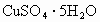 )多少克?(20℃时硫酸铜的溶解度是20g)
)多少克?(20℃时硫酸铜的溶解度是20g)
查看答案和解析>>
科目: 来源:高中化学同步单元练习册 全册 高二年级 题型:058
(1)请从下图中选用适当的实验装置,设计一个最简单的实验,制取和收集一瓶纯净的气体.
请填写:①应选用的装置是________(填写装置的字母).
②所选用的装置的连接顺序是(填各接口的字母).
( )接( ) ( )接( ) ( )接( )
(2)为了测定的分子量,还要进行下列操作:
①将收集好的气体连瓶带塞一起称量,质量为
;
②再将此瓶重新装满空气,用塞子塞好,称量质量为;
③测得此瓶装满水的质量为,已知实验时的温度T(K),压强p(kPa),水的密度
,空气平均分子量29.0,密度
.
试回答:
Ⅰ.本实验的测定原理是________.
Ⅱ.装有的集气瓶质量的称量,应重复操作,直到两次称量结果基本相同,理由是________.
Ⅲ.集气瓶内空气的质量m(空气)是________.(列出算式)
Ⅳ.集气瓶内的质量m(
)是________.(列出算式)
Ⅴ.由实验测得的相对分子质量是________.(列出算式)
查看答案和解析>>
科目: 来源: 题型:058
将10.000g氯化钠、溴化钾和氯化钙的混合物溶于水中,通入足量氯气充分反应,然后把溶液蒸干并灼烧(高温加热),灼烧后残留物的质量为9.813g,若将此残留物再溶于水并加入足量的碳酸钠溶液,所得的沉淀经干燥后质量为0.721g.求原混合物中各化物的质量.(按氯化钠、溴化钾和氯化钙顺序回答)
查看答案和解析>>
科目: 来源: 题型:058
下图中,A是氯气的发生装置,B、C是净化气体的装置,B中盛饱和食盐水,C中盛浓硫酸;D中装铁丝网;反应后E的底部有棕色固体聚集;F是吸收多余气体的装置.
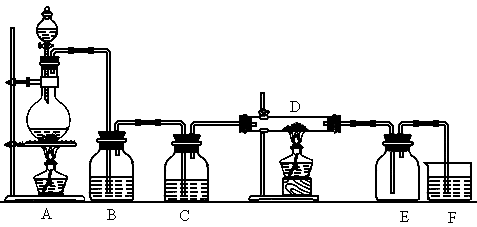
(1)反应前A中分液漏斗中装什么药品_______,烧瓶中装什么药品_______.
(2)通过B是为了除去________;通过C是为了除去__________.
(3)写出A、D、F中发生的化学方程式,属于氧化还原反应的标明电子转移方向和数目.
__________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com