
科目: 来源: 题型:058
乙酸乙酯是无色具有水果香味的液体,沸点77.2℃,实验室某次制取它用冰醋酸14.3mL,95%乙醇23mL.还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液.主要仪器如下图所示:
实验步骤是:
①先向A中蒸馏烧瓶注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用.这时分液漏斗里两种有物的物质的量比约为5∶7.
②加热油浴保温约135~145℃.
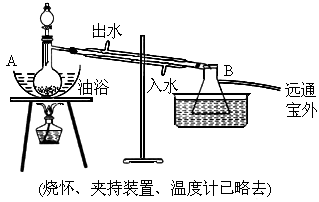
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加料速度使蒸出酯的速度与进料速度大体相等,直到加料完成.
④保持油浴温度一段时间,至不再有液体液后,停止加热.
⑤取下B中的锥型瓶,将一定量饱和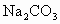 溶液分批少量多次地加到馏出液里,边加边摇荡,至无气泡产生为止.
溶液分批少量多次地加到馏出液里,边加边摇荡,至无气泡产生为止.
⑥将⑤的液混合物分液,弃取水层.
⑦用饱和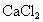 溶液(适量)加入到分液漏斗中,摇荡一段时间后静置,放出水层(废液).
溶液(适量)加入到分液漏斗中,摇荡一段时间后静置,放出水层(废液).
⑧分液漏斗里得到的是初步提的乙酸乙酯粗品.
试回答:
(1)实验中硫酸的主要作用是___________________________.
(2)用过量乙醇的主要目的是___________________________.
(3)用饱和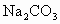 溶液洗涤粗酯的目的是___________________.如果用NaOH浓溶液代替
溶液洗涤粗酯的目的是___________________.如果用NaOH浓溶液代替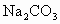 将引起的后果是_____________________.
将引起的后果是_____________________.
(4)用饱和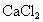 溶液洗涤粗酯的目的是__________________.
溶液洗涤粗酯的目的是__________________.
(5)为什么作③要使加料与馏出的速度大致相等?_________________.
(6)⑧所示的粗酯里还有的杂质是________________.
(7)B中锥型瓶为什么要长导管把蒸气送出室外?___________________.
查看答案和解析>>
科目: 来源: 题型:058
实验室用如图所示装置制取乙酸乙酯.
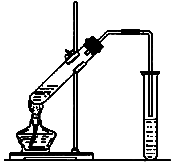
(1)在大试管中配制一定比例的乙醇、乙酸和浓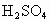 的混合溶液的方法是:_______________________________.
的混合溶液的方法是:_______________________________.
(2)加热前,大试管中加入几粒碎瓷片的作用是_____________;导气管不能插入饱和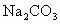 溶液中是为了:_______________.
溶液中是为了:_______________.
(3)浓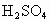 的作用是:①___________;②______________.
的作用是:①___________;②______________.
(4)饱和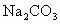 溶液的作用是____________.
溶液的作用是____________.
(5)实验生成的乙酸乙酯,其密度比水____________(填“大”或“小”),有气味.
(6)该实验的主要反应的化学方程式是:_________________.
查看答案和解析>>
科目: 来源: 题型:058
实验室制乙烯,常因温度过高而使烧瓶中液体变黑.为了验证被硫酸氧化确实有二氧化碳气体生成,某同学设计如图所示的A、B、C三个装置进行实验(乙醇与浓硫酸的反应装置省略,并假设装置C中的反应完全).请回答:

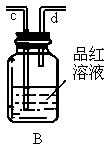
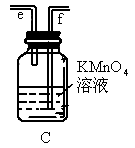
(1)装置B的作用是______________;
(2)三个装置之间的连接顺序是(填写导管口序号a、b、c、d、e、f):
气体发生装置导管口接________,然后________接_________,_________接_________;
(3)装置A、B、C中各有什么现象?
A中__________,B中___________,C中_________;
(4)乙醇与浓硫酸反应的装置与制取____________气体的装置相同;
(5)为了防止制得气体不纯,是否可以把温度控制在较低(140℃)情况下进行反应?为什么?
查看答案和解析>>
科目: 来源: 题型:058
实验室制乙烯,常因温度过高而使烧瓶中有黑色物质生成.为了验证液硫酸氧化确实有二氧化碳气体生成,某同学设计如图所示的A、B、C三个装置进行实验(乙醇与浓硫酸的反应装置省略,并假设装置C中的反应完全).请回答:
(1)装置B的作用是________.
(2)三个装置之间的连接须序是(填写导管序号):
气体发生装置导管口接________,然后________接________,________接________;
(3)装置A、B、C中各有什么现象?
A中_______________________________________________________.
B中_______________________________________________________.

C中________________________________________________________.
(4)乙醇与浓硫酸反应的装置与制取________气体的装置的作用;
(5)为了防止制得气体不纯,是否可以把温度控制在较低(140℃)情况下进行反应?为什么?
查看答案和解析>>
科目: 来源: 题型:058
实验室制乙烯时,常因温度过高而发生副反应.部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑.请用下列编号为①~④的实验装置设计一个实验,以验证上述反应后的混合气中含有二氧化碳、二氧化硫和水蒸气.

(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)________.
(2)装置⑤中的固体药品为_______,用以验证的产物是_______,现象是_______.
(3)装置①中的现象是________,验证_______;装置②中溴水的作用是________;装置③中品红溶液不褪色说明________;此时盛有________的装置④中出现________可以验证________气体的存在.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:058
镁是很活泼的金属,常用作脱硫剂、脱氧剂.在电子工业中利用镁制取硅的反应为2Mg+SiO2 2MgO+Si+372kJ,同时有副反应2Mg+Si
2MgO+Si+372kJ,同时有副反应2Mg+Si Mg2Si发生.Mg2Si遇盐酸迅速反应生成SiH4(硅烷).SiH4在常温下是一种不稳定、易分解的气体.如图所示是进行Mg与SiO2反应的实验装置.
Mg2Si发生.Mg2Si遇盐酸迅速反应生成SiH4(硅烷).SiH4在常温下是一种不稳定、易分解的气体.如图所示是进行Mg与SiO2反应的实验装置.
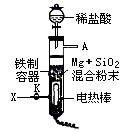
(1)由于O2的存在对该实验有较大影响,实验中应通入X气体作为保护气.X气体应选a(H2),b(N2),c(CO2)中的________(填标号).
(2)实验开始时,必须先通入X气体后,再接通电源加热反应物,其理由是________.
(3)当反应引发后,切断电源,反应能继续进行,其原因是________.
(4)反应结束时,待冷却至常温后,关闭K,从分液漏斗处加入稀盐酸,可观察到导管口A处有闪亮的火星.据此现象可推知________在空气中能自燃.
查看答案和解析>>
科目: 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:058
实验室用纯净氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:
2NH3+3CuO N2+3Cu+3H2O
N2+3Cu+3H2O
现取氧化铜W(CuO)g,反应后称得生成水的质量为W(H2O)g.
有下图实验装置可供选择:
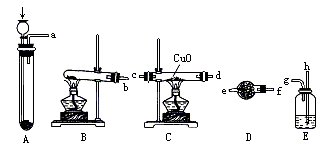
可供选用的固体药品有:
锌、石灰石、生石灰、碱石灰(NaOH,CaO).
可供选用的液体药品有:
浓盐酸、稀盐酸、浓氨水、稀氨水、浓硫酸、稀硫酸.
请据此回答下列各问:
(1)制取氨气的反应方程式是:________.
仪器装置应选择:________.
(2)各仪器按气流方向应当连接的正确顺序是(写仪器进出口编号,并可以重复使用)________.
(3)装置D中的药品是:________,其作用是:________.
装置E中的药品是:________,
其作用是:________.
(4)计算铜相对原子质量的表达式:________;若结果偏高则其原因是________.
查看答案和解析>>
科目: 来源: 题型:058
(1)已知某混合气体的体积百分组成为80.0%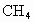 、15.0%
、15.0%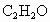 .请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
.请计算0.500mol该混合气体的质量和标准状况下的密度(g/L).
(2)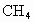 在一定条件下催化氧化可以生成
在一定条件下催化氧化可以生成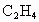 、
、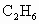 (水和其他产物忽略不计).取一定量
(水和其他产物忽略不计).取一定量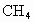 经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中
经催化氧化后得到一种混合气体,它在标准状况下的密度为0.780g/L.已知反应中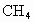 消耗了20.0%,计算混合气体中
消耗了20.0%,计算混合气体中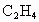 的体积百分含量.(本题计算过程中请保留3位有效数字)
的体积百分含量.(本题计算过程中请保留3位有效数字)
查看答案和解析>>
科目: 来源: 题型:058
在5L闭容器中,通入5mol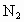 和8 mol
和8 mol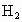 ,在一定条件下生成
,在一定条件下生成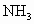 ,反应进行到2 min时,测得容器内有4mol
,反应进行到2 min时,测得容器内有4mol 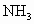 .求:
.求:
(1)2min内的平均速率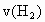 =_______
=_______![]() 、
、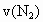 =_______
=_______![]() 、
、 =_______
=_______![]() _
_
(2)2min时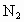 、
、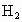 的浓度分别为________
的浓度分别为________![]() 和________
和________![]() .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com