
科目: 来源: 题型:058
工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制CuO粉(含有杂质FeO)用浓盐酸溶解,得到的氯化铜溶液中含有一定量的Fe2+。
|
金属离子 |
pH |
|
|
开始沉淀 |
沉淀完全 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Cu2+ |
4.4 |
6.4 |
|
Fe3+ |
2.7 |
3.7 |
(1)从上表提供的数据看,不能直接将溶液的pH调到9.6,除去Fe2+,其原因是
。
(2)实际生产中先用次氯酸钠的目的是 ,加入次氯酸钠后,溶液的pH值 (增大、减小、不变),然后用试剂将溶液的pH调至适当的范围,即可除去铁杂质。
(3)调节溶液的pH宜选用的试剂是 (填序号)
A.Ba(OH)2 B.MgCO3 C.CuO D.稀HCl
查看答案和解析>>
科目: 来源: 题型:058
某学生为将含有少量杂质铜的氯化铁提纯。拟定以下实验步骤:
①把样品加蒸馏水溶解;②过滤除去杂质;③把滤液加热蒸干,以得到FeCl3晶体。
(1)你以为此方案是否科学;试用化学方程式和简要文字表述其理由。
答 。
(2)请你设计提纯氯化铁的方案(只要求写出提纯步骤,最多只允许6步完成)。
答 。
查看答案和解析>>
科目: 来源: 题型:058
根据实验室中测定硫酸铜晶体结晶水含量的实验,填写下列空白。
(1)从下列仪器选出所需仪器(用标号字母填写) 。
(A)托盘天平(带砝码)、(B)研钵、(C)试管夹、(D)酒精灯、(E)蒸发皿、(F)玻璃棒、(G)坩埚、(H)干燥器、(I)石棉网、(J)三脚架
除上述仪器外,还需要的仪器是 。
(2)某学生实验后得到以下数据:
|
加热前质量 |
加热后质量 |
|
|
W1(容器) |
W2(容器+晶体) |
W3(容器+无水硫酸铜) |
|
5.4 g |
7.9 g |
6.8 g |
请写出结晶水含量(x%)的计算公式(用W1、W2、W3表示)x%= 。
该生测定结果是偏高还是偏低? 。从下列分析中选出该学生产生实验误差的原因可能是(填写字母) 。
A.加热前称量时容器未完全干燥;
B.最后两次加热后的质量相差较大(大于0.1 g);
C.加热后容器未放入干燥器中冷却;
D.加热过程中有少量溅失。
查看答案和解析>>
科目: 来源: 题型:058
A、B、C三种电解质溶液分别装在三个烧杯中,插入石墨电极,并按图所示方式连接电路。闭合开关K后,测得各支路电流强度IⅠ≈IⅡ(其中IⅡ略小)。
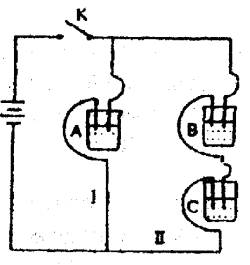
若撤去B,测知电流强度IA<IC;若撤去C,并将A、B两溶液混匀后均分为两等份,再重置于电路Ⅰ、Ⅱ处,测知通过A、B混合溶液的电流强度与先前通过A溶液的电流强度的相对大小关系为:IAB>IA。已知A、B、C分别选自下列溶液:0.1 mol•L-1盐酸、0.1 mol•L-1醋酸、0.1 mol•L-1 NaCl溶液、0.1 mol•L-1硫酸、0.1 mol•L-1 NaOH溶液、0.1 mol•L-1氨水。且25℃,A溶液pH<7。
回答下列问题:
(1)指出A、B、C可能是什么溶液?
A: B: C:
(2)再向C溶液中滴入酚酞试剂呈红色,则C必是 。
(3)将A、B、C分别以等体积进行两两混合,①A和B混合 ②A和C混合 ③B和C混合,混合液中水的电离度由大到小的排列顺序为 (填序号)。
查看答案和解析>>
科目: 来源: 题型:058
如图。A、B为带支管的试管,先在A中加入足量铁粉,再从漏斗中加入一定量的稀硫酸溶液和少量CuSO4溶液。

(1)若装入药品后b、d立即同时关闭,打开a,反应过程中产生的现象为 ,此装置的原理类似于 的工作原理。
(2)若加入药品后马上关闭a、b,打开c、d,A管内的物质充分反应。实验过程中B管内观察到的现象为 ,B中发生反应的化学方程式有 。
查看答案和解析>>
科目: 来源: 题型:058
如图装置中,a是250
mL的烧瓶,其中盛有标准状况下的空气(O2占![]() )和1.2 mol•L-1硝酸10
mL;b是未充气且放有0.384 g Cu粉的气球;C是夹紧的弹簧夹;d是盛有足量Na2O2的干燥管;e是充有CO2的注射器,整套装置不漏气。
)和1.2 mol•L-1硝酸10
mL;b是未充气且放有0.384 g Cu粉的气球;C是夹紧的弹簧夹;d是盛有足量Na2O2的干燥管;e是充有CO2的注射器,整套装置不漏气。
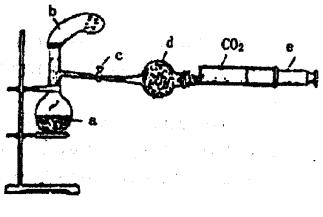
(1)将气体b中的Cu粉小心倒入烧瓶中,要使Cu粉发生反应,是否一定需要对反应混合物进行加热(填“是”或“否”) ,发生反应的化学方程式是 ;充分反应后Cu粉有剩余,在反应过程中可观察到的现象是:① ,② ,③ ,④ ;
(2)欲加快铜与硝酸的反应速率,可采用多种不同的措施,若采用化学试剂法,下列试剂中可以使用的是(填代号) ;
A.蒸馏水 B.无水醋酸钠 C.石墨 D.AgNO3(少量)
(3)将烧瓶不断振荡,发现气球逐渐变小,直至被吸入烧瓶内,发生这一现象的原因是(用化学方程式表示) 。
(4)打开弹簧夹将CO2推入干燥管内继续振荡,使气体与气体、气体与液体间充分接触,可使剩余铜粉完全溶解,上述整个过程用一个总化学方程式表示则为:
,在此过程中,至少需要CO2
mL。(标准状况)
查看答案和解析>>
科目: 来源: 题型:058
以六水合氯化镁(MgCl2•6H2O)为原料制备无水氯化镁。已知:MgCl2•6H2O晶体在空气中加热时,释出部分结晶水,同时生成Mg(OH)Cl或MgO;在干燥HCl气流中加热能制得无水MgCl2。
可选用的药品:MgCl2•6H2O晶体、NaCl(固)、KClO3(固)、MnO2、浓H2SO4、浓HCl、稀NaOH溶液。
仪器:见下图(装置可重复使用)。

回答下列问题:
(1)组装氯化氢气体发生器,应选用的仪器(用编号A、B…填入)是 ,有关的化学方程式是 ;
(2)按HCl气流方向,其余装置的连接顺序(用数字1、2…填入)是:( )→( )( )→( )( )→( )( );
(3)各装置中应放的药品:A B C D E ;
(4)B装置的作用是 ,B中能观察到的现象是 。
查看答案和解析>>
科目: 来源: 题型:058
(1)若CO2中混有CO,除去的方法是 ;
(2)若CO2中混有HCl,要得到纯净的CO2,其方法是 ;
(3)将镁条在空气中点燃后伸入装有纯净CO2的集气瓶中,能观察到的现象是(不必写产物的名称或分子式) ;
(4)在没有现成的CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置,应选用的仪器是(填入编号) ;

(5)若用上述装置发生CO2气体,而实验室只有稀硫酸、浓硝酸、水、块状纯碱、块状大理石,比较合理的方案,应选用的药品是 。
查看答案和解析>>
科目: 来源: 题型:058
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在,实验室里从海藻中提取碘的流程如下图:

(1)指出提取碘的过程中有关的实验操作名称:① ③ ;写出过程②中有关反应的离子方程式
(2)提取碘的过程中,可供选择的有机试剂是
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(3)为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是
(4)从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏,指出下列实验装置中的错误之处:
① ;
② ;
③ 。

(5)进行上述蒸馏操作时,使用水浴的原因是 最后晶体碘在 里聚焦。
查看答案和解析>>
科目: 来源: 题型:058
用下列仪器和药品制取氨气,并利用氨气和加热的氧化铜的反应来试验氨气是否具有还原性。通过实验发现:(1)氨具有还原性;(2)氨作还原剂时,生成物中有水;(3)氨作还原剂时,生成物中还有一种无色无味、遇空气不变色的纯净气体。
实验中使用的仪器如下:

实验中所需药品:a.消石灰 b.碱石灰 c.浓H2SO4 d.氯化铵 e.氧化铜 f.无水硫酸铜
(1)实验装置的各种仪器的连接顺序按各接口的代码字母填入( )中。并将相应仪器中所装的化学药品的代码字母填入[ ]中(有的仪器可重复使用)
( )接( ),( )接( ),( )接( ),( )接( )
[ ] [ ] [ ] [ ] [ ]
(2)氨与氧化铜反应的化学方程式为 。
(3)实验中可以证明氨具有还原性的最明显的现象是 。
(4)如果实验过程中未发现有水蒸气冷凝后形成的水珠,则证明氨作还原剂时生成物中有水的理由是 。
(5)证明生成的气体不是NO的简易方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com