
科目: 来源:安徽省舒城皖智高考复读学校2012届高三12月第一次旬考化学试题 题型:058
将2.5 g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1 mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:

(1)写出OA段所发生反应的离子方程式________、________.
(2)当加入35 mL盐酸时,产生CO2的体积为________mL(标准状况).
(3)原混合物中NaOH的质量为________g,碳酸钠的质量分数为________.
查看答案和解析>>
科目: 来源:安徽省舒城皖智高考复读学校2012届高三12月第一次旬考化学试题 题型:058
硫酸亚铁晶体
(FeSO4·7H2O)在医药上作补血剂.某课外小组测定该补血剂中铁元素的含量.实验步骤如下:
请回答下列问题:
(
1)步骤②加入过量H2O2的目的:________.(
2)步骤③中反应的离子方程式:________.(
3)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量.(
4)若实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示).(
5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定.(5Fe2++MnO4-+8H+![]() 5Fe3++Mn2++4H2O)
5Fe3++Mn2++4H2O)
①
实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需________.②上述实验中的
KMnO4溶液需要酸化,用于酸化的酸是________.a.
稀硝酸b.
稀硫酸c.
稀盐酸d.
浓硝酸③某同学设计的下列滴定方式中,最合理的是________ (夹持部分略去)(填字母序号)

(
6)正常人每天应补充14 mg左右的铁.其中绝大部分来自于食物.如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用________片含FeSO4·7H2O的片剂.查看答案和解析>>
科目: 来源:河北省衡水中学2011-2012学年高二上学期期中考试化学试题 题型:058
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.已知:

①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用是________;若用
同位素18O示踪法确定反应产物水分子中氧原子的提供者,
写出能表示18O位置的化学方程式:________.
(2)球形干燥管C的作用是________,若向反应前D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是________.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出________,再加入(从下列选项中选择)________,然后进行蒸馏,
收集________℃左右的馏分,以得到较纯净的乙酸乙酯.
A.五氧化二磷
B.碱石灰
C.无水硫酸钠
D.生石灰
查看答案和解析>>
科目: 来源:广东省佛山一中2011-2012学年高二上学期期中考试化学理科试题 题型:058
一定温度下,在一固定体积的容器中,通入一定量的CO和H2O,发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0
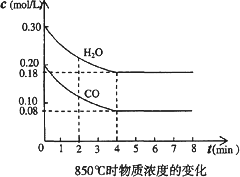
(1)在850℃时,CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO2)=________mol·L-1·min-1
(2)t1℃时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:

①计算t1℃该反应的平衡常数为k=________,t1℃________850℃(填“大于”、“小于”或“等于”).判断依据是:________.
②t1℃时,反应在4 min~5 min间,平衡________移动(填“向左”、“向右”或“不移动”),可能的原因是________.
a.增加CO的浓度
b.增加H2的浓度
c.加压
d.使用催化剂
(3)t2℃时,反应CO2 (g)+H2(g)![]() CO(g)十H2O(g)的平衡浓度符合c(CO2)·c(H2)=2c(CO)·c(H2O),则t2℃________850℃(填“大于”、“小于”或“等于”).
CO(g)十H2O(g)的平衡浓度符合c(CO2)·c(H2)=2c(CO)·c(H2O),则t2℃________850℃(填“大于”、“小于”或“等于”).
查看答案和解析>>
科目: 来源:河南省偃师市高级中学2011-2012学年高一第一次月考化学试题 题型:058
实验室用需配制250 mL 0.1 mol/L的Na2CO3溶液,填空并请回答下列问题:
(1)配制250 mL 0.1 mol/L的Na2CO3溶液

(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)________;
A.用30 mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B.用天平准确称量Na2CO3固体放入烧杯中,再加入少量水(约50 mL),用玻璃棒慢慢搅动,使其溶解
C.将已冷却的溶液沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1-2 cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是________.
(4)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作________;若定容时俯视刻度线________.
(5)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度________.
查看答案和解析>>
科目: 来源:山东省莱州一中2012届高三上学期模块检测化学试题 题型:058
甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加执装置已略,气密性已检验)

实验操作和现象:

(1)A中反应的化学方程式是________.
(2)C中白色沉淀是________.
(3)C中液面上方生成红棕色气体的化学方程式是________.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲同学认为是空气中的氧气参与反应,乙同学认为是白雾(硫酸酸雾)参与反应.
①为证实各自的观点,在原实验基础上;
甲同学在原有操作之前通N2一段时间,目的是________.乙同学在A、B间增加盛有饱和NaHSO3溶液的洗气瓶D,D中反应的离子方程式是________.
②各自进行实验,B中现象:
![]()
用离子方程式解释乙同学观察到的实验现象________(不必配平).
(5)若将(4)中两同学的方案进行联合试验,发现B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是________.
查看答案和解析>>
科目: 来源:山东省莱州一中2012届高三上学期模块检测化学试题 题型:058
实验室以食盐、二氧化碳、氨气为原料模拟生产纯碱,该实验先制得NaHCO3,进而制取纯碱.主要装置如下:

请回答下列问题:
(1)A中发生反应的离子方程式为________;B中所盛的溶液为________.
(2)D装置用来产生NH3,则固体D可以是(只填一种________;C装置中球形漏斗的作用是________.
(3)向C中通人气体时,应先通________,理由是________.C中反应的总的化学方程式为________.
(4)C中分离出的NaHCO3晶体可能含有的杂质有________,用该NaHCO3晶体制取纯碱时,有的杂质不会影响纯碱的纯度.原因是________(用化学方程表示).
(5)写出用NaHCO3制取纯碱的化学方程式________.
查看答案和解析>>
科目: 来源:山东省潍坊市三县2011-2012学年高一上学期模块学分认定检测化学试题 题型:058
实验是进行化学研究的重要手段之一.请回答下列问题:
(1)下列实验操作,错误的是________(填写序号).
a.用纸槽往试管里装粉末状药品时,试管应先横放再直立
b.称取氢氧化钠固体时,应将氢氧化钠固体直接放在左边托盘内,右边托盘放砝码
c.试管、烧杯、量筒、集气瓶都不能用酒精灯直接加热
d.用试纸检验气体性质时,手拿着试纸经水润洗后靠近气体观察试纸颜色的变化
e.闻气体气味时,应取一瓶盛满气体的集气瓶,稍打开玻璃片,用手轻轻扇地在瓶口扇动,使极少量的气体飘进鼻孔,闻气味
(2)实验室需要450 mL 0.1 mol·L-1 NaOH溶液和500 mL 0.5 mol·L-1硫酸溶液.请回答下
列问题:
①在下图所示仪器中,配制上述溶液肯定不需要的是________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有________.

②在容量瓶的使用方法中,下列操作正确的是________(填写序号).
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流注入容量瓶中,然后加蒸馏水.
d.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀.
③配制450 mL 0.1 mol·L-1 NaOH溶液的实验步骤如下:
a.计算应称取氢氧化钠固体的质量为________g.
b.称量氢氧化钠固体.
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶.
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却.
e.盖好瓶塞,反复上下颠倒,摇匀.
f.继续向容量瓶中加蒸馏水至刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切.
上述步骤的正确操作顺序为________(用序号表示).
④根据计算得知,需用量筒量取质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为________mL,如果实验室有15 mL、20 mL、50 mL量筒,应选用________mL量筒最好.
查看答案和解析>>
科目: 来源:四川省成都市六校协作体2011-2012学年高一上学期期中考试化学试题 题型:058
下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题

(1)该浓盐酸中HCl的物质的量浓度为________mol/L.
(2)配制250 mL 0.1 mol/L的盐酸溶液
A.用量筒量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入蒸馏水,用玻璃棒慢慢搅动,使其混合均匀.
B.将已冷却的盐酸沿玻璃棒注入容量瓶中.
C.用蒸馏水洗涤________2-3次,洗涤液均注入容量瓶,振荡.
D.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处,改用________加水,使溶液凹面恰好与刻度相切.
E.将容量瓶盖紧,振荡,摇匀.
(3)若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水________;
②向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,则浓度________;
③定容时俯视容量瓶刻度线________.
(4)实验室里迅速制备少量氯气可利用以下反应:
2KMnO4+16HCl![]() 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O
此反应不需要加热,常温下就可以迅速进行.
①用“双线桥法”标明电子转移的方向和数目:
2KMnO4+16HCl![]() 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O
②用该浓盐酸制得了标况下560 ml Cl2,则被氧化的HCl为________mol,需要KMnO4的质量________g
查看答案和解析>>
科目: 来源:云南省建水一中2011-2012学年高二上学期期中考试试化学文科试题 题型:058
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质.A中发生反应的化学方程式:
2NH4Cl+Ca(OH)2
(1)A中的反应________(填“是”或“不是”)氧化还原反应;
(2)A装置还可用于制取气体________(只填一种);
(3)实验室收集氨气的方法是________;
(4)C、D装置中颜色会发生变化的是________(填“C”或“D”);
(5)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是________(填“F”或“G”);
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴人1-2滴浓盐酸,可观察到的现象是________;
(7)2010年11月9日晚,我省一冷冻厂发生氨气泄漏事件,500多居民深夜大转移.假如你在现场,你会采用什么自救为法?________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com