
科目: 来源:宁夏中卫市海原一中2011-2012学年高二第一学段考试化学试题 题型:022
| |||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省杭州二中2011-2012学年高二上学期期中考试化学试题 题型:022
A、B、C为三种链烃,其碳原子数有如下组合:

试回答下列问题:
(1)若B、C为烷烃,且在一定条件下C可裂化为A和B,则其可能的组别为________.
(2)若A为烷烃,B、C各为烯烃和炔烃,将三者等物质的量混合后,各取1 mol的混合物完全燃烧,生成的水的质量相等的组别为________.
(3)若⑥组中A是烷烃、B是炔烃、C是烯烃且按物质的量1∶1∶2混合,取标准状况下该混合物和过量O2的混合气体840 mL点燃,将燃烧后的气体用过量碱石灰吸收,碱石灰增重0.93 g.求:碱石灰吸收后所剩气体的体积(标准状况下).
查看答案和解析>>
科目: 来源:浙江省杭州二中2011-2012学年高二上学期期中考试化学试题 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
科目: 来源:广东省翠园中学2011-2012学年高二上学期期中考试化学试题 题型:022
现有下列各化合物:

①上述化合物中的含氧官能团是(写名称)________、________、________、________;
根据官能团的特点可将C中两化合物划分为________类和________类.
②D中两化合物的名称分别是________;________.
③上述化合物中属于同分异构体的是________属于同系物的是________.
查看答案和解析>>
科目: 来源:山东省济宁市梁山二中2011-2012学年高二上学期期中考试化学试题 题型:022
一定温度下
,将2 mol SO2气体和1 mol O2气体通过一密闭容器中,发生如下反应:2SO2(g)+O2(g)若容器体积固定为2 L,反应1 min时测得剩余1.2 mol SO2,SO3的浓度为0.4 mol/L.
①1 min
内,O2的平均反应速率为________;②若反应经2 min达到平衡,平衡时
SO3的浓度________0.8 mol/L(填“大于”、“等于”或“小于”);③改变起始物质加入的量,欲使反应达到平衡时SO3的物质的量分数与原平衡相等,起始加入的三种物质SO2、O2、SO3的物质的量a、b、c之间应满足的关系式________;________.
查看答案和解析>>
科目: 来源:福建省南安一中2011-2012学年高一上学期期中考试化学试题 题型:022
电解原理在化学工业中有广泛应用.右图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)X的电极名称是________(填写“阳极”或“阴极”).
(2)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是________,Y电极的材料是________.
(3)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是________,Y极上的电极反应式为________.
(4)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是________.

查看答案和解析>>
科目: 来源:江苏省盐城中学2011-2012学年高二上学期期中考试化学试题(选修) 题型:022
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
(1)电解饱和食盐水的化学方程式为________.
(2)
常温下,某化学兴趣小组在实验室中,用石墨电极以下图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L.(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)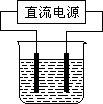
①
理论上,电解后溶液中c(OH-)=________mol/L.②若实际测得反应后溶液的
c(OH-)=0.1 mol/L,则造成这种误差的原因可能是:a.
可能为________(用离子方程式表示).b.2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
查看答案和解析>>
科目: 来源:山东省郓城一中2011-2012学年高二上学期模块考试化学试题 题型:022
电解原理在化学工业中有着广泛的应用.
现将你设计的原电池通过导线与下图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:

①若X和Y均为惰性电极,a为CuSO4溶液则阳极的电极反应式为________,电解时的化学反应方程式为________,通过一段时间后,向所得溶液中加入0.2 mol CuO粉末,恰好恢复到电解前的浓度和pH,则电解过程中转移的电子的物质的量为________.
②若X、Y分别为铁和铜,a仍为CuSO4溶液,则Y极的电极反应式为________
③若用此装置电解精炼铜,________做阳极,电解液CuSO4的浓度________(填“增大”、“减小”或“不变”).
④若用此装置在铁制品上镀铜,铁制品做________,电镀液的浓度________(填“增大”、“减小”或“不变”).
查看答案和解析>>
科目: 来源:山东省德州一中2011-2012学年高二模块检测化学试题 题型:022
采用惰性电极从NO![]() 、SO
、SO![]() 、Cl-、Cu2+、Na+、Ag+、H+选出适当离子组成的电解质(非熔融态下),并电解其水溶液
、Cl-、Cu2+、Na+、Ag+、H+选出适当离子组成的电解质(非熔融态下),并电解其水溶液
(1)若两极分别放出H2和O2,电解质可能为________.
(2)若阴极析出金属,阳极放出O2,电解质可能为________.
(3)若两极分别放出气体,且体积比为1∶1,电解质可能为________.
(4)若既无O2也无H2放出,则电解质可能为________.
查看答案和解析>>
科目: 来源:河北省唐山一中2011-2012学年高二上学期第二次调研考试化学试题 题型:022
如图所示的实验装置,丙为用淀粉碘化钾和酚酞混合溶液润湿的滤纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A、B两极产生的气体体积之比为2∶1,回答下列问题:

(1)M溶液可能是________(填序号).
A.KNO3溶液
B.Ba(OH)2溶液
C.H2SO4溶液
D.NaCl溶液
E.CuSO4溶液
(2)C极的电极反应式为________.
(3)滤纸丙的m端发生的现象为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com