
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
在某一化学反应中,反应物A的浓度在10 min内从4.0 mol·L-1变为1.0 mol·L-1.在这10 min内A的化学反应速率为________.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
仔细观察NaCl及CsCl的晶体模型,完成下列填空.
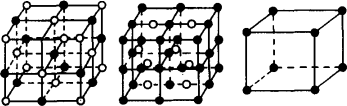
(1)在NaCl晶体中每个Na+周围同时吸引着________个Cl-,每个Cl-周围同时吸引着________个Na+.
(2)CsCl晶体中:每个Cs+周围同时吸引着________个Cl-,每个Cl-周围同时吸引着________个Cs+.
在NaCl、CsCl晶体中________单个的NaCl与CsCl分子,阴阳离子的个数比是________.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
1985年科学家发现的C60是由60个碳原子构成的,它的形状像足球,因此又称为“足球烯”.1991年,科学家又发现了一种碳的单质——碳纳米管,它是由六边形环形成的碳原子构成的管状分子(结构见教材中).应用我们所学的知识回答下列问题:
(1)金刚石、石墨、足球烯、碳纳米管物理性质有较大差异的原因是________.
(2)常温下足球烯和碳纳米管的化学性质是否活泼?________(答“是”或“否”),其理由是________.
(3)请设计一个实验方案,证明足球烯和碳纳米管都是由碳元素组成的:________.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
已知元素的电负性和原子半径一样,也是元素的一种基本性质.下面给出14种元素的电负性:

试结合元素周期律知识完成下列问题:
根据上表数据可推知元素电负性的变化规律是________.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
下列物质中含有共价键的是________,含有离子键的是________,离子化合物是________,共价化合物是________,微粒间只存在共价键的是________,只存在离子键的是________,既存在离子键又存在共价键的是________,不存在化学键的是________.
①NaOH;②NH4Cl;③O2;④CaO;⑤KI;⑥H2S;⑦CH3CH2OH;⑧SO2;⑨CO2;⑩SiO2;![]() Ar;
Ar;![]() K2SO4.
K2SO4.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
砷化镓(GaAs)是一种半导体材料,Ga、As位于元素周期表的ⅢA族、ⅤA族.
(1)Ga原子、As原子最外层电子数分别是________、________.
(2)GaAs中Ga、As的化合价分别是________、________.
(3)ⅣA族中的C和Si也可以形成与GaAs类似的化合物,该化合物也能作为半导体材料.试推断该化合物的化学式为________.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
SiC和CO2分子中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且易汽化.由此可判断,CO2是________晶体,而SiC可能是________晶体.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
BaCl2是无色晶体,熔点963℃,沸点1 560℃,溶于水,水溶液能导电,它可能属于________晶体.
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
A、B、C、D、E五种元素,它们的质子数依次递增,但都小于18.A元素原子核外只有1个电子.B元素原子和C元素原子最外层电子数之差为2.B元素原子L层上的电子数为K层电子数的2倍.B、C、D三种元素可以形成化学式为D2BC3的化合物,其焰色反应为黄色.0.5 mol E元素的单质与足量的稀盐酸反应有9.03×1023个电子转移.E和C的化合物中,E的质量占52.94%.又已知E的原子核中有14个中子.
(1)写出五种元素的名称.
A________,B________,C________,D________,E________.
(2)画出D原子结构示意图:________;
画出E离子的结构示意图:________.
(3)BC2的电子式为________,BA4的结构式为________.
(4)五种元素中原子半径最小的是________,金属性最强的是________(填元素符号).
查看答案和解析>>
科目: 来源:新课程模块教与练·高中化学必修2(苏教版) 苏教版 题型:022
| |||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com