
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
pH的定义
用[H+]的负对数来表示溶液的酸碱性的强弱,即:pH=________.
由于当[H+](或[OH-])的浓度小于或等于1 mol·L-1时,应用不方便,故引入pH,pH的范围是________.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
探究溶液的酸碱性的实质
在酸或碱溶液中,水的电离平衡被破坏.当加酸时,使水的电离平衡向________移动,致使溶液中[H+]________[OH-],溶液呈酸性;当加碱时,使水的电离平衡向________移动,致使溶液中[H+]________[OH-],溶液呈碱性.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
水的离子积
水的电离是一个________过程,在一定条件下可以达到________,平衡常数为:K=________.
由上式可得:K·[H2O]=________.在一定温度下,K与[H2O]都是常数,其乘积也必然是常数,因此________也是常数,即:Kw=________,式中的Kw称为水的________,简称水的________.Kw反映了水中[H+]和[OH-]的关系.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
水的电离及其电离方程式
有人测量了经过多次纯化处理所制得的水的电导率值,结果不为零.这证明水是极弱的________,它能发生微弱的电离,纯水中存在能________的离子,经分析知道它们是________和________.其电离方程式为:H2O![]() ________.
________.
水的电离特点:(1)由水分子电离出的H+和OH-数目相等.
(2)水的电离过程是可逆的、吸热的.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
牙齿表面由一层硬的成分为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:Ca5(PO4)3OH(s)![]() 5Ca2++3PO
5Ca2++3PO![]() +OH-.进食后,细菌和酶作用于食物,产生有机酸,这时牙齿会受到腐蚀,其原因是________________.已知Ca5(PO4)3F(s)的溶解度比Ca5(PO4)3OH更小,质地更坚固.请用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因是________________.根据以上原理,请提出另外一种促进矿化的方法:________________.
+OH-.进食后,细菌和酶作用于食物,产生有机酸,这时牙齿会受到腐蚀,其原因是________________.已知Ca5(PO4)3F(s)的溶解度比Ca5(PO4)3OH更小,质地更坚固.请用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因是________________.根据以上原理,请提出另外一种促进矿化的方法:________________.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
植物进行光合作用的化学反应方程式可表示为6CO2+12H2O![]() C6H12O6+6H2O+6O2.某科研单位把气体中CO2的浓度提高3~5倍,O2的浓度尽量减小,结果可以取得良好的增产效果.其原因是________________.
C6H12O6+6H2O+6O2.某科研单位把气体中CO2的浓度提高3~5倍,O2的浓度尽量减小,结果可以取得良好的增产效果.其原因是________________.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
取a mol A和b mol B置于V L容器内发生可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g).1 min后测得容器中A的浓度为x mol·L-1,则C的浓度为________,以A的浓度表示该反应速率为________.
cC(g)+dD(g).1 min后测得容器中A的浓度为x mol·L-1,则C的浓度为________,以A的浓度表示该反应速率为________.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
在容积相同的不同密闭容器中,分别充入等量N2和H2,在不同温度下,发生反应N2+3H2![]() 2NH3,并分别在t s时测定其中NH3的体积分数并绘成如图所示曲线.
2NH3,并分别在t s时测定其中NH3的体积分数并绘成如图所示曲线.
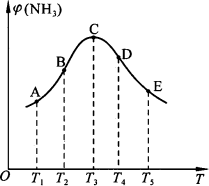
(1)A、B、C、D、E五点中,尚未达到化学平衡状态的点是________.
(2)此可逆反应的正反应是________反应(填“放热”或“吸热”).
(3)A~C段曲线是增函数曲线;C~E段曲线是减函数曲线.试从化学反应速率和化学平衡的角度说明理由:________________.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
N2+3H2![]() 2NH3(正反应为放热反应)生产中:
2NH3(正反应为放热反应)生产中:
(1)充入H2、N2的体积比控制在略小于3∶1的理由是________________;
(2)温度控制在500℃左右的原因是________________;
(3)平衡时测定的浓度[H2]=9 mol·L-1、[N2]=3 mol·L-1、[NH3]=2 mol·L-1,则起始浓度c(H2)=________mol·L-1,c(N2)=________mol·L-1.
查看答案和解析>>
科目: 来源:新课程同步学案专家伴读 化学选修4(化学反应原理) 鲁科版 鲁科版 题型:022
N2+3H2![]() 2NH3是正反应为放热反应的平衡体系.欲提高H2的转化率,应采取的办法是:(1)________________;(2)________________;(3)________________.
2NH3是正反应为放热反应的平衡体系.欲提高H2的转化率,应采取的办法是:(1)________________;(2)________________;(3)________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com