
科目: 来源:北京市四中2011-2012学年高二上学期期中考试化学试题 题型:022
H2S溶于水的电离方程式为________.
(1)向H2S溶液中加入浓盐酸时,电离平衡向________移动,c(H+)________(填增大、减小、不变),c(S2-)________(填增大、减小、不变).
(2)向H2S溶液中加入NaOH固体,电离平衡向________移动,c(H+)________(填增大、减小、不变),c(S2-)________(填增大、减小、不变).
(3)若要使H2S溶液中c(HS-)增大,且使H2S的电离平衡逆向移动,可以加入________.
(4)向H2S溶液中加水,c(HS-)________(填增大、减小、不变),溶液pH________(填增大、减小、不变)
查看答案和解析>>
科目: 来源:北京市四中2011-2012学年高二上学期期中考试化学试题 题型:022
在一定条件下,反应xA+yB![]() zC达到平衡:
zC达到平衡:
(1)若A、B、C均为气体,则该反应的平衡常数表达式为________;
(2)若A、B、C均为气体,减压后平衡向逆反应方向移动,则x、y、z间的关系是________;
(3)若已知C是气体,且x+y=z,在增大压强时,若平衡发生移动,则一定向________(填“正”或“逆”)反应方向移动;
(4)已知B、C是气体,当其他条件不变时,增大A的物质的量,平衡不移动,则A为________态;
(5)加热后C的质量分数减少,则正反应是________(填“放热”或“吸热”)反应.升高温度达到新的平衡后,该反应的平衡常数将变________(填“大”或“小”)
查看答案和解析>>
科目: 来源:北京市四中2011-2012学年高二上学期期中考试化学试题 题型:022
通常状况下,下列物质中①硫酸钡;②醋酸;③氯化氢;④三氧化硫;⑤氯气;⑥碳酸氢钠;⑦铜;⑧硫酸溶液;⑨氢氧化钾;⑩乙醇(下列各空填序号)
(1)属于强电解质的是:________
(2)属于弱电解质的是:________
(3)能导电的是:________
(4)属于非电解质的是:________
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第3讲 化学键(鲁科版) 题型:022
共价键都有键能之说,键能是指拆开1 mol共价键所需要吸收的能量.如H-H键的键能是436 kJ/mol,是指使1 mol H2分子变成2 mol H原子需吸收436 kJ的能量.
(1)已知H-Cl键的键能为431.4 kJ/mol,下列关于键能的叙述正确的是________.
A.每生成1 mol H-Cl键放出431.4 kJ能量
B.每生成1 mol H-Cl键吸收431.4 kJ能量
C.每拆开1 mol H-Cl键放出431.4 kJ能量
D.每拆开1 mol H-Cl键吸收431.4 kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是________.

A.HF
B.HCl
C.HBr
D.H2
(3)能用键能大小解释的是________.
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知Cl-Cl键的键能是243 kJ/mol,试求1 mol H2在足量的Cl2中燃烧,理论上放出的热量是________(其他形式的能量很少,可忽略不计).
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第3讲 化学键(鲁科版) 题型:022
氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3.请回答下列问题:
(1)Na3N的电子式是________,该化合物是由________键形成的.
(2)Na3N与盐酸反应生成________种盐,其电子式分别是________.
(3)Na3N与水的反应属于________(填基本反应类型)反应.
(4)比较Na3N中两种微粒的半径:r(Na+)________r(N3-)(填“>”、“=”或“<”).
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第2讲 元素周期表 元素周期律(鲁科版) 题型:022
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:

(1)④、⑤、⑥的原子半径由大到小的顺序是________.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是________.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:________.
(4)由表中两种元素的原子按1∶1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)________.
a.MnO2
b.FeCl3
c.Na2SO3
d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
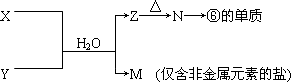
X溶液与Y溶液反应的离子方程式为________,N→⑥的单质的化学方程式为________,常温下,为使0.1 mol·L-1 M溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第1讲 原子结构(鲁科版) 题型:022
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素.Y的单质在W2中燃烧的产物可使品红溶液褪色.Z和W元素形成的化合物Z3W4具有磁性.U的单质在W2中燃烧可生成UW和UW2两种气体.X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体.
请回答下列问题:
(1)V的单质分子的结构式为________;XW的电子式为________;Z元素在周期表中的位置是________.
(2)U元素形成的同素异形体的晶体类型可能是(填序号)________.
①原子晶体
②离子晶体
③分子晶体
④金属晶体
(3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式)________;V、W的氢化物分子结合H+能力较强的是(写化学式)________.用一个离子方程式加以证明________.
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为________.由此可知VW和YW2还原性较强的是(写化学式)________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第1讲 原子结构(鲁科版) 题型:022
通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答:
(1)用化学符号表示下列4种微粒:
A:________;B:________;C:________;D:________.
(2)写出A、B、E三种微粒反应的离子方程式:________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第5章 第1讲 原子结构(鲁科版) 题型:022
设X、Y、Z代表3种元素.已知:
①X+和Y-两种离子具有相同的电子层结构;
②Z元素原子核内质子数比Y原子核内质子数少9个;
③Y和Z两种元素可以形成4核42个电子的负一价阴离子.
据此,请填空:
(1)写出X、Y、Z三种元素的名称X________,Y________,Z________.
(2)写出X、Y两种元素最高价氧化物对应水化物相互反应的离子方程式:________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第4章 第4讲 金属材料复合材料(鲁科版) 题型:022
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价为+1、+2.已知Cu2O与稀硫酸反应,溶液呈蓝色.现向Cu、Cu2O和CuO组成的混合物中,加入1 L 0.6 mol·L-1 HNO3溶液恰好使混合物溶解,同时收集到2240 mL NO气体(标准状况).请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式________.
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为________.
(3)若混合物中含0.1 mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com