
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
下图中,A、B、C是三种单质,D、E、F是三种化合物.B原子和C原子最外层电子数相同.A、B、C电子层数都不大于3,且电子层数互不相同.A、C、D、E常温下是气体,A、C无毒,D、E有毒,E能使雨水pH降低.B常温下为固体,淡黄色.F常温下为液体.

试完成下列问题:
(1)写出A、B、C、D、E、F的化学式.A:________、B:________、C:________、D:________、E:________、F:________.
(2)写出D、E反应的化学方程式:________.
(3)从D开始,按其中一种元素价态升高体系,用框图表示出其单质或化合物的转化过程:
![]() ________.
________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
实验室里研究不同价态硫元素间的转化
1.二氧化硫(SO2)
(1)物理性质:通常情况下,二氧化硫________色,有________气味,比空气________,有________性,________溶于水.标准状况下,1体积水能溶解________体积二氧化硫.
(2)化学性质:二氧化硫中硫元素为+4价(中间价态),所以二氧化硫既有________又有________,二氧化硫是酸性氧化物,是________的酸酐.
①氧化性:SO2+2H2S![]() ________
________
②还原性:2SO2+O2![]() ________
________
SO2+Cl2+2H2O![]() ________
________
③酸性氧化物:与H2O、NaOH、Ca(OH)2等物质反应.
SO2+H2O![]() ________
________
④漂白性
可以使品红或其他有色物质褪色.原理是:二氧化硫能与某些有色物质化合生成不稳定的无色物质.这种无色物质受热或光照时易分解,放出SO2,恢复原来的颜色.
2.硫酸(H2SO4)
(1)物理性质:纯硫酸是________色、黏稠、________状液体,沸点________、难挥发.常用的浓硫酸质量分数是________,密度比水________.硫酸溶于水时放出大量的热.
②脱水性
浓硫酸能从一些有机物中将氢、氧两元素按H2O的组成(H∶O=2∶1)脱去.
例如:浓硫酸能使火柴棒、纸张变黑,就体现了其脱水性.
③强氧化性
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
2H2SO4(浓)+C![]() ________.
________.
常温下,冷的浓H2SO4能使Fe和Al的表面形成一层________保护膜,阻止了内部金属与H2SO4反应.这种现象叫钝化.
总结:不同价态硫元素间的相互转化
0→-2:Fe+S![]() FeS,H2+S
FeS,H2+S![]() H2S……
H2S……
0→+4:S+O2![]() SO2,S+2H2SO4(浓)
SO2,S+2H2SO4(浓)![]() 3SO2↑+2H2O
3SO2↑+2H2O
0→+6:S+6HNO3(浓)![]() H2SO4+6NO2↑+2H2O
H2SO4+6NO2↑+2H2O
-20:2H2S+SO2![]() 2H2O+3S↓,H2S+Cl2
2H2O+3S↓,H2S+Cl2![]() 2HCl+S↓……
2HCl+S↓……
-2→+4:H2S+3H2SO4(浓)![]() 4SO2+4H2O
4SO2+4H2O
-2→+6:H2S+8HNO3(浓)![]() H2SO4+8NO2+4H2O
H2SO4+8NO2+4H2O
+4→0:2H2S+SO2![]() 2H2O+3S↓
2H2O+3S↓
+4→+6:2SO2+O2![]() ________……
________……
+6→+4:Cu+2H2SO4(浓)![]() ________
________
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
广泛存在的含碳化合物
1.含碳化合物
碳元素在自然界中主要以________的形式存在,碳元素是构成化合物种类________的元素.含碳化合物的矿石常见物质如右图:
2.Na2CO3与NaHCO3
(1)碳酸钠俗称________或________,是________固体,广泛用于________等工业;碳酸氢钠俗称________,是________固体,是焙制糕点所用的________的主要成分之一.
(2)Na2CO3和NaHCO3的化学性质
由于Na2CO3、NaHCO3都属于盐,所以Na2CO3能与某些酚、碱、盐反应;NaHCO3也能与某些酸、碱、盐反应.反应的化学方程式为:与酸反应:Na2CO3+2HCl![]() ________.
________.
NaHCO3+HCl![]() ________.
________.
与碱反应:Na2CO3+Ba(OH)2![]() ________.
________.
2NaHCO3+Ba(OH)2![]() ________.
________.
与盐:Na2CO3+BaCl2![]() ________,
________,
NaHCO3+BaCl2![]() ________.
________.
(3)NaHCO3的其他性质——受热分解
NaHCO3热稳定性差,受热发生________;Na2CO3热稳定性好,受热不发生分解反应.
2NaHCO3![]() Na2CO3+________.
Na2CO3+________.
(4)碳酸盐与碳酸氢盐的相互转化
一般说来,碳酸盐能与碳酸(二氧化碳和水)反应转化为________,碳酸氢盐能与碱反应转化为________.
例:

(5)总结:Na2CO3与NaHCO3列表比较

查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
今有Ba(NO3)2、AgNO3、Fe(NO3)3的混合液,欲将Ba2+、Ag+、Fe3+分离,分别得到三种元素的不溶物,按下图所示实验:
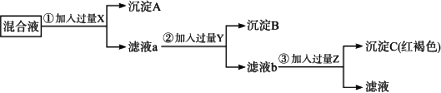
(1)加入的试剂(写化学式):X________,Y________,Z________.
生成的沉淀(写化学式):A________,B________,C________.
(2)写出反应①②③的离子方程式:①________,②________,③________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
Fe是地壳中含量很丰富的元素,也是生物体所必需的元素.自然界中铁矿石主要有赤铁矿和磁铁矿.金属铁是在高炉中高温冶炼的,高炉炼铁除了加入铁矿石外,还需加入焦炭和石灰石.请填空:
(1)写出磁铁矿主要成分的化学式:________.
(2)写出赤铁矿被一氧化碳还原成铁的化学方程式,用双线桥标出电子的得失和化合价的升降:________.
(3)加入CaCO3的目的是为了除去铁矿石中的脉石(SiO2)——使脉石转化为硅酸盐,形成矿渣而除去.写出高温下有关反应的两个化学方程式,并指出是否属于氧化还原反应:①________、________;②________、________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
探究铁及其化合物的氧化性和还原性
1.铁的存在形态:(1)游离态:如陨铁.(2)化合态:+2价铁和+3价铁.
2.铁的氢氧化物
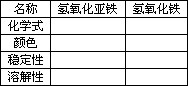
3.“铁”的五颜六色
(1)银白色:块状铁;白色:Fe(OH)2.
(2)黑色:FeO、Fe3O4、FeS.
(3)红棕色:Fe2O3;红褐色:Fe(OH)3;红色:[Fe(SCN)]2+.
(4)浅绿色:Fe2+,[Fe(SCN)]+.
(5)棕黄色:Fe3+;黄色:FeS2.
(6)灰黑色:粉状铁.
4.铁及其化合物的氧化性和还原性
(1)FeCl3的氧化性实验

(2)Fe的还原性实验

(3)FeCl2的氧化性、还原性实验

结论1:金属铁只有还原性;通常认为氯化铁只有氧化性;氯化亚铁既有氧化性,又有还原性.
结论2:金属铁、氯化铁、氯化亚铁之间的相互转化——铁三角:

查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
已知常见的强酸(H2SO4、HCl、HNO3)与常见的强碱(NaOH、KOH)生成的盐的水溶液也呈中性,如KNO3、K2SO4溶液.现将一固体粉末A加入无色中性液体中,按下图所示进行实验,其中“加C”或“加E”为滴加适量C或E溶液,恰好沉淀完全.试完成下列问题:

(1)若A是纯净物,为白色固体粉末,无色中性液体也是纯净物,则中性液体是(填化学式或名称)________,白色沉淀D是________,蓝色沉淀F是________.
(2)若A是纯净物,为白色固体粉末,无色中性液体是只含一种溶质的液体,则中性液体是________溶液或________溶液.
(3)若A是纯净物,但为另一固体粉末,无色中性液体也是纯净物,则有色溶液B与C混合时反应的化学方程式是________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
孔雀石和石青是自然界存在的两种碳酸盐类铜矿,它们的化学组成可表示为:xCuCO3·yCu(OH)2(x、y为正整数且x≤2,y≤2).
(1)孔雀石和石青分别与过量盐酸反应时,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4∶1;石青则为3∶1.请推算它们的化学组成.孔雀石:________;石青:________.
(2)现有孔雀石和石青混合样品,取两份等质量的样品,在一份中加入过量盐酸,生成CO2 3.36 L(标准状况下);加热另一份样品使其完全分解,得到CuO 20 g.试通过计算确定该混合物中孔雀石和石青的物质的量之比.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
有X、Y、Z三种元素,已知①X、Y、Z的单质在常温下均为气体;②X单质可在Z单质中燃烧,生成XZ,火焰为苍白色;③XZ极易溶于水,电离出X+和Z-,其水溶液可使蓝色石蕊试纸变红;④每2个X2分子可与1个Y2分子化合生成2个X2Y分子,X2Y在常温下为液体;⑤Z单质溶于X2Y中,所得溶液具有漂白作用;⑥细铁丝能在Z2(g)中剧烈燃烧,且产生棕褐色烟.推断X、Y、Z三种元素的名称为X________,Y________,Z________;化合物的化学式XZ________,X2Y________;6个过程中涉及的化学反应方程式为________、________、________、________.
查看答案和解析>>
科目: 来源:设计必修一化学鲁科版 鲁科版 题型:022
研究物质性质的基本程序
1.研究物质性质的基本程序
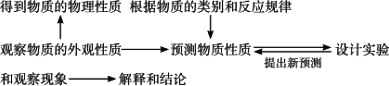
2.研究氯气的性质
(1)认识Cl2的物理性质
(2)Cl2的化学性质

(3)氯水的性质

(4)含氯化合物的漂白与消毒作用
①HClO不仅有漂白作用,还有杀菌消毒作用.次氯酸盐是常用漂白剂和消毒剂的主要成分.
2NaOH+Cl2![]() NaCl+NaClO+H2O
NaCl+NaClO+H2O
NaClO+H2O+CO2![]() NaHCO3+HClO
NaHCO3+HClO
②漂白粉的制取原理
2Ca(OH)2+2Cl2![]() CaCl2+Ca(ClO)2+2H2O
CaCl2+Ca(ClO)2+2H2O
漂白粉的失效:在空气中放置过长,就会与空气中的CO2及水蒸气反应生成HClO,HClO分解,就会导致漂白粉失效.
Ca(ClO)2+CO2+H2O![]() CaCO3↓+2HClO,2HClO
CaCO3↓+2HClO,2HClO![]() 2HCl+O2↑
2HCl+O2↑
(5)假说和模型
①假说:是以已有事实材料和科学理论为依据,面对未知事实或规律所提出的一种推测性说明.
②模型:是以客观事实为依据建立起来的,是对事物及其变化的简单模拟.
(6)现代化学实验室
①先进的新型仪器:色谱仪、质谱仪等.
②计算机化学:用计算机做实验.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com