
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
如图中A、B、C是气体发生装置,D、E、F是气体收集装置.
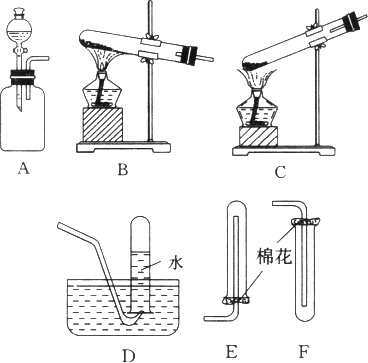
(1)若要用固态Ca(OH)2和NH4Cl制取氨气,应将________装置与________装置相连.当收集氨气的试管中充满氨气时,用蘸浓盐酸的玻璃棒靠近试管口,可以看到的现象是:________,发生的化学反应是:________.
(2)小亮和小强同学想观察NO是否真是无色的,请你帮助他们实现这个愿望:(供选用的试剂:铜片、浓硝酸)
a.制取并收集气体时,你要选择将________装置和________装置连接;
b.首先产生的是________色的________气体;
c.通过反应________(写化学反应方程式)他们可得到NO.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
工业上测量SO2、N2、O2混合气体中SO2含量的装置如图.反应管中装有碘的淀粉溶液.SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O![]() H2SO4+2HI
H2SO4+2HI

(1)混合气体进入反应管后,量气管内增加的水的体积等于________的体积(填写气体的化学式).
(2)反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量________(选填:“偏高”“偏低”“不受影响”).
(3)反应管内的碘的淀粉溶液也可以用________代替(填写物质名称).
(4)若碘溶液体积为VamL,浓度为c mol·L-1.N2与O2的体积为VbmL(已折算为标准状况下的体积).用c、Va、Vb表示SO2的体积分数为:________.
(5)将上述装置改为简易实验装置,除导管外,还需选用的仪器为________(选下列仪器的编号).
a.烧杯
b.试管
c.广口瓶
d.容量瓶
e.量筒
f.单孔塞
g.双孔塞
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
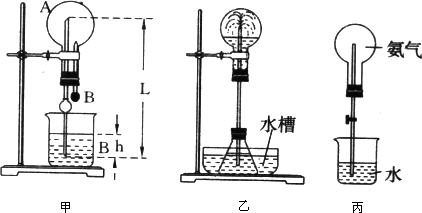
(1)在如图甲所示的装置中,烧瓶中充满干燥气体A,将滴管中的液体B挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,尖嘴管有液体呈喷泉状喷出,最终几乎充满烧瓶,下列情况满足题意的是________.
①NH3-H2O
②HCl-H2O
③CO2-4 mol/L NaOH溶液
④Cl2-饱和NaCl水溶液
⑤HCl-AgNO3溶液
⑥Cl2-淀粉碘化钾溶液
⑦Cl2-溴化钠溶液
⑧NH3-汽油
⑨NO2-H2O
⑩NH3-酚酞溶液
(2)500 mL烧瓶中充满某种气体(273 K、101325 Pa)X,烧杯中盛满水,L=30 cm,h=6 cm,气体溶解度在此状况下为1∶40.通过计算回答:如果能看到喷泉,开始时胶头滴管应先向烧瓶内注入水的体积是________mL.
(3)某学生利用氨和水做喷泉实验,(氨为该学生制备和收集),结果未能形成喷泉,请你替他分析实验不成功的可能原因?
(4)①在图乙的锥形瓶中,分别加入足量的下列物质,反应可能产生喷泉的是________
A.CaCO3和稀H2SO4
B.NH4HCO3和稀盐酸
C.Al和浓硝酸
D.NaHCO3与NaOH溶液
②锥形瓶中加入酒精,水槽中加入冷水,再加入足量下列物质,结果也产生喷泉的是
A.浓硫酸
B.食盐
C.硝酸铵
D.硫酸铜
③城市中常见的人造喷泉及火山爆发的原理与上述(填图甲或图乙)装置的原理是相同的.
(5)如果只提供如图丙的装置,请说明引发喷泉的方法:________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
某校课外活动小组为了探究铜与稀硝酸反应产物中的NO而设计了一个实验.其装置如图(加热装置和固定装置均已略去).图中K为止水夹(处于关闭状态),F是一半空的注射器,D是尾气处理装置(兼有防倒吸能力).

请回答有关问题:
(1)设计装置A的目的是________;为达此目的,应如何操作________;A中反应的化学方程式为________.
(2)在(1)中的“操作”后将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是________;B中反应的离子方程式是________.
(3)装置E和F的作用是________;为实现此作用,其操作方法是________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
用图中的简易装置可以进行气体的制取和收集.

(1)实验前应如何检查装置的气密性?
答:________.
(2)拔开试管a的橡皮塞,加入10 mL 6 mol·L-1的稀硝酸和1 g薄铜片,立即将带有导管的橡皮塞塞紧试管口,反应开始时速度缓慢,逐渐加快.请写出试管a中所发生的所有反应的化学方程式________.
(3)从反应开始到反应结束,预期在试管a中可观察到哪些现象?请依次逐一写出________.
(4)在反应开始时,可观察到导管b中的水面先沿导管b慢慢上升到一定高度,此后又回落,然后有气泡从管口冒出.试说明反应开始时,导管中水面先上升的原因________.
(5)试管c收集满气体后,用拇指堵住管口,取出水槽,将管口向上,松开拇指,片刻后,再次堵住管口,将试管又倒置在水槽中,松开拇指,此时可观察到什么现象?________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
有两个实验小组的同学为探究过氧化钠与二氧化硫的反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.

请回答下列问题:
(1)第1小组同学认为Na2O2与SO2反应生成了Na2SO3和O2,该反应的化学方程式是:________.
(2)请设计一种实验方案证明Na2O2与SO2反应生成的白色固体中含有Na2SO3.________
(3)第2小组同学认为Na2O2与SO2反应除了生成Na2SO3和O2外,还有Na2SO4生成.为检验是否有Na2SO4生成,他们设计了如下方案:

上述方案是否合理?________.请简要说明两点理由:
(1)________;
(2)________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
某化学研究小组的成员经过学习得知,Cl2与H2O发生下列化学反应,并且HClO具有比Cl2更强的氧化性.
Cl2+H2O他们为了探究新制饱和氯水的组成和性质而进行了科学实验:先观察了氯水的外观性质以后,又用胶头滴管将该氯水逐滴滴入含有酚酞的NaOH溶液中,边滴边振荡.并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液.以下的一些问题需要请你来配合回答:
(1)请写出新制饱和氯水中含有氯元素物质的化学式:________.
(2)若不再进行更多的实验,请说明能快速判断氯水中含有Cl2的主要依据:________.
(3)根据预测,实验中溶液红色褪去的原因可能有两种,请用简要的文字说明之:
①________;
②________.
(4)他们又要通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②,在此之前先做了实验预案的设计.请你简述实验的方法、现象和结论:________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
实验室用图所示装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物.

(1)如何检查装置A的气密性:________.
(2)装置A发生的反应有时要向其中加入少量硫酸铜溶液,其目的是________.
(3)为了安全,在点燃D处的酒精灯之前,在C出口处必须________.
(4)装置B的作用是________,装置C中装的液体是________,所起的作用是________.
(5)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生的化学反应方程式是________.
(6)若FeO和Fe2O3固体混合物的质量为23.2 g,反应完全后U形管的质量增加7.2 g,则混合物中Fe2O3的质量为________g.
(7)U形管E右边又连接干燥管F的目的是________,若无干燥管F,测得Fe2O3的质量将________(填“偏大”“偏小”或“无影响”).
(8)若反应后得到的残留固体中还有少量FeO,测得的Fe2O3质量将________(填“偏大”“偏小”或“无影响”).
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂.实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2遍~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50℃~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2次~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存.
请回答下列问题:
(1)实验步骤①的目的是________,加热的作用是________.
(2)实验步骤②明显不合理,理由是________.
(3)实验步骤④中用少量冰水洗涤晶体,其目的是________.
(4)经查阅资料后发现,硫酸亚铁在不同温度下结晶可分别得到FeSO4·7H2O、FeSO4·4H2O和FeSO4·H2O.硫酸亚铁在不同温度下的溶解度和该温度下析出晶体的组成如下表所示(仅在56.7℃、64℃温度下可同时析出两种晶体).

请根据上表中数据在图中作出硫酸亚铁的溶解度曲线.

(5)若需从硫酸亚铁溶液中结晶出FeSO4·4H2O,应控制的结晶温度(t)的范围为________.
查看答案和解析>>
科目: 来源:高考总复习全解 化学 一轮复习·必修课程 (人教实验版) 人教实验版 题型:058
| |||||||||||||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com