
科目: 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:058
已知:(A)Cu2+,Fe2+在pH值为4~5的条件下不水解而Fe3+却几乎全部水解;(B)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O.
用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取50毫升纯净的盐酸,加入一定量的粗CuO加热搅拌,充分反应后过滤,经测定溶液的pH值是3
②向滤液中加入双氧水,搅拌.
③向②中加入过量纯CuO,微热,搅拌,此时测定溶液的pH值为4,过滤.
④把③所得滤液浓缩.
填空:
(Ⅰ)②中发生反应的离子方程式是________.
(Ⅱ)③中过滤后滤渣的成分是____________.
(Ⅲ)①③中如何用pH试纸测定溶液的pH值:________.
(Ⅳ)③中pH值升高的原因是:________.(用离子方程式表示)
查看答案和解析>>
科目: 来源:101网校同步练习 高二化学 山东科学技术出版社 鲁教版 题型:058
为了测定乙醇的结构是 还是
还是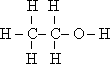 利用乙醇与钠的反应,设计如图装置实验,在烧瓶中放入足量的钠,从漏斗中缓缓滴入一定量的无水乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积.
利用乙醇与钠的反应,设计如图装置实验,在烧瓶中放入足量的钠,从漏斗中缓缓滴入一定量的无水乙醇,通过测量量筒中水的体积,就可知反应生成的氢气的体积.
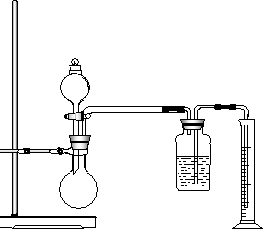
(1)检验该装置气密性的操作:________;
(2)有人认为装置中有空气,所测的气体体积应扣除装置中空气的体积,才是氢气的体积,你认为________(填“正确”或“不正确”)
(3)若用此装置来完成“验证C6H5OH、CH3COOH、H2CO3的酸性强弱”实验,分液漏斗中盛放________,烧瓶中盛放CaCO3固体,广口瓶中盛放饱和NaHCO3溶液,作用是________,上述装置还应该如何改动?(答出2点)
查看答案和解析>>
科目: 来源:101网校同步练习 高二化学 人教社(新课标B 2004年初审通过) 人教实验版 题型:058
| |||||||||||||||||||||
查看答案和解析>>
科目: 来源:101网校同步练习 高三化学 山东科学技术出版社 鲁教版 题型:058
实验室用如图所示装置制取乙酸乙酯.

(1)在大试管中配制一定比例的乙醇、乙酸和浓H2SO4的混合液的方法是_______.
(2)加热前,大试管中加入几粒碎瓷片的作用是________;导气管不能插入饱和Na2CO3溶液中是为了________.
(3)浓H2SO4的作用是:
①________________;
②________________________.
(4)饱和Na2CO3溶液的作用是________________.
(5)实验生成的乙酸乙酯,其密度比水________(填“大”“小”),有________气味.
(6)若实验中温度过高,温度达170℃,副产物中主要有机产物是________(填名称).
查看答案和解析>>
科目: 来源:2008年江苏高考化学全真模拟二 题型:058
为了测定氢氧化钠固体混合物m g中碳酸钠的质量分数,甲、乙两位同学分别设计了如下的实验方案:
(Ⅰ)甲同学的方案是:将样品溶解,加过量氯化钡溶液,过滤、洗涤、烘干,称量得固体n g.
(1)混合物中碳酸钠的质量分数为(用m、n表示)________.
(2)甲同学洗涤沉淀的操作是________________.
(3)Ca2+、Ba2+都可以使CO32-沉淀完全,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是:
①________________________;
②________________________;
(Ⅱ)乙同学的方案如图所示:

(1)根据乙同学的实验装置图分析,在每次实验中,完成测定过程至少要进行________次称量操作.
(2)他重复正确操作了三次,结果数据出现了较大的偏差,你认为主要原因可能是(任写三个):①________________________________;
②_______________________________________;
③_______________________________________.
查看答案和解析>>
科目: 来源:山东省曲阜师范大学附中2006~2007学年度第二学期期末考试、高一化学试题 题型:058
某课外活动小组设计的实验室制乙酸乙酯的装置如下图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.

已知:
①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH.
②有关有机物的沸点如下:
请回答:
(1)浓硫酸的作用是________;
(2)球形干燥管C的作用是________,反应结束后D中的现象________________.
(3)从D中分离出来的乙酸乙酯中常含有一定量的乙酸、乙醇和水,应先加入足量无水氯化钙,分离出________,然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯.
查看答案和解析>>
科目: 来源:山东省曲阜师范大学附中2006~2007学年度第二学期期末考试、高一化学试题 题型:058
某高一化学兴趣小组通过如下实验提取海带中的碘:①粉碎海带,加入一定量的氢氧化钠溶液后高温炭化;②用水浸泡海带灰,过滤;③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I-),生成碘单质;④用四氯化碳萃取水溶液中的碘.请回答下列问题:
(1)实验步骤②中所用到的主要仪器有:________(填名称).
(2)实验步骤③中相关的离子方程式为:________________.
(3)实验步骤③中也可以用H2O2代替KIO3,相关的化学方程式为:
________________________________.
(4)关于实验步骤④各项操作,下列说法正确的是:________(填选项)
A.分液前需对分液漏斗进行检漏
B.为保证分液漏斗内的液体顺利流出,可以将上口的玻璃塞打开
C.分液时,将下层液体从分液漏斗下端放出后,换一只烧杯再将上层液体从分液漏斗下端放出
D.将混合液倒入分液漏斗中不用振荡
E.从分液漏斗上口倒出上层水溶液
查看答案和解析>>
科目: 来源:大连市第八中学2006~2007学年度下学期期末考试高二化学 题型:058
乙二酸(HOOC-COOH)俗称“草酸”,常见的草酸是含有两分子结晶水的晶体.其主要物理常数如下:

某化学课外兴趣小组进行乙二酸性质的实验探究,回答下列问题:

(1)在一大试管中加入3 mL乙二醇,然后边振荡试管边加入2 mL浓硫酸和2 mL乙二酸,按图甲连接好装置,小心加热3~5 min,产生的蒸气经导气管以通到饱和Na2CO3溶液的上方.
①反应中加入过量乙二醇的目的是________________________
②饱和Na2CO3溶液的作用是________________________
(2)已知劳动日酸分解的化学方程式为H2C2O4![]() H2O+CO↑+CO2↑.图乙是加热草酸晶体,验证草酸受热分解及其产物的实验装置图,但有人认为该装置不合理.请你根据草酸晶体的某些物理常数和实验目的,指出图中两种不合理的原因.
H2O+CO↑+CO2↑.图乙是加热草酸晶体,验证草酸受热分解及其产物的实验装置图,但有人认为该装置不合理.请你根据草酸晶体的某些物理常数和实验目的,指出图中两种不合理的原因.
________________________________________________
(3)某一草酸晶体的组成可表示为H2C2O4·XH2O,为了测定X的值,进行如下实验:
①准确称取W g草酸晶体,配成100 mL溶液;②取25.00 mL所酸草酸溶液于锥形瓶中,加入适量稀硫酸,用浓度为a mol/L的KMnO4溶液滴定至终点.重复上述滴定操作三次,实验数据记录如下表所示:
![]()
已知草酸与酸性高锰酸钾反应方程式:
H2C2O4+KMnO4+H2SO4→K2SO4+MnSO4+CO2↑+H2O(未配平)
①滴定终点溶液的颜色变化为________________
②X的值为________.
查看答案和解析>>
科目: 来源:重难点手册 高中化学·必修1 配人教版新课标 人教版新课标 题型:058
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、![]() 、Cl-、Mg2+、Fe3+、
、Cl-、Mg2+、Fe3+、![]() 、
、![]() ,现每次取100.00 mL进行实验:
,现每次取100.00 mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加足量NaOH后加热,收集到气体0.896 L(标准状况下);
③第三份加足量BaCl2后,得干燥沉淀6.27 g,沉淀经足量盐酸洗涤干燥后,剩2.33 g.
试完成有关问题:
(1)判断K+、Cl-是否存在?K+________,Cl-________.(填序号)
A.一定存在 B.可能存在 C.一定不存在
(2)肯定存在的离子的原溶液中的物质的量浓度分别为________.
查看答案和解析>>
科目: 来源:重难点手册 高中化学·必修1 配人教版新课标 人教版新课标 题型:058
某学生为了验证Cl2的性质,利用如图所示甲装置制取Cl2.试回答下列问题.

(1)甲装置中,Ⅱ的作用是:①将产生的气体随取随用;②________.装置Ⅱ________(填“能”或“不能”)用乙装置来代替,原因是________.
(2)Ⅱ装置中盛有的液体是________.
(3)甲与丙连接,通入Cl2后丙装置中溶液变蓝,证明Cl2具有________,其离子方程式为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com