
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒.”“纸漏斗的下部被烧穿,有熔融物落入沙中.”又已知,Al、Fe2O3、Al2O3、Fe的熔点、沸点数据如下:

(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放热能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金,你认为他的解释是否合理?答:________(填“合理”或“不合理”).
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝.填写下列表格:

(3)实验室欲溶解此熔融物,下列试剂中最好用________(填序号),理由是:________.
A.浓硫酸
B.稀硫酸
C.稀硝酸
D.NaOH溶液
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:800 mL烧杯、100 mL量筒、短颈漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·L-1)、水.按图示装置进行实验,完成下列问题.(设合金样品完全反应,产生的气体体积不超过100 mL)

补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在800 mL烧杯底部,把短颈漏斗倒扣在样品上面.
②____________________________________.
③____________________________________.
④____________________________________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
今用铝、稀硫酸和氢氧化钠溶液为原料,实验室制备一定量的氢氧化铝.可分别采用如下化学方程式表示的两种方法:
①2Al+3H2SO4![]() Al2(SO4)3+3H2↑
Al2(SO4)3+3H2↑
Al2(SO4)3+6NaOH![]() 2Al(OH)3↓+3Na2SO4
2Al(OH)3↓+3Na2SO4
②2Al+2NaOH+2H2O![]() 2NaAlO2+3H2↑
2NaAlO2+3H2↑
2NaAlO2+H2SO4+2H2O![]() 2Al(OH)3↓+Na2SO4
2Al(OH)3↓+Na2SO4
(1)请问上述哪一种方法比较节约试剂?[提示:试从每生产2 mol Al(OH)3所耗费的试剂用量予以说明]
(2)原料相同,请设计一种更为节约试剂的方法.(以方程式表示,并说明其可以最节约试剂的根据)
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
在铝质易拉罐中收集满CO2气体,然后在其中倒入10 mL浓NaOH溶液,并迅速用胶带将易拉罐口封住,能够观察到的实验现象是易拉罐突然变瘪了,可经过一段时间之后,又可以观察到的现象是________.试解释易拉罐变瘪的原因________;并解释后一现象的原因________.写出反应过程中的两个离子方程式________;________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
实验室用下图所示实验装置制取纯净的CuCl2,完成下列问题:
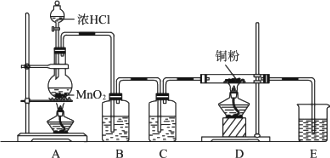
(1)实验室里,实验前检查整套装置的气密性方法是:________.
(2)装置A中发生的化学反应方程式为________.
(3)装置B的广口瓶盛________,其作用是________.装置C的广口瓶盛________,其作用是________.装置E的烧杯中盛有,其作用是________.
(4)待充分反应后,装置D的玻璃管中剩余物呈________色,冷却后,将制得的产物配成饱和溶液,溶液呈________色.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
有人设计了如图所示实验装置,目的是做钠与水反应实验并验证:①钠的物理性质;②钠与水反应的产物是什么?
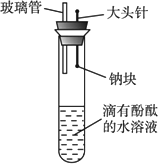
(1)当进行适当操作时还需要的仪器有__________________________.
(2)如何进行操作?___________________________.
(3)实验现象是_______________________________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
已知某氯化钾样品中含有K2SO4杂质,为了除去K2SO4杂质,设计了以下实验步骤:
(1)将KCl样品溶于适量蒸馏水,配成溶液;
(2)向溶液中滴入BaCl2溶液,边滴加边振荡至不再产生白色沉淀;
(3)向溶液中滴入K2CO3溶液,边滴加边振荡至不再产生白色沉淀;
(4)过滤,将白色沉淀滤出;
(5)向滤液中滴加稀HCl,边滴加边振荡至不再产生气体;
(6)将滤液蒸干,得到晶体.
正确的实验操作程序为________.
有关的离子方程式:________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥砂等不溶性杂质.我们食用的精盐是用粗食盐提纯而得到的.通过教材中“粗盐的提纯”及你做过的该实验回答下列问题.
(1)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热.其正确的操作顺序为________.
(2)如何运用最简便方法检验溶液中有无![]() ?________.如果有,应该如何除去
?________.如果有,应该如何除去![]() ?________.
?________.
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止.请问这步操作的目的是________.
(4)将经过操作(3)后的溶液过滤.请问这一操作能除掉哪些杂质?
________________________.
(5)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;溶解时:________.过滤时:________.蒸发时:________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
(1)配制500 mL浓度为0.2 mol·L-1的氢氧化钠溶液,需要NaOH固体________g;称量该固体时,应先在天平左盘放一________,称出其质量,再将NaOH固体置于其中称量.然后再在________里加适量水,将上述固体溶解,待________后,再转移到容量瓶定容,使溶液体积达到500 mL.
(2)在(1)实验中若其他操作均正确,但定容时俯视刻度线,则所得溶液浓度________0.2 mol·L-1(填“大于”“等于”或“小于”).
(3)在(1)实验中若NaOH溶液在转移至容量瓶中时,洒落了少许,则所得溶液浓度________0.2 mol·L-1(填“大于”“等于”或“小于”).
(4)将正确配制的上述溶液取出10 mL,其浓度为,所含Na+个数为________;将此10 mL溶液稀释至1 L,则Na+浓度为________,Na+数目为________.
查看答案和解析>>
科目: 来源:志鸿系列全优设计必修一化学苏教版 苏教版 题型:058
实验室用碳酸钠晶体配制1.00 mol·L-1的Na2CO3溶液100 mL,完成下列问题:
(1)所需主要仪器为:药匙、________、________、________、________和________.
(2)本实验需称量碳酸钠晶体(Na2CO3·10H2O)________g.
(3)容量瓶上标有________、________、________.
(4)某同学将称量好的碳酸钠晶体用适量的蒸馏水在烧杯中溶解,冷却后直接倒进所选的且经检查不漏水的容量瓶中,洗涤烧杯2-3次,洗涤液也移至容量瓶中,然后加水至离刻度线2 cm处,用滴管加水至刻度线.请指出上述操作中的3处错误:
①___________________________
②___________________________
③___________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com